Корректировка плотности электролита | Описания, разъяснения | Статьи
Зачастую, можно услышать, что если плотность электролита в источнике питания понизилась, то нужно мигом долить электролит, тем самым повысить его плотность. Также говорят, что при заряде электролит из батареи может выплескивается. Так ли это?В реальности при заряде выделяются пузырьки газа – это молекулы кислорода и водорода, т. е вода. Сера из батареи никуда не пропадает. Поэтому не стоит сразу искать электролит, чтобы увеличить его плотность. Лучше найти то, из-за чего, собственно, снижается плотность.
Включенные днем фары, магнитофон, сигнализации, обогреватели и много-много другого дополнительное оборудование не дают источнику питания полностью зарядиться, поскольку от генератора часть энергии попадает не на зарядку аккумулятора, а на обслуживание всех этих опций. Также играют роль и городской режим, при котором авто еле движется в пробках. Аккумуляторная батарея на машине нормально заряжается при быстром движении, а в пробках на холостых оборотах зарядки АкБ практически нет, вся энергия тратится на питание электроприборов машины.
Постоянный недозаряд батареи приводит к его сильной сульфатации. Определенное количество серы не растворяется, а кристаллизуется на одной из частей пластин. В этот момент образуется достаточно твердый слой сульфата свинца с большими кристаллами, который тормозит работу этой части пластин. Плотность электролита становится меньшей т.к. часть серы остается на пластинах и превращается в сложно растворимые кристаллы.
При ситуации, которая не сильно запущена, можно воспользоваться полной зарядкой аккумуляторной батареи. А лучше произвести парочку циклов заряд-разряд, при этом полностью заряжая аккумулятор.
Если Вы имеете регулируемое зарядное приспособление, то нужно его настроить на зарядный ток 0,05С номинальной емкости и производить зарядку источника питания от 12 до 72 часов. Во время зарядки нужно все время проверять плотность и уровень электролита. Для полного заряда источника питания настройка зарядного приспособления должна происходить не менее 2,65В на элемент или 15,9В для 12В батарей.
Инновационные автоматические зарядные приспособления для стартерных батарей настроены с итоговым зарядным напряжением 14,4В (2,4В на элемент), так же как настроены реле регуляторы на машинах. Такое напряжение защищает автомобиль от бурного газовыделения, но не позволяет аккумулятору зарядиться на все 100%.
По этим причинам изготовители стартерных источников питания советуют один раз в полгода проверять плотность электролита и до конца заряжать автобатарею.
Если Вы дольете электролит, то в батарее может увеличится количество серы, и соответственно плотность увеличится. Но кристаллы свинца, которые связывают пластины будут препядствовать их работе полностью. К тому же большое количество серы будет влиять на отслоение активной массы на пластинах.
ЧИТАЙТЕ ТАКЖЕ
Корректировка плотности и замена электролита
Специалисты АКБ-Сервиса в Ижевске напоминают о том, что проверку плотности электролита в аккумуляторе необходимо выполнять не реже одного раза в год.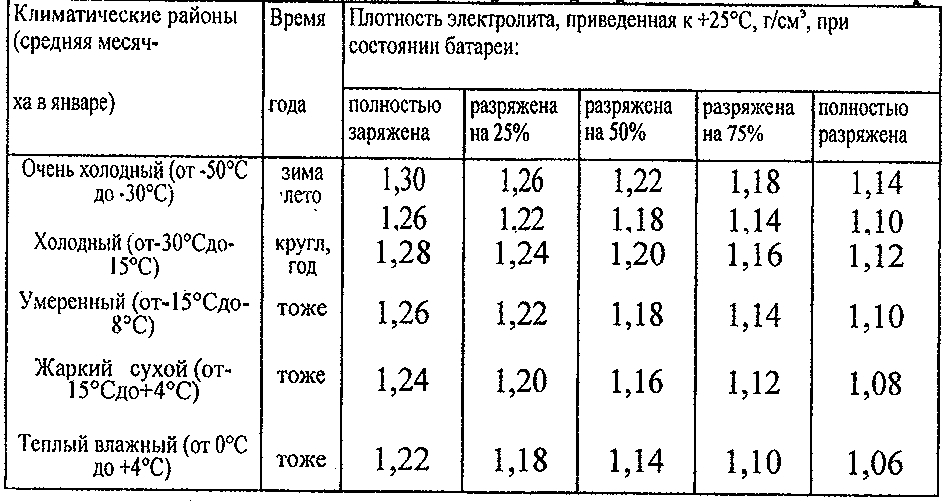 Почему изменяется плотность электролитической жидкости?
Почему изменяется плотность электролитической жидкости?
Во время скоростного движения аккумулятор получает необходимое электричество для полного заряда. Однако если вы часто двигаетесь в пробках, львиная доля электроснабжения уходит на обслуживание других электроприборов, а батарея заряжается не полностью.
В результате происходит сульфатация – частицы серы оседают, образуя плотный слой, а в самой жидкости концентрация серы уменьшается. Если ситуация не критична, поможет полная зарядка аккумулятора. Если же выпало в твердый осадок большое количество серы, необходима помощь специалистов из АКБ-Сервиса в Ижевске. Другое дело – когда плотность электролита снизилась из-за его пролива. Выяснить в чем проблема и решить ее вы можете, приехав к нам в любое удобное время.
- Мы проведем тщательную диагностику батареи, чтобы определить причину снижения плотности электролитической жидкости.
- Мы приведем плотность к нормальному состоянию (при 25 градусах 1,28+-0,01г/см3), используя технологию, которая будет эффективной и безопасной в конкретной ситуации.
- Если аккумуляторная батарея нуждается в замене электролита, мы используем качественные составы проверенных производителей.
- Если в процессе диагностики выяснится, что причиной снижения плотности является выработка батареи, корректировка плотности электролита или его доливка – не выполняются, так как это лишние расходы для наших клиентов. В таком случае мы проконсультируем по поводу покупки новой АКБ для автомобиля.
Чтобы вы могли самостоятельно контролировать плотность электролитической жидкости в аккумуляторе машины, вы можете использовать недорогой современный ареометр. Прибор прост в использовании и имеет доступную цену. Купить ареометр для электролита в Ижевске вы можете как на нашем сайте, так и непосредственно в АКБ-Сервисе.
Корректировка плотности электролита — Справочник химика 21
Корректировку плотности электролита рекомендуется проводить следующим образом. Если плотность электролита, приведенная к 25 °С, ниже требуемой, то в аккумуляторы доливают электролит плотностью 1,40 г/см , а если она выше — доливают дистиллированную воду. Сначала из аккумулятора в зависимости от имеющейся и требуемой плотности отбирают определенный объем электролита. Затем в соответствии с табл. 7.3 доливают определенное количество электролита плотностью 1,40 г/см или дистиллированной воды. И, наконец, через 30 мин проверяют плотность электролита в аккумуляторах. При нормальном ее значении доводят уровень электролита до нормы. Если разница между фактической и требуемой плотностями электролита велика, то операцию отбора—доливки повторяют три-четыре раза с интервалами между ними в 30 мин. Это необходимо для выравнивания плотности электролита в аккумуляторе. [c.99]
Сначала из аккумулятора в зависимости от имеющейся и требуемой плотности отбирают определенный объем электролита. Затем в соответствии с табл. 7.3 доливают определенное количество электролита плотностью 1,40 г/см или дистиллированной воды. И, наконец, через 30 мин проверяют плотность электролита в аккумуляторах. При нормальном ее значении доводят уровень электролита до нормы. Если разница между фактической и требуемой плотностями электролита велика, то операцию отбора—доливки повторяют три-четыре раза с интервалами между ними в 30 мин. Это необходимо для выравнивания плотности электролита в аккумуляторе. [c.99] Электролит I обладает хорошей рассеивающей способностью и позволяет осаждать медь непосредственно на железных изделиях. Однако он токсичен, требует более частой корректировки. Электро лит II прост по составу, но обладает низкой рассеивающей способностью. Применение перемешивания и подогрева в электролите II позволяет увеличить плотность тока до 10—20 а дм .

Аноды из никеля в пирофосфатном электролите пассивируются уже при низких плотностях тока и поэтому они не пригодны. Можно применять аноды из олова при анодной плотности тока 1>а до 2 а/дм с периодической корректировкой электролита по никелю или аноды из термического сплава при >а до 3 а/дм . Свойства осадков сплава 5п—Ni из пирофосфатного электролита мало отличаются от осадков, полученных из хлорид-фторидного электролита. [c.207]
Электролитический способ снятия олова с жестяных отходов получил наиболее широкое применение, особенно в небольших установках при консервных заводах для переработки обрезков белой жести (до 30% производства банок). В кислых растворах железо на аноде растворяется вместе с оловом этого можно почти полностью избежать, если ввести в раствор серной кислоты сильный окислитель, например, хромовый ангидрид, тогда можно получать довольно чистое олово иа катоде с плотностью тока до 1000 а м однако кислый электролит требует частой корректировки, приготовление его сложно, аппаратура должна быть кислотостойкой.
Важнейшими неполадками при хромировании являются неравномерное покрытие — от неравномерной плотности тока пригорелые или матовые осадки — от повышенной плотности тока при данной температуре темные полосы — от недостатка серной кислоты и от частиц шлама темные осадки — от избытка трехвалентных ионов и от низкой температуры отслаивание— от плохого обезжиривания, плохого подслоя никеля, несоответствия температуры и плотности тока наросты, бугры и углубления на толстых осадках хрома — от загрязнений в электролите и т. д. Хромовый электролит требует постоянного контроля и корректировки.
Сю ДО напряжения 1,8 в, электролит удаляется и аккумулятор доверху заполняется дистиллированной водой. Через 3—4 ч вода удаляется, аккумулятор заливается электролитом с удельным весом 1,24 и заряжается до постоянства напряжения на аккумуляторе и плотности электролита. После заряда плотность электролита корректируется. Если она меньше 1,215, корректировка производится раствором серной кислоты с удельным весом 1,3. Для этого резиновой грушей отбирается часть электролита и вместо него вводится в аккумулятор указанный раствор. После этого для перемешивания электролита заряд продолжается еше 2 ч. [c.223]
После заряда плотность электролита корректируется. Если она меньше 1,215, корректировка производится раствором серной кислоты с удельным весом 1,3. Для этого резиновой грушей отбирается часть электролита и вместо него вводится в аккумулятор указанный раствор. После этого для перемешивания электролита заряд продолжается еше 2 ч. [c.223]
Сущность этого явления заключается в том, что анод, в силу его плохой смачиваемости, обволакивается пленкой анодного газа. Плохо проводящая газовая пленка резко увеличивает сопротивление на участке анод — электролит, что приводит к резкому скачку напряжения на ванне (в 5— 10 раз больше нормального) или такому же резкому падению силы тока. При этом электролит перегревается, выход по току падает, расход материала анода и электроэнергии весьма возрастает, а генератор постоянного тока получает вредный толчок. Анодный эффект можно ликвидировать корректировкой и перемешиванием электролита, а также снижением анодной плотности тока ниже критической.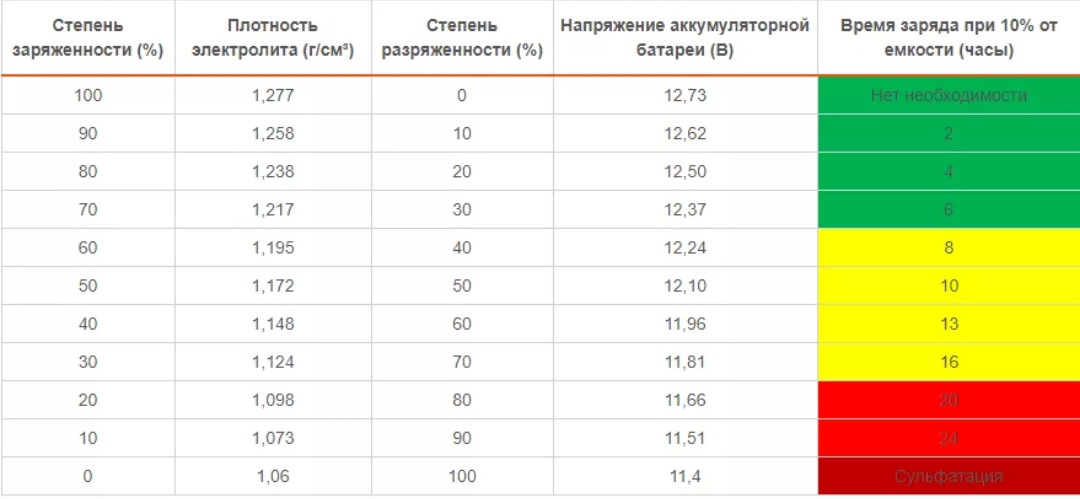
Аммиакатные (хлористые) электролиты стали применять сравнительно недавно. Эти электролиты имеют простой состав, устойчивы в работе, не требуют частой корректировки. По рассеивающей способности они подобны цинкатным и, так же как последние, применяются для замены ядовитых цианистых растворов при покрытии не очень рельефных деталей. Выход металла по току высокий и в рабочем интервале плотностей тока приближается к теоретическому. Электролиты хорошо работают при 35—40 °С. В хлор-аммиакатном электролите цинк находится в виде комплексной соли состава [2п(КНз)4]С12, которая диссоциирует с образованием комплексного катиона
К недостаткам цианистых электролитов относятся ядовитость и неустойчивость состава вследствие взаимодействия цианида натрия (калия) с СО2 из воздуха и выделения циановодорода необходимость постоянной корректировки электролита по цианиду натрия (калия) меньшая допустимая катодная плотность тока и более низкий выход по току, чем в кислом электролите склонность анодов к пассивированию. [c.35]
[c.35]
С повышением концентрации марганца в электролите до 40 г/л увеличивается его содержание в сплаве. Дальнейший рост концентрации соли марганца неблагоприятно сказывается на процессе электролиза, что объясняется значительной окисляемостью марганца на аноде. Последнее приводит к оседанию образующихся окис-ных соединений марганца на поверхности анода и ее пассированию. Отрицательным следствием этого процесса является непроизводительное снижение концентрации марганца в электролите, вызывающее необходимость частой корректировки последнего и зачистку анодов. За 12 часов работы количество марганца в электролите при исходном значении 30 г л и плотности загрузки 0,3 дм л [c.110]
С целью поддержания постоянной концентрации металла в электролите часть цинковых анодов рекомендуется заменить стальными. Плотность тока в этом случае подбирают такой, чтобы происходила пассивация только цинковых анодов, но не стальных.
 При этом распределение тока должно быть пропорционально их переходным сопротивлениям. Регулируя соотношение анодных площадей цинка и стали, можно добиться полного соответствия между анодным и катодным выходами по току и предотвратить накопление цинка в растворе. Оптимальная поверхность стальных анодов составляет 30—50% цинковых катодная плотность тока 4—8 А/дм . При необходимости более точного регулирования растворения цинковых анодов применяют анодные штанги с раздельными цепями питания, снабженными реостатом и амперметром. Цепь стальных анодов дополнительно обеспечивается прерывателем для отключения во время перерывов в работе. В противном случае образующаяся гальваническая пара Ре—2п способствует интенсивному растворению последнего. Изменяя сопротивление в анодной цепи, можно с большой точностью регулировать концентрацию ионов цинка в растворе, а своевременной корректировкой раствора по другим компонентам и тщательной очисткой от примесей создать условия, когда цинковые электролиты будут работать годами, не требуя замены.
При этом распределение тока должно быть пропорционально их переходным сопротивлениям. Регулируя соотношение анодных площадей цинка и стали, можно добиться полного соответствия между анодным и катодным выходами по току и предотвратить накопление цинка в растворе. Оптимальная поверхность стальных анодов составляет 30—50% цинковых катодная плотность тока 4—8 А/дм . При необходимости более точного регулирования растворения цинковых анодов применяют анодные штанги с раздельными цепями питания, снабженными реостатом и амперметром. Цепь стальных анодов дополнительно обеспечивается прерывателем для отключения во время перерывов в работе. В противном случае образующаяся гальваническая пара Ре—2п способствует интенсивному растворению последнего. Изменяя сопротивление в анодной цепи, можно с большой точностью регулировать концентрацию ионов цинка в растворе, а своевременной корректировкой раствора по другим компонентам и тщательной очисткой от примесей создать условия, когда цинковые электролиты будут работать годами, не требуя замены. [c.88]
[c.88]Так как в электролите содержится шестивалентный хром, выделению железа предшествует восстановление хрома до трехвалентного. Оптимальными условиями восстановления являются плотность электролита 1,7, температура 20—25° С, плотность тока катодная 0,5 А/дм , анодная 2—5 А/дм [19, 63] (табл. 4). Катодом служит свинцовая пластина анодное пространство отделяется свинцовыми дырчатыми сосудами, заключенными в стеклоткань, или керамическими пластинами. Процесс выделения железа целесообразно начинать при плотности электролита 1,7. Остаточная концентрация железа 1,0—1,5% (в пересчете на РегОз). После этого производится анодное окисление трехвалентного хрома и корректировка кислот до рабочих концентраций. [c.93]
После растворения электролит готов к эксплуатации без введения каких-либо добавок. Электролит допускает колебания концентрации серебра в пересчете на металл от 6 до 40 г л. Рабочая температура электролита 15—25°С. Осаждение серебра ведут при плотности тока = 0,2- -h0,3 а/дм . Перемешивание электролита не рекомендуется. Аноды серебряные. Выход по току т] = 100%. Электролит обладает высокой рассеивающей способностью и позволяет получать мелкокристаллические и хорошо полирующиеся покрытия. Корректировка электролита состоит в приливании сульфита натрия или в добавлении свеже-осажденного сульфита серебра. Осаждение серебра из этого электролита на детали из меди и ее сплавов требует предварительной подготовки поверхности, заключающейся либо в амальгамировании, либо в контактном серебрении. [c.29]
Электролит I обладает хорошей рассеиваюше способность о и позволяет осаждать медь непосредственно па железных изделиях. Однако ои токсичен, требует более частой корректировки, Электро- цт II прост по составу, ио обладает низкой рассеивающей срюсоб-иостью. Применение перемешиза-иин и подогрева в электролите II 11038.1 увеличить плотность то- [c.945]
К недостаткам цианидных электролитов относятся токсичность и неустойчивость состава вследствие взаимодействия цианида натрия (калия) с СО2 воздуха и выделения циановодо-рода необходимость частой корректировки электролита по цианиду натрия (калия) меньшая допустимая катодная плотность тока н более низкий выход по току, чем в кислом электролите склонност ) анодов к пассивации. В цианидных электролитах необходим избыток свободного цианида натрия (калия) для обеспечения устойчивости комплексного соединения, улучшения структуры осадков, увеличения рассеивающей способности электролита и устранения пассивации анодов. Однако большой избыток цианида допускать не следует, так как резко снижается катодный выход но току меди. В качестве активатора анодов в электролит вводят согнетову соль и роданиды. [c.33]
В цианидных электролитах необходим избыток свободного цианида натрия (калия) для обеспечения устойчивости комплексного соединения, улучшения структуры осадков, увеличения рассеивающей способности электролита и устранения пассивации анодов. Однако большой избыток цианида допускать не следует, так как резко снижается катодный выход но току меди. В качестве активатора анодов в электролит вводят согнетову соль и роданиды. [c.33]
Эфирногидридный электролит — основной неводный электролит алюминирования промышленного масштаба. Исходный вариант его был предложен и разработан А. Бреннером [702, 282, 764, 767] под названием ИБС (национальное бюро стандартов США). Состав эфирногидридного электролита следующий хлорид алюминия (1—4М), гидрид лития (0,5—1,0 М) или смешанный литиевоалюминиевый гидрид (0,1 —0,4 М), абсолютированный диэтиловый эфир. Ванну на основе электролита НБС обычно герметизируют сухим азотом или аргоном, рабочая температура — комнатная. Электроосаждение проведено на самые различные подложки от активных металлов (уран) до инертных конструкционных материалов (стали, латуни, медь, серебро), аноды — алюминиевые. В интервале плотностей тока до 0,1—0,15 А/см с 90—100 %-ным выходом катодно осаждается мелкокристаллический плотный эластичный осадок алюминия, при этом могут быть получены гальвано-пластические слои до 2—5 мм. Осадок алюминия содержит лишь следы тяжелых металлов. Процесс электроосаждення включает приемы, обеспечивающие выравнивание поверхности покрытия проточный, равномерно омывающий рабочий электрод электролит медленное вращение катода непрерывное фильтрование электролита и др. При тщательной герметизации, строгом соблюдении условий электролиза и корректировки ванна может работать непрерывно в течение 18 месяцев. Основным недостатком ванны на основе НБС является высокая летучесть и легкая воспламеняемость. [c.149]
В интервале плотностей тока до 0,1—0,15 А/см с 90—100 %-ным выходом катодно осаждается мелкокристаллический плотный эластичный осадок алюминия, при этом могут быть получены гальвано-пластические слои до 2—5 мм. Осадок алюминия содержит лишь следы тяжелых металлов. Процесс электроосаждення включает приемы, обеспечивающие выравнивание поверхности покрытия проточный, равномерно омывающий рабочий электрод электролит медленное вращение катода непрерывное фильтрование электролита и др. При тщательной герметизации, строгом соблюдении условий электролиза и корректировки ванна может работать непрерывно в течение 18 месяцев. Основным недостатком ванны на основе НБС является высокая летучесть и легкая воспламеняемость. [c.149]
Химически чистый КС1 обезвоживают в муфельной печи при температуре 350—400° С. Состав расплава 30—70 /о КС1, 10—30% K2Zrp6, 20—40% KF. Температура электролиза 750 — 800° С, катодная плотность тока 0,3—0,5 а/см , выход по току 50—60%. Продолжительность наращивания катодной груши 2—2,5 ч. В процессе электролиза для корректировки состава электролита в ванну вносят 20 г K2ZrFe и 25 г КС1 на каждые 10 а-ч, пропущенные через электролит. В открытых электролизерах чистота металла не превышает 0,3—0,4% по кислороду и 0,01 % по азоту, а в герметичных электролизерах с защитной атмосферой содержание кислорода 0,06 /о, азота 0,003%. Катодный осадок содержит 307о металла и электролит. [c.301]
В процессе электролиза для корректировки состава электролита в ванну вносят 20 г K2ZrFe и 25 г КС1 на каждые 10 а-ч, пропущенные через электролит. В открытых электролизерах чистота металла не превышает 0,3—0,4% по кислороду и 0,01 % по азоту, а в герметичных электролизерах с защитной атмосферой содержание кислорода 0,06 /о, азота 0,003%. Катодный осадок содержит 307о металла и электролит. [c.301]
Впервые о возможности получения сплавов d—Ti я Zn—Ti из цианистых электролитов было сообщено в [77]. В [78] описан технологический процесс электроосаждения сплава d—Ti на детали самолетов из высокопрочных сталей 4340, применяемый на заводах фирмы Боинг . Растворимую соль титана получали следующим образом. Фирменная титановая паста, содержащая 15% титана, наносилась на фильтровальную ткань. Затем паста растворялась с помощью перекиси водорода и через фильтровальную ткань переводилась в цианистую ванну кадмирования ( d 21—26 г/л, Na N 97—128 г/л, NaOH 15—19 г/л, Nas Os 37,5 г/л). Из-за нестабильности перекисных титановых соединений содержание титана в ванне должно постоянно корректироваться. Корректировка производилась при непрерывном растворении и фильтрации титана через фильтровальную ткань также с помощью перекиси водорода. Содержание титана в электролите составляло 0,24—0,41 г/л. На изделие вначале наносится тонкая пленка сплава в течение 15 сек. при повышенной плотности тока 4,3—4,8 а/дм . Затем электролиз ведут при обычной плотности тока 1,6—3,2 а/дм . Содержание титана в осадке составляет обычно 0,1—0,5%. Указывается, что после осаждения такого покрытия толщиной 12,5 мк для восстановления механических свойств изделий требовалось всего 2 часа прогрева при температуре 190° по сравнению с обычными 24 часами. Для надежности на производстве прогрев производили в течение 12 час. По мнению авторов, снижение наводороживания стали при электроосаждении сплава d—Ti объясняется, во-первых, тем, что титан сам поглощает значительные количества водорода, и, во-вторых, частич- [c.
Из-за нестабильности перекисных титановых соединений содержание титана в ванне должно постоянно корректироваться. Корректировка производилась при непрерывном растворении и фильтрации титана через фильтровальную ткань также с помощью перекиси водорода. Содержание титана в электролите составляло 0,24—0,41 г/л. На изделие вначале наносится тонкая пленка сплава в течение 15 сек. при повышенной плотности тока 4,3—4,8 а/дм . Затем электролиз ведут при обычной плотности тока 1,6—3,2 а/дм . Содержание титана в осадке составляет обычно 0,1—0,5%. Указывается, что после осаждения такого покрытия толщиной 12,5 мк для восстановления механических свойств изделий требовалось всего 2 часа прогрева при температуре 190° по сравнению с обычными 24 часами. Для надежности на производстве прогрев производили в течение 12 час. По мнению авторов, снижение наводороживания стали при электроосаждении сплава d—Ti объясняется, во-первых, тем, что титан сам поглощает значительные количества водорода, и, во-вторых, частич- [c. 204]
204]
К электролитам предъявляются требования высокая рассеивающая способность, возможность работать с большими плотностями тока и получение металла с высокими механическими свойствами (например, для использования в качестве матриц при прессовании). Для осаждения меди применяют, например, интенсивно работающий электролит, состоящий из 240—260 г uS04 5h30, 60—70 г h3SO1 и 0,2, г сульфированного антрацена в 1 л при плотностях тока 4—10 а/дм , температуре 37—39° и при перемешивании сжатым воздухом, направленным на катод. Аноды — из электролитной меди, однако для корректировки электролита вводят, кроме того, нерастворимые свинцовые аноды и изменяют их площадь по мере надобности. Часто применяют вращающиеся катоды. [c.384]
В электролите химического никелирования, содержащего первоначально сульфат никеля (СН) N 504 х х7НаО 20 г/л (Сен) и гипофосфит натрия (ГФ) НаНаРОаХ хНаО—10 г/л (Сгф), никелируются детали на толщину покрытия 6 = 12 мкм при плотности загрузки деталей 5 = 1,5 дм л. Покрытие содержит / Ы1 —92 вес.% никеля и рр = 9% фосфора и имеет плотность = 7,9 г/см . Коэффициент использования гипофосфита при химических превращениях составляет К г 1 = 42%. После каждого цикла покрытия раствор корректируется химикатами до начального содержания. Такую корректировку проводят до тех пор, пока концентрация фосфита НаНзРОз не достигнет максимально допустимой величины Сф = 60 г/л. Механические потери раствора при уносе с деталями, в вентиляцию и при корректировке составляют р = = 0,20 л на 1 м никелируемых деталей. Какое количество циклов никелирования можно провести в таком электролите Каковы общие коэффициенты использования сульфата никеля и гипофосфита натрия (см. задачу 234) [c.186]
Покрытие содержит / Ы1 —92 вес.% никеля и рр = 9% фосфора и имеет плотность = 7,9 г/см . Коэффициент использования гипофосфита при химических превращениях составляет К г 1 = 42%. После каждого цикла покрытия раствор корректируется химикатами до начального содержания. Такую корректировку проводят до тех пор, пока концентрация фосфита НаНзРОз не достигнет максимально допустимой величины Сф = 60 г/л. Механические потери раствора при уносе с деталями, в вентиляцию и при корректировке составляют р = = 0,20 л на 1 м никелируемых деталей. Какое количество циклов никелирования можно провести в таком электролите Каковы общие коэффициенты использования сульфата никеля и гипофосфита натрия (см. задачу 234) [c.186]
Корректировку электролита по электропроводности производят хромовым ангидридом, концентрацию которого допускается доводить до 250 г л. При введении в электролит борной кислоты оксидная пленка приобретает красивый серо-голубой цвет и приобретает сходство с эмалированной поверхностью, вследствие чего процесс получил наименование эмати ирования. Для этой цели применяется электролит, содержащий 28—32 г/л хромового ангидрида и 1—2 г/л борной кислоты. Рабочая температура 45 3° С, плотность тока Da = 1 а дм , выдержка 50—60 мин. [c.179]
Для этой цели применяется электролит, содержащий 28—32 г/л хромового ангидрида и 1—2 г/л борной кислоты. Рабочая температура 45 3° С, плотность тока Da = 1 а дм , выдержка 50—60 мин. [c.179]
Сурьмяновиннокислый калий готовят путем растворения окиси сурьмы ЗЬаОз в винной кислоте с последующей нейтрализацией едким кали. Корректировку pH производят соляной кислотой. Электролит требует предварительной проработки в течение 10—20 ч при плотности тока 0,25 а дм . Отношение площади анодов к покрываемой поверхности следует поддерживать равным 4 1. Толщину слоя сурьмы можно доводить до 200 мкм и более. [c.108]
Нерастворимые аноды применяются из платины или графита. Корректировка электролита заключается в основном во введении добавок АзгОд для компенсации металла, израсходованного на осаждение. Электролит отличается высокой рассеивающей способностью. Слой мышьяка осаждается блестящий, темно-серого цвета и с хорошей адгезией не только, к металлам, но и к полупроводникам, например к германию. Толщину покрытия можно доводить до 20 мкм. Хорошие результаты дает также осаждение мышьяка из раствора метаарсенита калия в глицерине при температуре / = 210° С и плотности тока Ок = 8 а дм . [c.111]
Толщину покрытия можно доводить до 20 мкм. Хорошие результаты дает также осаждение мышьяка из раствора метаарсенита калия в глицерине при температуре / = 210° С и плотности тока Ок = 8 а дм . [c.111]
Электролит корректировка плотности электролита — Энциклопедия по машиностроению XXL
Незначительную сульфатацию можно устранить следующим образом батарею разряжают током 10-часового режима (ом. табл. 2) до напряжения 1,7 В на банке сливают из батареи электролит и заливают дистиллированную воду производят зарядку током /з = = (0,030,05) Сном, А, до тех пор, пока плотность электролита и напряжение на батарее не будут оставаться постоянными в течение 2—5 ч. Если в конце заряда напряжение на батарее соответствует номинальному, то после корректировки плотности электролита батарею можно направить в эксплуатацию, в противном случае она требует ремонта. [c.37]В конце заряда плотность электролита, измеренная с учетом температурной поправки, приведенной выше, должна соответствовать норме (см.
 табл. 4). В противном случае необходимо провести корректировку плотности электролита. Дистиллированную воду доливают, если плотность электролита выше нормы, а раствор кислоты плотностью 1,400 г/см — если она ниже нормы. После корректировки заряд батареи продолжают в течение 30 мин для полного перемешивания электролита. Через 30 мин после отключения батареи от зарядного устройства измеряют уровень электролита во всех аккумуляторах. Если окажется, что уровень электролита ниже нормы, то в аккумулятор надо добавить электролит (плотность см. по табл. 4). Если уровень электролита выше нормы, то избыток электролита следует отобрать резиновой грушей. После проведения перечисленных работ батарею можно эксплуатировать.
[c.72]
табл. 4). В противном случае необходимо провести корректировку плотности электролита. Дистиллированную воду доливают, если плотность электролита выше нормы, а раствор кислоты плотностью 1,400 г/см — если она ниже нормы. После корректировки заряд батареи продолжают в течение 30 мин для полного перемешивания электролита. Через 30 мин после отключения батареи от зарядного устройства измеряют уровень электролита во всех аккумуляторах. Если окажется, что уровень электролита ниже нормы, то в аккумулятор надо добавить электролит (плотность см. по табл. 4). Если уровень электролита выше нормы, то избыток электролита следует отобрать резиновой грушей. После проведения перечисленных работ батарею можно эксплуатировать.
[c.72]В аккумулятор систематически доливалась вода без корректировки плотности электролита Полностью или частично заменить электролит [c.58]
Получение и промывку хлористого серебра следует производить в затемненном помешении, так как оно светочувствительно. При серебрении поверхность серебряных анодов обычно меньше катодной, в результате чего электролит обедняется серебром. Содержание цианидов в электролите уменьшается вследствие их разложения. Таким образом, корректировка электролита заключается в систематическом добавлении солей серебра и цианистого калия. Корректируют электролит по данным анализов, которые следует производить не реже одного раза в неделю. При приготовлении электролитов для серебрения рекомендуется применять цианистый калий, а не цианистый натрий, так как присутствие солей калия благоприятно влияет на структуру осадка и позволяет несколько повысить плотность тока при нанесении покрытия.
[c.122]
При серебрении поверхность серебряных анодов обычно меньше катодной, в результате чего электролит обедняется серебром. Содержание цианидов в электролите уменьшается вследствие их разложения. Таким образом, корректировка электролита заключается в систематическом добавлении солей серебра и цианистого калия. Корректируют электролит по данным анализов, которые следует производить не реже одного раза в неделю. При приготовлении электролитов для серебрения рекомендуется применять цианистый калий, а не цианистый натрий, так как присутствие солей калия благоприятно влияет на структуру осадка и позволяет несколько повысить плотность тока при нанесении покрытия.
[c.122]
Добавлять золото в электролит не требуется, если поверхность анодов достаточно велика и если не происходит их пассивирование из-за большой анодной плотности тока, а также если не применяется цианистый натрий вместо цианистого калия. В этом случае при корректировке добавляют лишь цианистый калий. [c.128]
В обслуживаемых аккумуляторах производится чистка вентиляционных отверстий в пробках или крышке, а также проверка уровня электролита в банках. Восстанавливают его, доливая дистиллированную воду. Чтобы повысить энерго-отдачу АКБ при низких отрицательных температурах, рекомендуется увеличить плотность электролита на 0,01 -0,02 г/ см но не более, чем до 1,28 г/см (для нашей климатической зоны). В противном случае активизируется процесс сульфатации пластин, а это ускоряет выход АКБ из строя. Плотность электролита определяют с помощью ареометра. Подержанный или глубоко разряженный аккумулятор можно подвергнуть контрольно-тренировочному циклу (КТЦ). Эта операция в большинстве случаев позволяет восстановить работоспособность батареи, а также определить ее пригодность к дальнейшей эксплуатации. Подобная процедура показана для всех аккумуляторов, за исключением еще не бывших в эксплуатации. Если провести КТЦ нет возможности, перед зимней эксплуатацией АКБ, снятый с автомобиля, рекомендуется полностью зарядить от внешнего зарядного устройства, после чего произвести корректировку (выравнивание) плотности электролита во всех банках. Если плотность выше нормы, в аккумулятор доливают дистиллированную воду, если ниже — электролит плотностью 1,4 г/см [c.146]
Электролит может работать без корректировки в течение 8— 10 а-час/ л, что составляет в переводе на производственную ванну емкостью 900 л при объемной плотности тока 0,1—0,15 а л 70— 80 час. непрерывной работы. [c.16]
Для замены электролита батарею разряжают током 10-часового разряда (см. табл. 2) до напряжения на банке 12 В (7,2 В на 12-вольтовой батарее), определяют плотность электролита в банках, промывают банки батареи дистиллированной водой и заливают в них свежнй электролит такой же плотности, что и слитый из батареи. Затем батарею заряжают в соответствии с данными табл. 2 и производят корректировку плотности электролита. [c.37]
Разбавленный электролит проверяется на плотность ареометром. В случае необходимости производится корректировка содержания хлористого железа. Если содержание железа выше заданного, в электролит добавляют воду, а если содержание железа недостаточно, — дополнительно травят стружку или прорабаты- [c.24]
Контроль и корректировка содержания железа в электролите. При промышленной эксплуатации простых хлористых электролитов содержание в них хлористого железа вполне допустимо контролировать при помощи обыкновенного ареометра. Изменение плотности электролита на 0,01 соответствует изменению в нем концентрации Fe l2-4h30 на 17—18 г/л. Ареометр и таблица плотности электролитов с совершенно достаточной точ- [c.25]
Стандартный электролит хромирования имеет некоторые недостатки. Он очень чувствителен к колебанию температуры, допуская незначительное отклонение ( 2°С) от рабочего режима процесса.. Необходимо также поддерживать постоянную плотность тока в следить за соотношением между концентрациями хромового ангид—рида и серной кислоты, что связано с частой корректировкой электролита. [c.61]
Корректировку электролита по электропроводности производят хромовым ангидридом, концентрацию которого допускается доводить до 250 г л. При введении в электролит борной кислоты оксидная пленка приобретает красивый серо-голубой цвет и приобретает сходство с эмалированной поверхностью, вследствие чего процесс получил наименование эмати ирования. Для этой цели применяется электролит, содержащий 28—32 г/л хромового ангидрида и 1—2 г/л борной кислоты. Рабочая температура 45 3° С, плотность тока Da = 1 а дм , выдержка 50—60 мин. [c.179]
При соблюдении приведенных выше соотношений щелочи и воды плотность получится либо не требующей никакой корректировки, либо требующей добавления небольшого кюличества воды. Затем электролиту дают отстояться до полного осветления от 6 до 12 часов и сливают осветленную часть в бутылки с плотно закрывающейся пробкой. Остывший и отстоявшийся электролит пригоден для заливки аккумуляторов. [c.91]
Хромирование в саморегулирующемся электролите. При введении в электролит вместо серной кислоты трудно растворимых солей сернокислого стронция 8г504 и кремнефтористого калия К231Рв в количестве, превышающем их растворимость, электролит становится устойчивым и саморегулирующимся, так как автоматически поддерживается постоянство концентрации ионов 504 и При избытке в электролите указанных солей, превышающих их растворимость, часть солей будет находиться в растворе в виде диссоциированных ионов, а часть — на дне ванны в виде твердой фазы. При изменении концентрации хромового ангидрида концентрация ионов 804 и 51Рв будет автоматически поддерживаться постоянной за счет частичного растворения солей. Таким образом, необходимость в частых корректировках электролита отпадает. Применяется следующий состав электролита (г/л) хромовый ангидрид 200—300 сульфат стронция 5,5—6,5 кремнефторид калия 18—20. Плотность тока = 50 100 А/дм = 50 -е- 70° С выход по току 17—18%. [c.277]
Какую кислоту заливают в аккумулятор
Большинство водителей никогда в жизни не задумывались, какую кислоту добавляют в аккумулятор авто и зачастую высказывают неправильные догадки. Одни скажут, что там вода, другие назовут соляную кислоту, поэтому мы расставим все точки над «и». В аккумуляторах применяется смесь серной кислоты и дист. воды. Знакомьтесь, это электролит.
На практике встречаются устройства, где в роли электролита выступает щелочь (никель-кадмиевые аккумуляторы). Также есть несколько гелевых устройств, но по факту гель – это та же самая кислота, находящаяся в другом состоянии или пропитывающий стекловолоконные частицы.
Она применяется в промышленном изготовлении АКБ для авто. Обычно, электролит — это 35% серной кислоты и 65% дист. воды. Заливать любую другую воду категорически запрещается, поскольку она содержит соли, которые существенно сократят срок работы АКБ.
Концентрированная серная кислота производится в 2 стадии. В первой её концентрацию доводят до 65-70%, а во второй – до 98%. Это необходимо для того, чтобы увеличить срок хранения кислоты. Вероятно даже повышение концентрации до 99%, но из-за потерь SO3 значение все равно будет снижено до 98 процентов.
Как сделать электролит в домашних условиях?
Рекомендуем купить его в магазине, но его можно сделать и своими руками.
Нам потребуются:
- Дистиллированная вода;
- Серная кислота;
- Емкость из стекла, керамики или свинца, устойчивая к кислотам;
- Эбонитовая палочка.
Чтобы сделать электролит надо залить воду в специальную емкость и добавить туда серную кислоту в пропорции 3:1. Тщательно перемешать смесь эбонитовой палочкой. Вещество плотно накрыть и оставить на 1 день до выпадения осадка.
Таблица для расчета приготовляемого электролитаНеобходимо сказать, что превышения в допустимой концентрации электролита может привести к самым неприятным последствиям. От чрезмерно концентрированного вещества пластины аккумулятора очень быстро «разъест», что в кратчайшие сроки вызовет выход аккумулятора из рабочего состояния.
В дист вода добавляем кислоту, а не наоборотА вот слишком низкий уровень плотности вещества может очень быстро вызывать сульфатацию. Наверняка вы знаете, что это такое. Нет? Это процесс оседания кристаллических осадков на пластинах, в результате чего аккумулятор теряет свои свойства и просто оказывается неспособным держать заряд долгое время.
Зачем нужен электролит?
Суть работы АКБ базируется на реакциях, проходящих только при помощи этого вещества. Батарея состоит из плюсовых и минусовых пластинок, погружаемых в кислотный раствор. Эти пластины оснащены токоотводными решетками, сделанными из свинца.
Как проконтролировать состояние электролита?
Держать под контролем состояние электролита нужно. Для контроля сгодится пластмассовый корпус от обычной пластиковой ручки. Открываем пробки и погружаем его к пластинам, после чего зажимаем сверху и вынуть. Идеальный уровень – 10-12 мм. Если надо, дольем электролит.
Измерение уровня электролита в АКБОчень важно следить за временем года и параметрами раствора в соответствии с ним. Можно существенно продлить жизнь батареи, если использовать растворы с разными параметрами в разное время. К примеру, слишком концентрированное вещество в летнее время деструктивно воздействует на АКБ. Высокая плотность увеличивает энергопотери, а серный ангидрид может полностью разрушить электроды устройства.
Срок эксплуатации электролита
У такого электролита нет срока эксплуатации. Данный критерий может быть определен только по способности выполнения своих функций на 100%. Среди факторов, которые могут повлиять на жизненный цикл электролита, важнейшими являются:
- Плотность;
- Температуру работы аккумулятора;
- Заряд.
Если все показатели в норме, то и электролит не будет тревожить Вас годами.
Как увеличить плотность вещества?
Увеличить плотность можно при повышении температуры и гидролиза. Также важно постоянно добавлять дистиллят для поддержания показателей на нормальном уровне. Если же концентрация кислоты ниже 1,275 грамм на сантиметр кубический, её нужно поднять.
Корректировка плотности электролита в АКБПовысить такой уровень можно 2-мя способами: сменой содержимого или доливом концентрированной кислоты.
Если разбавлять жидкость, то необходимо совершить определенные действия для всех банок:
- Откачать максимум электролита при помощи шприца;
- Внести в банку половину от его объема;
- Подать нагрузку с низкой мощностью для смешивания жидкости.
- Если изменений в уровне нет, добавляем во вторую половину электролит и получаем идеальную плотность.
Кислота – вредная субстанция для кожи. Использование резиновых перчаток, фартука и защитных очков при работе с этим веществом категорически обязательно!
Как заливать и доливать кислоту?
Электролит заливается при помощи трубки до 15 мм над пластинками батареи. Затем оставляем аккумулятор на 2 часа для остывания и заряжаем током в 10 раз меньшим от объема АКБ.
Ключевые характеристики надо проверять пару раз в году с помощью особого прибора и не пропускать проверки.
При смешивании дистводы с кислотой, важно добавлять именно кислоту в воду, так как в обратном случае есть вероятность активации бурной реакции вещества с тепловыделением, доведением её до состояния кипения.
Внимательно соблюдайте все вышеперечисленные рекомендации и АКБ будет служить очень долгое время!
Сдать старый АКБ за деньги вы сможете в нашей фирме, тарифы на приём акумуляторов на этой странице.
Как корректировать плотность электролита в аккумуляторе
В продолжение предыдущей записи про доливку дистиллированной водички в аккум, после двух лет эксплуатации без обслуживания.
После доливки до MAX дистиллированной водички в каждую банку (влезло 0,5 л на все 6 банок) и зарядки автоматическим зарядным устройством, током от 2 А до 0,5 А в течении 20 часов, по истечении суток эксплуатации замерил плотность электролита в банках.
Оказалось, что в средних четырех банках плотность одинаковая — 1,27, а в двух крайних банках (слева и справа) она чувствительно меньше — 1,23; 1,24.
Погуглив, почитав различные статьи по предмету выяснил, что как бы это не конец, но позаботиться о продлении жизни аккуму неплохо бы 🙂
Если зарядка не помогла выровнять плотность электролита, необходимо выровнять при помощи концентрированного электролита плотностью 1,4.
Ринулся по магазинам торгующими аккумуляторами и автомагазинам по пути следования.
К моему удивлению, концентрированного электролита нигде не было в наличии.
В одном из магзиков консультант поделился, что плотность 1,4 запрещена и не выпускается уже давненько, а стандартный корректирующий электролит плотностью 1,33, не привозили уже месяца три, в связи с какими-то предстоящими изменениями в законодательстве и скорее всего корректирующий будет еще меньшей плотности.
Правда или нет, но за что купил, за то и продаю 🙂
Доехал до авторынка, где есть множество мелких магазинчиков-палаток и в одном из них без проблем нашлась литрушка корректирующего электролита 1,33, всего за 70 руб 🙂
Итак, чего и сколько отливать/доливать…
Статьи в инете в основном старинные, т.к. аккумулятор давно уже перешел в разряд расходников и обслуживать его стремятся немногие.
За основу для расчетов взята статья с сайта — Автоэлектроника: Простенько и со вкусом
Суть корректировки плотности электролита в банке аккумулятора заключается в следующем:
а) из банки забирается некоторый объём электролита;
б) вместо него в банку добавляется тот-же объём либо дистиллированной воды (плотность 1,00) — для понижения плотности электролита в банке, либо корректирующего электролита (обычно плотностью 1,40) — для повышения плотности;
Равенство объёмов забираемой и добавляемой жидкостей используется только для упрощения всей процедуры и более простого логического осмысления её результатов.
По мере приобретения опыта, указанное равенство может нарушаться.
в) батарея включается на 30 минут на заряд номинальным током для лучшего перемешивания электролита в результате газовыделения;
г) батарея отключается от зарядного устройства и выдерживается 0,5÷2 часа для выравнивания плотности электролита в объёме банок;
д) измеряется плотность электролита в каждой банке и его уровень, оба параметра приводятся в норму.
Т.е. при необходимости, все операции а) и д) повторяются
Ниже приведена формула, при использовании которой можно применять корректирующий электролит с плотностью отличной от 1,40
где:
Vэ — объём удаляемого из банки электролита, см3,
Vб — объём электролита в одной банке, см3,
ρн — начальная плотность электролита до корректировки, г/см3,
ρк — конечная плотность, которую надо получить, г/см3,
ρд — плотность доливаемой жидкости, (вода — 1,00 г/см3 или корректирующий электролит — * г/см3)
Следует учесть, что при использовании данной формулы объёмы удаляемого и добавляемого электролитов равны.
Итак, теперь главный вопрос, какой объем электролита в нашем ISTA CALCIUM 12V 70A/h?
На него ответа так и не нашел, но решено по аналогии с размерами наших русских аккумов, взять за исходник объем в 6СТ-55 (60) — 3,8 л. По итогу вышло, что вероятно в нашем аккуме примерно 3,5 л.
По расчетам при плотности начальной 1,24, необходимо заместить на корректирующий электролит 1,33, примерно 211 см3.
Чтобы сильно не ошибиться, для начала из каждой крайней банки изъято четыре раза по 40 единиц объема указанного на колбе ареометра, итого 160 из каждой 🙂
Соответственно столько же и залито электролита 1,33
После перемешивания, перебулькивания 🙂 плотность как раз оказалась 1,27
Оставляю заряжаться на 10 ч током от 2 до 0,5 А (автоматическое зарядное) и утром плотность оказывается практически 1,32 в каждой банке.
Многовато, но это только сразу после отключения зарядки.
Через пару дней проверяю, в каждой банке ровно 1,30, во всех шести.
Повторяю процедуру с замещением небольших объемов в кажой банке на дистиллированную воду.
В этот раз из каждой банки забрал по 60 см3, взамен заливаю дистиллировку.
Полчаса подзарядил, покатался денек и на проверку.
Ну вот теперь около дела, во всех банках плотность электролита одинакова — 1,26
для стремительно надвигающегося лета в самый раз 🙂
Если все эти манипуляции помогут продлить жизнь аккуму еще года на три, то в принципе не напрягает.
Да и когда знаешь, что мерять и доливать, то совсем все просто.
Следующая проверка состояния в октябре/ноябре 🙂
PS: прошло более полутора лет с момента данной операции с корректирующим электролитом и уже после этого читал много мнений, что нельзя так корректировать плотность, правильный вариант только полной зарядкой аккума стационарным зарядником, что в итоге после полной зарядки получится перекос по плотности в банках… НО, буквально на днях заморочился полной зарядкой аккума в несколько этапов и в итоге в этих крайних банках плотность по окончанию заряда как и в остальных — 1,27 все норм.
В этот раз подвела только одна банка в середине, во всех 1,27, а в одной 1,25 после полной зарядки.
КТЦ для аккума проведены, полный заряд произведен, думаю терять нечего, с одной средней банкой повторю экзекуцию с корректирующим электролитом
Владельцы автомобилей часто сталкиваются с проблемой отказа двигателя от запуска. Подобное случается из-за разрядки аккумулятора и ухудшения свойств электролита. Перед тем как поднять плотность в аккумуляторе, нужно выяснить причину ухудшения качества кислотного раствора. После этого можно приступать к восстановлению батареи. Действия не представляют особых сложностей.
Почему снижается плотность электролита
Снижению плотности способствуют такие факторы:
- Разряд. При потере заряда снижается и плотность наполнителя. Во процессе зарядки этот параметр постепенно увеличивается. Если батарея утрачивает большую часть емкости, речь идет о падении концентрации кислоты.
- Длительная эксплуатация или хранение в условиях низких температур.
- Выкипание электролита при перезаряде. Если зарядное устройство подает слишком высокое напряжение, жидкий электролит переходит в газообразное состояние и выводится наружу через имеющиеся на корпусе отверстия.
- Частое добавление воды. Водители добавляют жидкость для поддержания стабильного уровня электролита. Не все пользуются ареометром, измеряющим плотность. Вместе с водой выкипает и кислота, что приводит к снижению концентрации.
Опасности низкой и высокой концентрации кислоты
Повышенная концентрация электролита становится причиной преждевременного выхода батареи из строя. Кислота разрушает металлические пластины. К воздействию составов на основе серной кислоты чувствительна даже сталь.
Низкая концентрация приводит к таким проблемам:
- Сульфатация. На пластинах появляется налет, состоящий из сульфата свинца. Аккумуляторная батарея становится неспособной принимать заряд.
- Повышение порога замерзания. Жидкость кристаллизуется уже при -5°С. Лед сдвигает и повреждает металлические детали. При деформации пластин и коротком замыкании емкостей батарею восстановить невозможно. При плотности 1,28 г/см³ электролит замерзнет только при -58°С.
- Проблемы при запуске двигателя. Наиболее выражен этот признак в зимний период.
Проверка плотности электролита
Определить плотность электролита можно в домашних условиях. Процедуру рекомендуется проводить при комнатной температуре.
Перед началом работы подготавливают такие инструменты:
- Защитные перчатки, костюм и очки. В состав наполнителя аккумулятора входит кислота. При попадании на кожу вещество вызывает химический ожог. Опасными являются и пары кислоты, поэтому работают только в хорошо проветриваемом помещении.
- Денсиметр. Прибор используется для измерения плотности. Имеет вид стеклянной трубки с грушей и встроенным ареометром.
Самостоятельно измерение плотности выполняют так:
- Аккумулятор вынимают из посадочного гнезда. Защитный кожух демонтируют, вывинчивают пробки.
- Проверяют уровень электролита. В свинцово-кальциевых батареях раствор должен на 1,5 см закрывать пластины.
- Батарею полностью заряжают. Проверку плотности начинают через 5-6 часов после завершения зарядки. При нормальном уровне электролита трубку денсиметра погружают в банки, выкачивая небольшое количество жидкого наполнителя.
- Оценивают показатели прибора. Ареометр должен свободно плавать в растворе. Соприкосновение прибора со стенками емкости не допускается. Показания оценивают с учетом температуры окружающей среды.
- Проверяют плотность электролита в остальных банках. Показания записывают и сравнивают с нормальной плотностью.
Такой способ проверки подходит только для разборной батареи, когда имеется доступ к электролиту. Необслуживаемый аккумулятор снабжен индикатором, цвет которого меняется в зависимости от плотности наполнителя.
Как откорректировать плотность раствора
Нормальное показание лежит в диапазоне 1,25-1,29 г/см³. Если при температуре +25°С отмечается более низкое значение, его нужно повышать. Падение концентрации в одной из банок свидетельствует о коротком замыкании.
Высокие значения выявляются после зарядки мощным током, сопровождающейся кипением электролита. Повысить плотность можно путем добавления кислоты, заправки готового состава или использования зарядного устройства.
Плотность раствора в холодный период
В холодное время года плотность наполнителя заряженного аккумулятора должна составлять 1,27 г/см³. Дополнительная корректировка в регионах с суровым климатом при смене сезона не проводится.
Подготовка к восстановлению батареи
На этапе подготовки выполняют такие действия:
- Зарядка батареи. Нельзя начинать восстановление при низком заряде. Добавление электролита способствует резкому повышению концентрации кислоты. Это приводит к разрушению металлических пластин, при котором батарею утилизируют.
- Нормализация температуры электролита. Показатель лежит в пределах +20…+25°С. Уровень электролита в каждой банке должен быть нормальным.
- Осмотр батареи. Корпус не должен иметь трещин и сколов, особенно возле выводов. Повреждению способствует раскачивание при попытке снять прикипевшую клемму.
Повышение плотности электролита
Если плотность составляет более 1,18, доливают готовый состав с нормальной концентрацией серной кислоты.
Процедура включает такие этапы:
- Разрядка батареи. Долив электролита проводится только при полном разряде. Для этого АКБ подключают к мощной лампе или другому потребителю энергии.
- Подготовка корректирующего компонента. Уровень кислоты в таком средстве должен составлять не менее 1,4 г/см³.
- Добавление корректирующего состава. Предварительно откачивают часть имеющегося электролита. Густота раствора должна повыситься до 1,25. Действие выполняется для каждой банки. Объем доливаемой жидкости должен составлять не более 50% от откачанного. После добавления жидкости АКБ встряхивают, давая наполнителю перемешаться.
- Зарядка батареи. Аккумулятор оставляют на полчаса, что позволяет концентрации в банках выровняться. Элемент питания подключают к зарядному устройству на 30 минут. Сила тока должна быть минимальной. Через 2 часа после прекращения зарядки замеряют плотность и количество наполнителя. Если концентрация не поднимается, вышеуказанные действия повторяют.
Можно ли повысить минимальную плотность
Когда плотность падает до отметки ниже 1,18, добавление кислоты оказывается неэффективным. Для восстановления батареи используют раствор, содержащий большее, чем электролит, количество действующего вещества.
Для замены наполнителя выполняют такие действия:
- Слив содержимого. Максимальное количество жидкости выкачивают грушей. Затем аккумулятор помещают в большую емкость и переворачивают на бок. В дне каждой банке формируют небольшое отверстие. Батарею возвращают в прежнее положение и дожидаются вытекания жидкого наполнителя.
- Добавление воды. Жидкость заливается через крышки банок для удаления остатков старого наполнителя. Сделанные ранее отверстия закрываются полимерным материалом, устойчивым к воздействию кислот.
- Заправка батареи новым раствором. Если все действия выполнены правильно, АКБ становится готовой к использованию. Недостатком метода является снижение срока эксплуатации аккумулятора. Несколько недель устройство проработает, однако потом придется покупать новое.
Как повысить при помощи зарядного устройства
Если концентрация кислоты упала за зиму, ее можно восстановить путем подачи слабого тока. Зарядка занимает не менее 3 суток, она считается эффективной при невозможности восстановления АКБ другими методами. Содержимое набравшей полную мощность батареи при зарядке начинает кипеть. Признаком испарения воды является образование мелких пузырьков на поверхности.
Избыток жидкости испарится, концентрация кислоты увеличится. Общий уровень наполнителя станет маленьким, поэтому придется добавлять готовый аккумуляторный раствор. После завершения процедуры пользуются ареометром. Если показатели прибора слишком низкие, зарядку и добавление электролита повторяют.
Плотность электролита в аккумуляторе очень важный параметр у всех кислотных АКБ, и каждый автовладелец должен знать: какая плотность должна быть, как её проверить, а самое главное, как правильно поднять плотность аккумулятора (удельный вес кислоты) в каждой из банок со свинцовыми пластинами заполненных раствором h3SO4.
Проверка плотности – это один из пунктов процесса обслуживания аккумуляторной батареи, включающий так же проверку уровня электролита и замер напряжения АКБ. В свинцовых аккумуляторах плотность измеряется в г/см3. Она пропорциональна концентрации раствора, а обратно зависима, относительно температуры жидкости (чем выше температура, тем ниже плотность).
По плотности электролита можно определить состояние батареи. Так что если батарея не держит заряд, то следует проверить состояние её жидкости в каждой его банке.
Плотность электролита влияет на емкость аккумулятора, и срок его службы.
Проверяется денсиметром (ареометр) при температуре +25°С. В случае, если температура отличается от требуемой, в показания вносятся поправки, как показано в таблице.
Итак, немного разобрались, что это такое, и что нужно регулярно делать проверку. А на какие цифры ориентироваться, сколько хорошо, а сколько плохо, какой должна быть плотность электролита аккумулятора?
Какая плотность должна быть в аккумуляторе
Выдерживать оптимальный показатель плотности электролита очень важно для аккумулятора и стоит знать, что необходимые значения зависят от климатической зоны. Поэтому плотность аккумулятора должна быть установлена исходя из совокупности требований и условий эксплуатации. К примеру, при умеренном климате плотность электролита должна находиться на уровне 1,25-1,27 г/см3 ±0,01 г/см3. В холодной зоне, с зимами до -30 градусов на 0,01 г/см3 больше, а в жаркой субтропической — на 0,01 г/см3 меньше. В тех регионах, где зима особо сурова (до -50 °С), дабы аккумулятор не замерз, приходится повышать плотность от 1,27 до 1,29 г/см3.
Много автовладельцев задаются вопросом: «Какой должна быть плотность электролита в аккумуляторе зимой, а какой летом, или же нет разницы, и круглый год показатели нужно держать на одном уровне?» Поэтому, разберемся с вопросом более подробно, а поможет это сделать, таблица плотности электролита в аккумуляторе с разделением на климатические зоны.
Также нужно помнить, что, как правило, аккумуляторная батарея, находясь на автомобиле, заряжена не более чем на 80-90 % её номинальной ёмкости, поэтому плотность электролита будет немного ниже, чем при полном заряде. Так что, требуемое значение, выбирается чуть-чуть повыше, от того, которое указано в таблице плотности, дабы при снижении температуры воздуха до максимального уровня, АКБ гарантированно оставался работоспособным и не замерз в зимний период. Но, касаясь летнего сезона, повышенная плотность может и грозить закипанием.
Таблица плотности электролита в аккумуляторе
Таблица плотности составляется относительно среднемесячной температуры в январе-месяце, так что климатические зоны с холодным воздухом до -30 °C и умеренные с температурой не ниже -15 не требуют понижения или повышения концентрации кислоты. Круглый год (зимой и летом) плотность электролита в аккумуляторе не стоит изменять, а лишь проверять и следить, чтобы она не отклонялась от номинального значения, а вот в очень холодных зонах, где столбик термометра часто на отметке ниже -30 градусов (в плоть до -50), корректировка допускается.
Плотность электролита в аккумуляторе зимой
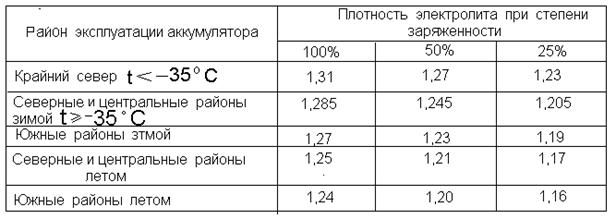
Плотность электролита в аккумуляторе зимой должна составлять 1,27 (для регионов с зимней температурой ниже -35 не менее 1.28 г/см3). Если будет значение ниже, то это приводит к снижению электродвижущей силы и трудного запуска двигателя в морозы, вплоть до замерзания электролита.
Когда в зимнее время плотность в аккумуляторной батареи понижена, то не стоит сразу бежать за корректирующим раствором дабы её поднять, гораздо лучше позаботится о другом – качественном заряде АКБ при помощи зарядного устройства.
Получасовые поездки от дому к работе и обратно не позволяют электролиту прогрется, и, следовательно, хорошо зарядится, ведь аккумулятор принимает заряд лишь после прогрева. Так что разряженность изо дня в день увеличивается, и в результате падает и плотность.
Для новой и исправной АКБ нормальный интервал изменения плотности электролита (полный разряд – полный заряд) составляет 0,15-0,16 г/см3.
Помните, что эксплуатация разряженного аккумулятора при минусовой температуре приводит к замерзанию электролита и разрушению свинцовых пластин!
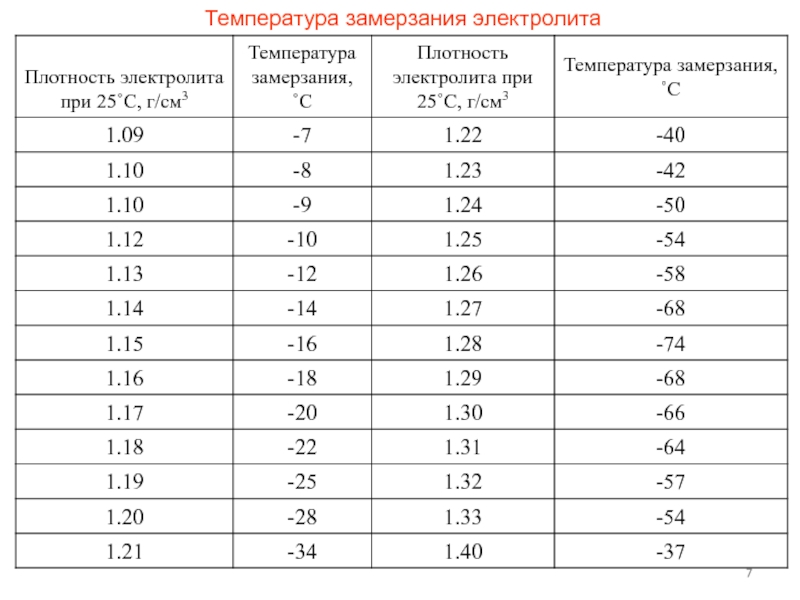
По таблице зависимости температуры замерзания электролита от его плотности, можно узнать минусовой порог столбика термометра, при котором образовывается лед в вашем аккумуляторе.
Как видите, при заряженности на 100% аккумуляторная батарея замерзнет при -70 °С. При 40% заряде замерзает уже при -25 °С. 10% не только не дадут возможности запустить двигатель в морозный день, но и напрочь замерзнет в 10 градусный мороз.
Когда плотность электролита не известна, то степень разряженности батареи проверяют нагрузочной вилкой. Разность напряжения в элементах одной батареи не должна превышать 0,2В.
Показания вольтметра нагрузочной вилки, B
Степень разряженности батареи, %
Если АКБ разрядилась более чем на 50% зимой и более чем на 25% летом, её необходимо подзарядить.
Плотность электролита в аккумуляторе летом
Летом аккумулятор страдает от обезвоживания, поэтому учитывая то, что повышенная плотность плохо влияет на свинцовые пластины, лучше если она будет на 0,02 г/см3 ниже требуемого значения (особенно касается южных регионов).
В летнее время температура под капотом, где зачастую находится аккумулятор, значительно повышена. Такие условия способствуют испарению воды из кислоты и активности протекания электрохимических процессов в АКБ, обеспечивая высокую токоотдачу даже при минимально допустимом значении плотности электролита (1,22 г/см3 для теплой влажной климатической зоны). Так что, когда уровень электролита постепенно падает, то повышается его плотность, что ускоряет процессы коррозионного разрушения электродов. Именно поэтому так важно контролировать уровень жидкости в аккумуляторной батарее и при его понижении добавить дистиллированной воды, а если этого не сделать, то грозит перезаряд и сульфация.
Если аккумулятор разрядился по невнимательности водителя или другим причинам, следует попробовать вернуть ему его рабочее состояние при помощи зарядного устройства. Но перед тем как заряжать АКБ, смотрят на уровень и по надобности доливают дистиллированную воду, которая могла испариться в процессе работы.
Через некоторое время плотность электролита в аккумуляторе, из-за постоянного разбавления его дистиллятом, снижается, и опускается ниже требуемого значения. Тогда эксплуатация батареи становится невозможной, так что возникает необходимость повысить плотность электролита в аккумуляторе. Но для того, чтобы узнать насколько повышать, нужно знать как проверять эту самую плотность.
Как проверить плотность аккумулятора
Дабы обеспечить правильную работу аккумуляторной батареи, плотность электролита следует проверять каждые 15-20 тыс. км пробега. Измерение плотности в аккумуляторе осуществляется при помощи такого прибора как денсиметр. Устройство этого прибора состоит из стеклянной трубки, внутри которой ареометр, а на концах — резиновый наконечник с одной стороны и груша с другой. Чтобы произвести проверку, нужно будет: открыть пробку банки аккумулятора, погрузить его в раствор, и грушей втянуть небольшое количество электролита. Плавающий ареометр со шкалой покажет всю необходимую информацию. Более детально как правильно проверить плотность аккумулятора рассмотрим чуть ниже, поскольку есть еще такой вид АКБ, как необслуживаемые, и в них процедура несколько отличается — вам не понадобится абсолютно никаких приборов.
Индикатор плотности на необслуживаемой АКБ
Плотность необслуживаемого аккумулятора отображается цветовым индикатором в специальном окошке. Зеленый индикатор свидетельствует, что все в норме (степень заряженности в пределах 65 — 100%), если плотность упала и требуется подзарядка, то индикатор будет черный. Когда в окошке отображается белая или красная лампочка, то нужен срочный долив дистиллированной воды. Но, впрочем, точная информация о значении того или иного цвета в окошке, находится на наклейке аккумуляторной батареи.
Теперь продолжаем далее разбираться, как проверять плотность электролита обычного кислотного аккумулятора в домашних условия.
Проверка плотности электролита в аккумуляторе
Итак, чтобы можно было правильно проверить плотность электролита в аккумуляторной батарее, первым делом проверяем уровень и при необходимости его корректируем. Затем заряжаем аккум и только тогда приступаем к проверке, но не сразу, а после пары часов покоя, поскольку сразу после зарядки или долива воды будут недостоверные данные.
Следует помнить, что плотность напрямую зависит от температуры воздуха, поэтому сверяйтесь с таблицей поправок, рассматриваемой выше. Сделав забор жидкости из банки аккумулятора, держите прибор на уровне глаз – ареометр должен находиться в состоянии покоя, плавать в жидкости, не касаясь стенок. Замер производится в каждом отсеке, а все показатели записываются.
Таблица определения заряженности аккумулятора по плотности электролита.
Уход за аккумуляторами
ДИАГНОСТИКА АВТОМОБИЛЬНОГО АККУМУЛЯТОРА И ЕГО ОБСЛУЖИВАНИЕ
Автомобильный аккумулятор служит для накопления электрической энергии и питания ею бортовой сети автомобиля, прежде всего электростартера двигателя при запуске. В статье речь пойдет о том, как правильно производится диагностика аккумулятора автомобиля, контроль его заряда, а также будет рассмотрена проверка уровня и плотности электролита в аккумуляторе.
Система электрооборудования большинства автомобилей 12-вольтовая, с отрицательной массой. Конструкция автомобильных аккумуляторов довольно проста: состоят они из 6 блоков свинцовых пластин с наполнителем, погруженных в емкость, которую заполняет электролит. Электролит является водным раствором серной кислоты. Каждый из блоков обеспечивает напряжение около 2-х вольт и соединяются последовательно, в сумме обеспечивая напряжение на уровне 12-13 В. Подзарядка аккумулятора автомобиля осуществляется генератором при работе двигателя. Отдельно стоят гелевые аккумуляторы, которые отличаются по устройству от кислотных аккумуляторов. Достоинства и недостатки гелевых аккумуляторов можно узнать здесь. Перед обслуживанием аккумуляторную батарею необходимо снять с автомобиля. Отсоединение аккумулятора от бортовой сети – процесс ответственный. Сначала обязательно снимается отрицательная клемма, а в процессе установки эту же клемму устанавливают последней.
ПРОВЕРКА УРОВНЯ ЭЛЕКТРОЛИТА В АККУМУЛЯТОРЕ. ПРИГОТОВЛЕНИЕ ЭЛЕКТРОЛИТА
Проверку уровня и плотности электролита следует проводить раз в три месяца, чтобы своевременно контролировать состояние батареи.
Уровень электролита в аккумуляторе проверяется через заливные отверстия при помощи полой стеклянной трубки, имеющей внутренний диаметр 4-5 мм. Один конец трубки опускается через отверстие до упора в предохранительный щиток. Отверстие трубки на другом конце плотно закрывается пальцем, после чего она вынимается. Столбик электролита, оставшегося в трубке должен быть в пределах 12-15 мм. Если в аккумуляторе имеется индикатор (тубус), то уровень электролита должен находиться на одном уровне или быть выше него на 3-5 мм.
Приготовление электролита для аккумуляторов производится только из аккумуляторной серной кислоты с добавлением дистиллированной воды. Использовать техническую серную кислоту и обычную воду не допускается, так как электролит обязан иметь высокую степень чистоты. В противном случае будет происходить ускоренная саморазрядка (сульфитация) батареи, уменьшение ее емкости и разрушение пластин. При понижении уровня электролита в результате испарения воды для восстановления требуемого объема необходимо доливать исключительно дистиллированную воду и ни в коем случае готовый электролит! В случае, когда уровень электролита превышает нормальный, его следует отсасывать резиновой грушей со стеклянным или эбонитовым наконечником. Если в аккумуляторе будет повышенный уровень электролита, то он способен выплескиваться, что также нежелательно.
Во время приготовления электролита серная кислота тонкой струйкой доливается в воду, при этом раствор перемешивается стеклянной или эбонитовой палочкой. Лить воду в кислоту запрещается, так как плотность воды намного ниже кислоты. Вода не сможет погрузиться в кислоту и останется на поверхности, при этом происходящие химические реакции вызовут нагрев и разбрызгивание кислоты. Существует вероятность получить ожоги.
Проверка уровня электролита аккумулятора
ПРОВЕРКА ПЛОТНОСТИ ЭЛЕКТРОЛИТА. ДЕНСИМЕТР
Одним из важнейших параметров электролита является его плотность. Плотность электролита в аккумуляторе проверяется денсиметром при температуре +25°С. В случае, если температура отличается от требуемой, в показания денсиметра вносятся поправки в соответствии с приведенной таблицей
В период эксплуатации аккумулятора плотность электролита непрерывно изменяется. Существует обратимое изменение плотности – нормальный интервал заряда и разряда батареи. Для новой и исправной АКБ нормальный интервал изменения плотности электролита (полный разряд – полный заряд) составляет 0,15-0,16 .
Существуют также необратимые изменения плотности, например, при испарении воды во время кипения электролита. При этом его плотность увеличивается.
Высокая плотность электролита приводит к снижению срока службы аккумуляторной батареи. Низкая плотность электролита в аккумуляторе приводит к снижению напряжения, затрудненному пуску двигателя.
Ниже приведена таблица рекомендуемой плотности электролита для климатической зоны, в которой эксплуатируется АКБ.
Плотность электролита измеряется специальным прибором – денсиметром.
Он состоит из
1 ареометра
2 резиновой груши
3 стеклянной трубки
4 наконечника.
Наконечник 4 погружается в электролит через заливное отверстие в корпусе аккумулятора и с помощью резиновой груши часть электролита засасывается внутрь стеклянной трубки. При этом ареометр (поплавок) должен всплыть в корпусе трубки, не касаясь ее стенок. После прекращения колебаний ареометра производится отсчет показаний по шкале вдоль линии жидкости. Взгляд наблюдателя должен находиться на уровне поверхности.
Определение уровня плотности электролита по денсиметру.
Проверка плотности производится в каждом отсеке АКБ отдельно, разница между показаниями не должна превышать 0,01 . Низкая плотность электролита зимой создает опасность его замерзания.
При необходимости производится корректировка плотности. Предварительно из отсека АКБ отсасывается некоторый объем электролита, вместо которого добавляется либо корректирующий электролит, либо дистиллированная вода. Низкая плотность электролита в аккумуляторе устраняется путем добавления корректирующего электролита с плотностью 1,40 . Соответственно при повышенной плотности электролита в аккумуляторе следует добавить дистиллированную воду. После этого производится зарядка батареи номинальным током в течение 30 мин с последующей выдержкой в течение 1-2 часов для лучшего перемешивания электролита и выравнивания его плотности во всех отсеках АКБ.
КАК ПРОВЕРИТЬ ЗАРЯД АККУМУЛЯТОРА
Как проверить заряд аккумулятора автомобиля? Провести эти измерения можно с помощью нагрузочной вилки. Этот прибор состоит из двух контактов, вольтметра, рукоятки и переключателя нагрузочного сопротивления. Один из вариантов представлен на рисунке.
Нагрузочное сопротивление настраивается таким образом, чтобы обеспечить ток разряда, больший значения емкости в 3 раза. К примеру, если емкость аккумулятора составляет 55 Ач, значит, ток разряда должен быть равен 165 А. Нагрузочная вилка своими контактами подключается к клеммам батареи, после чего замеряется время, в течение которого напряжение снизится с 12,6 до 6 В. Для полностью заряженной и исправной АКБ это время должно составлять не менее 3-х минут.
Заряд аккумулятора также можно оценить по величине выходного напряжения. Для его измерения необходимо воспользоваться вольтметром или мультиметром, предварительно сняв провод с минусовой клеммы АКБ. Ниже приведена таблица зависимости заряда от выходного напряжения.
Современные необслуживаемые батареи имеют индикатор заряда аккумулятора. При полной зарядке индикатор имеет зеленый цвет. При уменьшении заряда его цвет меняется от зеленого до белого или красного.
Для зарядки аккумулятора стоит воспользоваться специальным зарядным устройством. Зарядное устройство представляет собой источник постоянного тока. При подсоединении его к аккумулятору положительный полюс соединяют строго с положительной клеммой батареи, отрицательный – с отрицательной клеммой. Необходимо, чтобы выходное напряжение зарядного устройства было обязательно выше напряжения АКБ для обеспечения прохождения зарядного тока.
Автомобильный аккумулятор заряжается номинальным током, равным 10% от номинальной емкости батареи. Например, при емкости 60 Ач номинальный ток зарядки должен составлять 6 А. При этом зарядка может продолжаться до 13-15 часов. Пробки заливных отверстий должны быть обязательно открыты!
Зарядка аккумуляторной батареи считается завершенной, если наблюдается постоянство плотности электролита и выходного напряжения в течение 2-х часов.
Своевременная проверка электролита и зарядка аккумулятора должна стать хорошей привычкой для автолюбителя. Это позволит продлить срок службы батареи, обеспечить бесперебойное питание всех электроприборов автомобиля и сэкономить средства.
Концентрация электролита — обзор
2.3.4 Гидратация в концентрированных растворах
По мере увеличения концентрации электролита количество молекул воды во вторичной гидратной сфере уменьшается. Следовательно, происходит усиление связи между катионом металла и гидратными водами во внутренней сфере (Choppin, Jensen, 2006). Основываясь на ЯМР-исследованиях трехвалентных актинидов и лантаноидов, Чоппин пришел к выводу, что комплексообразование внутренней сферы перхлорат-ионами не происходит ниже примерно 8–10 М (Choppin, Labonne-Wall, 1997).Множественные равновесия для системы уранилхлорида (UO 2 Cl 2 (H 2 O) 2 , UO 2 Cl 3 (H 2 O) — и UO 2 Cl 4 2–) использовались для отделения урана от его дочерних продуктов или других металлов. Поскольку Th 4 + не образует анионных хлоридных комплексов, он удерживается на катионообменной смоле, в то время как анионные хлоридные комплексы UO 2 2 + проходят через колонку в элюате.Альтернативно такие анионные комплексы можно удерживать на анионообменной колонке.
Число гидратации Eu (III) остается относительно постоянным в соляной кислоте примерно до 6–8 M, выше которой концентрация уменьшается. То же самое верно и для числа гидратации Cm (III) в HCl, которое начинает снижаться примерно при 5 M HCl. Эта разница между (Eu 3 + и Cm 3 + ) отражает большее комплексообразование трехвалентного иона актинида с относительно мягким анионом Cl —.Разница в комплексообразовании хлоридов использовалась для обеспечения эффективного отделения трехвалентных актинидов от трехвалентных актинидов в концентрированных растворах HCl путем пропускания через колонки с катионообменной смолой с 1950-х годов (Diamond et al., 1954).
Нитратные комплексы для четырехвалентных актинидов, например Th 4 + и Pu 4 + , чрезвычайно важны в процессах разделения и очистки актинидов. Нитрат-ионы начинают образовывать комплексы внутренней сферы при более низких концентрациях, чем хлорид-анионы; это наблюдение подтверждается уменьшением числа гидратации катиона даже при относительно более низких концентрациях (Choppin, Jensen, 2006).Однако, поскольку атомы кислорода нитрата являются твердыми донорами, нет никаких доказательств какого-либо ковалентного усиления его связывания, как это видно с анионами хлорида для трехвалентных катионов актинидов по сравнению с катионами лантанидов (Choppin, Jensen, 2006). В процессах разделения и очистки чрезвычайно важны нитратные комплексы актинидов. Раствор нитрат-азотной кислоты является наиболее распространенной водной средой в процессах разделения ядер. В случае нейтральных экстрагентов, таких как трибутилфосфат (TBP), карбамоилметилфосфиноксид (CMPO) или дипиколинамиды (DPA), он обеспечивает нитратные единицы, необходимые для компенсации заряда катионов актинидов для обеспечения экстракции.Комплексообразование нитрата с шестивалентными ионами актинида происходит очень слабо, и определение констант образования для разновидностей водного раствора нитрата является чрезвычайно трудным. В водных условиях с высокими концентрациями азотной кислоты комплексы формы AnO 2 (NO 3 ) (H 2 O) x + , AnO 2 (NO 3 ) 2 (H 2 O) 2 и AnO 2 (NO 3 ) 3 — (An = U, Np, Pu), вероятно, будут присутствовать.Лимитирующим веществом в ряду нитратов является комплекс гексанитрато, An (NO 3 ) 6 2– (Matonic et al., 2002). Известно комплексообразование пятивалентных ионов Pa и Np нитратом; однако доступны ограниченные термодинамические и структурные данные. Предполагаемая стехиометрия для видов Np (V) — NpO 2 (NO 3 ) (H 2 O) x . Для протактиния, который легко гидролизуется, были предложены смешанные гидроксо / нитрато- или оксо / нитрато-комплексы.
Фториды и хлориды являются наиболее изученными актино-галогенидными системами, и они очень важны для процессов пирообработки и электрорафинирования.
Карбоновые кислоты прочно связаны с ионами актинидов. Первичный способ связывания простых карбоновых кислот — бидентатный, тогда как в комплексах поликарбоновых кислот карбоксилаты имеют тенденцию к монодентатной координации с ионом металла. Сродство низковалентных актинидов к этим лигандам увеличивается с увеличением дентальности лиганда, например, этилендиаминтетраацетата (ЭДТА) >>> ацетата.Для An 4 + лиганд EDTA является гексадентатным с конформацией скручивания (спиральная конформация, охватывающая ион металла, а не инкапсулирующая ион металла в центральной полости, как триподальные или макробициклические лиганды). Диэтилентриамин-N, N, N ‘, N ″, N ″ -пентаацетат (DTPA) имеет еще более высокое сродство к ионам An 3 + и An 4 + .
Температурная коррекция удельного веса: Служба технической поддержки
При измерении удельного веса важно внести поправку на температуру.См. Таблицу ниже:
В приведенной выше таблице показаны фактические показания ареометра кислоты при удельном весе 1,265 при 25ºC (77ºF). Когда кислота охлаждается, она сжимается, и кажущаяся плотность увеличивается, а когда она нагревается, она расширяется, и кажущаяся плотность уменьшается. Это важно при определении уровня заряда. Если температура электролита составляет 38 ° C (100 ° F), а значение плотности составляет 1,258 и не корректируется, может произойти ненужная зарядка. Это сократит срок службы батареи, приведет к потере электроэнергии и излишнему газу батареи.В этом случае потребуется дальнейшее обслуживание из-за дополнительного полива.
Лучший способ измерить степень заряда аккумулятора — это измерить удельный вес. Это можно делать под нагрузкой, но следует соблюдать осторожность, и никогда не рекомендуется, если погрузчик находится в эксплуатации. В следующей таблице показаны различные уровни заряда и соответствующая скорректированная удельная масса аккумулятора при полной зарядке при 1,265 и 25 ° C (77 ° F).
Полная зарядка при 1,265 при 25ºC (77ºF)
% Заряд Удельный вес
100% 1.255 — 1,275
75% 1,215 — 1,235
50% 1,180 — 1.200
25% 1,155–1,165
0% 1,110-1,130
Емкость аккумулятора и время зарядки аккумулятора основаны на каждой ячейке, имеющей температуру электролита 25 ° C (77 ° F). Температура ниже номинальной 25 ° C (77 ° F) снижает эффективную емкость и увеличивает время восстановления полной зарядки аккумулятора. Температура выше 25 ° C (77 ° F) немного увеличит емкость, но также увеличит саморазряд и сократит срок службы батареи.
Основные проблемы возникают при экстремальных температурах. Это диапазон от 4ºC (40ºF) до 38ºC (100ºF). Электролит в полностью заряженной батарее имеет точку замерзания приблизительно –85ºF (-65ºC). Однако электролит в полностью разряженной батарее с низким удельным весом имеет гораздо более высокую точку замерзания; чуть ниже 0ºC (32ºF). Полностью разряженный аккумулятор может замерзнуть ниже 4ºC (40ºF), и его следует немедленно зарядить. Повреждения, вызванные замерзанием, обычно не подлежат восстановлению и требуют замены.
Более низкая температура — меньшая мощность, более интенсивная цикличность.
Более высокая температура — большая емкость, больший саморазряд и износ аккумулятора.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться у системного администратора.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Влияние модуля электролита на локальную плотность тока на кончике дендрита на литий-металлическом электроде
Интерес к переносу ионов металлическими литиевыми электродами возрастает из-за того, что в настоящее время уделяется особое внимание увеличению плотности энергии перезаряжаемых литиевых батарей. 1 Теоретически замена графитового электрода на металлический литий в литий-ионной батарее приведет к увеличению плотности гравиметрической энергии на 40%. 2 Химический состав аккумуляторов с плотностью энергии, значительно превышающей химический состав литий-ионных аккумуляторов, таких как литий-сера и литий-воздух, зависят от наличия перезаряжаемого металлического литиевого анода. Электроосаждение металлических пленок также является неотъемлемой частью производства и использования широкого спектра устройств, от бытовой электроники до накопителей энергии. 3–5 Обычно как в аккумуляторных батареях, так и при электрохимической обработке металлы электроосаждены из жидких электролитов. 6–8 Однако последние достижения в области полимерных и керамических электролитов позволили осаждение (и удаление) металлов из электролитов с высоким модулем упругости. 9–11 Эти жесткие электролитические материалы влияют на механизм электроосаждения металлов. В частности, известно, что жесткие полимерные электролиты подавляют рост дендритов в батареях, содержащих анод из металлического лития. 12,13 Подавление роста выступающих металлических структур лития, таких как дендриты и глобулы, необходимо для безопасного и надежного использования аккумуляторных батарей с высокой плотностью энергии с металлическими анодами. 14,15
Многочисленные экспериментальные исследования были посвящены вопросу роста дендритов в литиевых батареях. 8,16–25 Хотя увеличение плотности тока вблизи дендрита или глобулы, возможно, является наиболее важной движущей силой в этом процессе, это увеличение до сих пор ускользало от экспериментального исследования.Насколько нам известно, в предыдущих исследованиях элементов, содержащих электроды из металлического лития, сообщалось только о средней плотности тока. 26–28 В этом исследовании мы используем рентгеновскую микротомографию с временным разрешением для количественной оценки топологии металлического литиевого электрода и локальной плотности тока по всему электроду симметричной литий-литиевой ячейки с твердым блок-сополимерным электролитом в качестве электролита. функция заряда прошла. Мы, естественно, сосредотачиваем свое внимание на областях внутри клетки в непосредственной близости от растущих глобул.Наши эксперименты также позволяют определить локальную деформацию в твердом полимерном электролите, что, в свою очередь, позволяет оценить локальное напряжение. Мы представляем данные о взаимодействии между локальным напряжением и осаждением лития в окрестности вершины выступа.
Обычно при моделировании роста дендрита лития предполагается, что площадь проекции или поперечное сечение дендрита на границе между электродом и электролитом остается постоянным, поскольку он распространяется через электролит, как удлиняющаяся игла. 29–31 В случае роста глобулы через твердый электролит, мы показываем, что эта проектируемая площадь увеличивается по мере распространения глобулы через электролит. Это увеличение площади притупляет наконечник, значительно замедляя вертикальный рост глобул лития. Следовательно, увеличение модуля упругости электролита не только подавляет рост глобул за счет замедления кинетики осаждения на кончике глобулы, но также приводит к увеличению радиуса кривизны на кончике, что приводит к более медленному росту за счет делокализации тока.
Эта статья является частью серии исследований циклирования литий-литиевых элементов с помощью рентгеновской микротомографии. После первоначального обнаружения образования глобул лития в циклических клетках с помощью рентгеновской микроскопии ex situ было проведено множество экспериментов для определения влияния таких параметров, как температура и время зарядки, на морфологию глобул в клетках с использованием твердой блок-сополимерной электролитной мембраны. 13,32,33 Затем были разработаны клетки, которые вписывались в пучок рентгеновской микротомографии для определения характеристик роста глобул с остановкой движения.Качественное описание этих результатов было опубликовано ранее. 2 Настоящее исследование направлено на количественную оценку кинетики осаждения лития на глобуле и вблизи нее по мере ее прохождения через твердый полимерный электролит.
Полистирол- b -поли (этиленоксид) синтезировали анионной полимеризацией, как описано ранее. 34,35 Молекулярная масса блок-сополимера составляла 240–260 кг / моль с объемной долей поли (этиленоксида) 0,5 и дисперсностью 1.26. После синтеза полимер сушили вымораживанием и хранили в перчаточном боксе, заполненном аргоном, где уровни кислорода и воды контролировались и оставались ниже 5 частей на миллион.
Чтобы приготовить электролитную мембрану, блок-сополимер растворяли в N-метил-2-пирролидоне (NMP) с литиевой бис (трифторметановой) сульфонамидной солью (LiTFSI) в концентрации 0,085 Li + для остатков этиленоксида. Раствор выливали на плоскую поверхность, покрытую никелевой фольгой, и распределяли в пленку с помощью ракельного ножа.Пленке давали высохнуть на плоской поверхности при 60 ° C в течение ночи. На этом этапе пленка была снята с никелевой фольги пинцетом. Отдельно стоящей пленке давали высохнуть в течение дополнительных 24 часов при 90 ° C под вакуумом в передней камере перчаточного ящика. После высыхания отдельно стоящую пленку из твердого полимерного электролита толщиной 30 мкм оборачивали никелевой фольгой и хранили в герметичном контейнере внутри перчаточного бокса. Фольга металлического лития чистотой 99,9% была приобретена у FMC Lithium. Рулон фольги толщиной 150 мкм хранился в эксикаторе внутри перчаточного бокса.
Симметричные образцы литий — полимерный электролит — литий для покадровой рентгеновской микротомографии были собраны следующим образом. Сначала использовали круглый металлический пуансон диаметром 13 мм, чтобы вырезать кусок электролита из отдельно стоящей пленки полимерного электролита. Три слоя металлической литиевой фольги были уложены друг на друга на чистом куске никелевой фольги, чтобы создать литиевый электрод толщиной 450 мкм с никелевой фольгой. Круглый металлический пуансон диаметром 11 мм использовался для штамповки двух литиевых электродов из пакета лития на никелевой фольге.Два литиевых электрода помещали по обе стороны от мембраны из полимерного электролита. Прокладка из нержавеющей стали толщиной 0,57 мм была помещена на одну сторону образца, а прокладка из нержавеющей стали толщиной 0,35 мм была установлена на другой стороне образца. Эти прокладки удерживали образец в плоском состоянии, что было важно для визуализации. Алюминиевые язычки токосъемника помещали с обеих сторон образца, и образец герметично закрывали в алюминиевом пакете, облицованном нейлоном и полипропиленом.
Этот толстый литиевый электрод с никелевой фольгой был полезен для покадровой рентгеновской микротомографии, поскольку литий создавал область с низким поглощением рентгеновских лучей вокруг границы раздела литий-полимер.Если материалы, которые сильно поглощают рентгеновское излучение 22 кэВ, такие как никель или нержавеющая сталь, находятся на пути рентгеновского луча, они, как правило, вызывают значительные артефакты в реконструированных объемах, скрывая интересующие особенности литий-полимерного интерфейс. Толстые литиевые электроды отодвинули эти хорошо поглощающие материалы от интересующей области, что позволило получить четкие реконструированные объемы. Алюминиевые вкладки были достаточно прозрачными для рентгеновского излучения, чтобы получать изображения хорошего качества, даже несмотря на то, что они блокировали путь луча.Язычки не контактировали напрямую с литиевой фольгой, поскольку известно, что алюминий реагирует с литием. Прокладки из нержавеющей стали, расположенные между образцом, имели разную толщину, так что при вакуумной герметизации граница раздела литий-полимер располагалась немного выше центральной плоскости образца, где избыток материала мешочка от вакуумного уплотнения мог добавлять шум к полученным изображениям томографии. Собрана серия из шести образцов этого типа.
Один из образцов был прокручен до отказа из-за короткого замыкания, используя следующую процедуру.Пропускали ток 0,175 мА / см 2 лития в течение четырех часов с последующим 45-минутным отдыхом. Затем пропускали ток -0,175 мА / см 2 в течение четырех часов с последующим 45-минутным отдыхом. Эту процедуру цикла повторяли до тех пор, пока образец не вышел из строя из-за короткого замыкания после 32 циклов. Затем цикл других пяти образцов был выполнен таким же образом, но был остановлен после 17 циклов. Намерение состояло в том, чтобы приблизить образцы к разрушению, чтобы сократить время прохождения луча, необходимое для того, чтобы увидеть, как образец выходит из строя из-за короткого замыкания.
На этом этапе один из пяти образцов был визуализирован с помощью микротомографии с жесткими рентгеновскими лучами, а затем поляризован в течение дополнительных 4,5 часов. Эту поляризацию, при которой заряд проходил в одном направлении в течение 4,5 часов, повторяли четырнадцать раз с рентгеновскими микротомографическими изображениями, полученными с шагом в 4,5 часа. Затем образец поляризовали в течение 31 часа перед следующим изображением. Наконец, образец был поляризован в течение дополнительных 114 часов, когда он, наконец, вышел из строя из-за короткого замыкания и был отображен. Вся электрохимическая поляризация и циклы выполнялись, пока образец выдерживался при 90 ° C в печи.Из-за ограниченного доступа к прибору томографа покадровая съемка была выполнена только на одном образце. Литиевые глобулы аналогичного размера и формы были замечены в посмертных экспериментах с двумя дополнительными образцами, которые циклически переключались и поляризовались таким же образом.
Образец удаляли из оборудования для электрохимического циклирования и охлаждали до комнатной температуры перед каждым сеансом визуализации. Визуализацию выполняли на канале жесткой рентгеновской микротомографии в Advanced Light Source (Beamline 8.3.2). Параметры, используемые для изображения образца, приведены в дополнительной таблице 1. Самые большие глобулы были обнаружены в окончательных реконструированных объемах и были отслежены до исходного изображения, где они еще не начали формироваться. Программа обработки изображений Avizo использовалась для измерения высоты, объема и площади глобул.
Большие реконструированные объемы были обрезаны, чтобы они содержали только глобулу, закоротившую ячейку. Последовательность обрезанных реконструированных объемов была преобразована в двоичную форму для последующего анализа в Matlab.Положение нижней границы раздела литий-полимер рассчитывалось в Matlab относительно фиксированного эталона, нижней части электрода. Плотность тока i jk в пикселе с индексами j , k была рассчитана с использованием объема нанесенного лития V jk в этом пикселе:
, где ρ — плотность металлического лития, F — постоянная Фарадея, M Li — молекулярная масса металлического лития, a — площадь пикселя в см 2 и t — время.Этот расчет предполагает, что весь заряд, нанесенный на литиевый анод, нанесен в виде металлического лития. Предполагалось, что образование SEI происходит во время циклов кондиционирования.
Данные томографии непосредственно показали смещение полимерного электролита на границе раздела электродов. Эти измерения использовались для определения локальных напряжений вблизи глобулы лития следующим образом. Во-первых, поскольку глобула приблизительно осесимметрична, была построена гладкая осесимметричная поверхность, как описано в дополнительной информации, чтобы приблизительно представить границу между глобулой и электролитом для каждого из отображаемых состояний.Затем сглаженной поверхности придавали параболическую форму, так что наклон кривой на вершине глобулы был равен нулю, что соответствовало томографическим изображениям.
Для каждой поверхности была определена цилиндрическая система координат с осью z , совпадающей с осью симметрии поверхности. Переменная r была определена как перпендикулярное расстояние к оси z . За исключением непосредственной близости от глобулы, поверхности лития представляют собой приблизительно параллельные плоскости, поэтому начало координат было принято за пересечение оси z с плоскостью, из которой растет глобула.Положительное направление z было определено как направление роста глобулы.
Поскольку система является осесимметричной, а механический отклик электролита представляет интерес, необходимо было решить только смещение электролита в пределах любой плоскости r — z .
Области электролита вблизи глобул испытали сильные смещения. Напряжения были рассчитаны с использованием формулировки большой деформации. Численная реализация близко соответствует частям работы, подробно описанной в предыдущей статье. 36 Обзор математической формулировки настоящей модели описан ниже, а дополнительные детали реализации представлены в дополнительном материале.
Уравнение импульса
Поскольку инерция незначительна в экспериментальных условиях, смещение электролита описывается уравнением механического равновесия, выраженным в пространственном описании как:
Нижний индекс x указывает, что дифференциация выполняется относительно текущих позиций; в моделях с конечной деформацией, в которых материал может испытывать значительные смещения, необходимо четко определить значение положения.Тензор напряжений Коши, σ , моделируется с использованием закона линейной упругости Гука:
, где модуль Юнга E был определен из экспериментальных реологических измерений, ν — коэффициент Пуассона, I — тензор идентичности и tr E — след тензора деформации Альманси E . Модуль сдвига для этого полимера был измерен ранее и составляет примерно 1 × 10 6 Па в пределе низкой скорости деформации. 13 Это значение модуля сдвига было преобразовано в модуль Юнга с учетом коэффициента Пуассона 0,33. В этой модели конечной деформации E можно вычислить как
, где градиент деформации F определяется как
Нижний индекс x 0 аналогично указывает, что дифференцирование должно выполняться относительно начальных положений, а x относится к текущему положению материала.
Отметим, что использование закона Гука в качестве определяющего уравнения может привести к завышению прогнозов напряжений при больших перемещениях; однако в настоящее время отсутствуют определяющие уравнения, специально адаптированные для описания этого материала электролита.
Граничные условия
Смоделированная область электролита простирается в направлении z от одного литиевого электрода к другому. Простая проверка данных томографии не дает всей необходимой информации о смещении границ, поскольку область электролита не содержит идентифицируемых маркеров, поэтому необходимо сделать некоторые предположения.Предполагается, что электролит остается прочно прикрепленным к обеим литиевым поверхностям, так что смещения вдоль верхней границы раздела нет. Предполагается, что смещение вдоль нижней границы раздела (включая границу с глобулой) происходит только в направлении z . Кроме того, поскольку это осесимметричная система, на оси нет смещения в направлении — , а в осевом направлении на управляющей поверхности, совпадающей с осью, имеется нулевое напряжение.
На внешней радиальной поверхности первоначально цилиндрического контрольного объема накладывается граничное условие простого смещения, как показано на рисунке 1. Электролит закреплен на верхней и нижней границах раздела, поэтому внешняя поверхность первоначально цилиндрического контрольного объема может быть описывается кривой, описывающей смещение как функцию z. Истинное смещение внешней радиальной поверхности можно описать с помощью ряда синусов Фурье. Для простоты предполагается, что вертикального смещения нет и что горизонтальное смещение этой внешней поверхности (первоначально при r = R) определяется выражением
На рис. 1 представлена схема расчетной области в исходном и деформированном состоянии.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 1. Схема расчетной области в начальном и деформированном состояниях. Верхняя и нижняя поверхности остаются неподвижными, за исключением области глобулы. Внешний край домена смещается наружу, чтобы компенсировать проникновение глобулы и ограниченную сжимаемость электролита.
В этой форме используется только первый непостоянный член синусоидального ряда Фурье.Здесь z = Z — вертикальное положение верхней поверхности лития. Величина A была определена из оценки общего изменения объема, испытываемого электролитом в пределах контрольного объема, и рассчитана путем решения следующего квадратного уравнения в A :
Вывод этого уравнения приведен в дополнительной информации. При этом моделировании для полимерного электролита были приняты коэффициент Пуассона 0,33 и модуль сдвига 1 × 10 6 Па.
В нашем подходе локальная плотность тока рассчитывалась на основе различий между последовательными изображениями, в то время как напряжение рассчитывалось только на основе отдельного изображения. Количество заряда, прошедшего перед первым из двух изображений, используемых для расчета плотности тока, указано в подписях к рисункам. Например, когда для серии данных плотности тока сообщается, что пройденный заряд составляет 0 Кл / см 2 , эта плотность тока была получена путем анализа изображений, на которых количество заряда, нанесенного до изображений, составляло 0 Кл / см 2 и 8.27 С / см 2 .
Теоретически, модуль электролита должен быть примерно в два раза больше, чем у металлического лития, чтобы полностью подавить рост дендритов лития. 37 Металлический литий имеет модуль сдвига при комнатной температуре около 4 × 10 9 Па. 38 Полистирол- b -поли (этиленоксид) с молекулярной массой 240–260 кг / моль имеет модуль сдвига, который на 2–3 порядка ниже, чем при примерно 10 6 –10 7 Па при 90 ° C. 13 Гомополимер поли (этиленоксида) с молекулярной массой 360 кг / моль имеет модуль сдвига около 10 5 Па. 12 Отношение модуля сдвига электролита к металлическому литию составляет приблизительно 0,0003 для нашего полистирол — b — полиэтиленоксидная мембрана и 0,00003 для поли (этиленоксидного) гомополимера. Учитывая, что эти отношения намного меньше двух, даже усиленная мембрана из блок-сополимера-электролита слишком мягкая, чтобы полностью подавить рост дендритов в соответствии с теоретическими моделями.
На рис. 2а показана зависимость высоты глобулярного выступа от времени для двух самых быстрорастущих глобул лития, измеренных в нашем исследовании, названных глобула 1 и глобула 2. На рис. 2b показана рентгеновская микротомограмма глобулы лития после ее прокола. электролита и вызвал отказ элемента из-за короткого замыкания. Темно-серая фаза на изображении — это металлический литий, а светло-серая фаза — полимерный электролит. В основании глобулы лития видна примесная частица. Эта частица изначально находилась на границе раздела литий-полимер, как показано на рисунке 3.Белая стрелка указывает высоту части глобулы, которая выступает в блок-сополимерный электролит и в верхний литиевый электрод. Кроме того, в исследовании, проведенном Rosso et al., Отслеживали высоту выступа глобулы по мере ее роста через гомополимер поли (этиленоксида) 300 кг / моль. показан для сравнения. 23 В обоих исследованиях плотность приложенного тока составляла 0,175 мА / см 2 , а отклик по напряжению составлял около 0,07 В. Основное различие между двумя исследованиями заключается в толщине образца.В исследовании Rosso толщина электролита составляла 1,2 мм, в то время как толщина электролита в нашем исследовании составляла 30 мкм. Можно было бы ожидать, что более сильный градиент концентрации соли образуется в более толстом электролите с аналогичными транспортными свойствами для данной плотности тока. Влияние этой разницы толщин на морфологию глобул неизвестно.
Увеличить Уменьшить Сбросить размер изображения
Рис. 2. a Скорость роста глобул лития через полиэтиленоксид, усиленный сополимеризацией с полистиролом (SEO), сравнивается со скоростью роста дендрита лития через традиционный гомополимерный электролит на основе поли (этиленоксида). как сообщает Россо, М.и др. . в 2006 г. Высота выступа определяется высотой части литиевой глобулы, выступающей в слой полимерного электролита, как показано двойной белой стрелкой на b. Частица примеси видна в основании глобулы, как показано нижней белой стрелкой. b Рентгеновская томограмма, показывающая, что глобула 2 пробивает электролитную мембрану SEO. Темно-серая фаза представляет собой металлический литий, а светло-серая фаза — полимерный электролит.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 3. Верхний ряд: рентгеновские томограммы плоскости yz в симметричном литий-полимерном электролит-литиевом элементе, показывающие рост глобулы лития. Темно-серая фаза представляет собой металлический литий, а светло-серая фаза — полимерный электролит. Маленькое светло-серое пятно в основании глобулы — это примесная частица, которая изначально присутствовала в литиевой фольге. Средний ряд: соответствующая плоскость xy, показывающая поверхность раздела между нижним литиевым электродом и полимерным электролитом. Круглая структура в центре изображения — это растущая глобула лития.Нижний ряд: 3D-изображения из рентгеновских микротомографических изображений, показывающие рост глобулы лития. Светло-серая область — это литиевый электрод, на котором осажден литий. Голубая область — это мембрана из твердого полимерного электролита. Светло-красная структура в основании глобулы — это примесная частица, которая изначально находилась в фольге металлического лития. Серая глобула лития для наглядности обведена проволочной сеткой. Белые стрелки указывают на частицу примеси, которая изначально присутствовала на границе раздела литий-полимер.Перед каждым изображением проходит заряд 0 C / см 2 b 8,27 C / см 2 c 16,53 C / см 2 d 35,82 C / см 2 e 54,72 C / см 2 .
Из данных, показанных на рисунке 2, очевидно, что скорость роста выступов лития значительно ниже в усиленном полистиролом блок-сополимерном электролите. Самая быстрорастущая глобула лития, измеренная в этом эксперименте, выступала в электролит полистирол-b -поли (этиленоксид) со скоростью 0.37 мкм / час. В случае гомополимера поли (этиленоксида) глобула росла со скоростью 11 мкм / час, что на порядок быстрее, чем в блок-сополимере. Удивительно, что изменение модуля упругости электролита с 10 5 до 10 7 Па оказывает такое большое влияние на осаждение лития, поскольку оба значения значительно ниже модуля упругости металлического лития. Следующая серия рисунков поможет нам понять это явление.
На рис. 3 показаны рентгеновские томограммы и трехмерные изображения глобулы 2 на пяти стадиях во время ее роста через блок-сополимерный электролит.Исходное изображение, показанное в части 3а, показывает частицу примеси на нижней границе раздела литий-полимер. Шаровидная структура, видимая на последующих изображениях, еще не начала формироваться. Следующие изображения, показанные в частях 3b, 3c, 3d и 3e, показывают то же место в образце после 8,27 ° C / см 2 , 16,53 ° C / см 2 , 35,82 ° C / см 2 и 54,72 ° C / см 2 лития осаждалось на весь нижний литиевый электрод, как измеряли по показаниям потенциостата. В верхнем ряду показана плоскость yz через растущую глобулу лития.Изображения выравниваются по нижней части литиевого электрода, так что абсолютное положение изображения остается неизменным от кадра к кадру. Полимерный электролит поднимается по мере отделения лития от верхнего электрода и его осаждения на нижнем электроде. Частица примеси, которая первоначально находилась на границе раздела литий-полимер на рис. 3а, остается в основании глобулы лития по мере ее роста. Яркая полоса, идущая в направлении y от границы раздела полимерного электролита через глобулу лития, является артефактом изображения, вызванным длинной и яркой границей раздела литий-полимер.В центральном ряду показана плоскость xy через границу раздела между нижним литиевым электродом и полимерным электролитом для той же литиевой глобулы. Изображения в плоскостях zy, xy и yz получаются путем визуализации ортосрезов через стопку реконструированных рентгеновских микротомографических изображений. В нижнем ряду показан 3D-рендеринг растущей глобулы лития. Нижний серый слой — это нижний металлический литиевый электрод в литий-полимерно-литиевой ячейке. На объемных изображениях голубой слой представляет собой блок-сополимерную электролитную мембрану.Верхний литиевый электрод не был включен в рендеринг для ясности. Образующаяся в центре изображений темно-серая глобула заполнена литием. Нижний литиевый электрод становился толще, поскольку литий отделялся от верхнего электрода и осаждался на нижнем электроде. Глобула лития выросла в электролит по мере осаждения лития. В конце концов, глобула лития пробила электролитную мембрану, вызвав короткое замыкание.
На рис. 4 показаны высота, объем и площадь глобулы как функция толщины лития, осажденного вблизи глобулы, t Li .Абсцисса на рисунке 4 представляет толщину лития, нанесенного примерно на 5–10 мкм от края глобулы, измеренную по изображениям рентгеновской микротомографии. Высота глобулы, измеренная от основания эллипсоидальной глобулы до кончика, увеличивается лишь немного быстрее, чем окружающий литиевый электрод. Положительное отклонение от линии y = x на рисунке 4a соответствует высоте кончика глобулы, выступающей в электролит. Остальная часть глобулы оказывается захороненной плоскими отложениями лития, окружающими глобулу.
Увеличить Уменьшить Сбросить размер изображения
Рис. 4. Высота (a), объем (b) и площадь (c) двух наиболее быстро растущих глобул лития показаны как функция от количества осажденного лития. Обратите внимание, что все эти количества, включая количество осажденного лития, измеряются непосредственно с помощью рентгеновских микротомографических изображений. На вставленных изображениях указано, что определяется как высота, объем и площадь глобулы.Разница между высотой глобулы, показанной в a и линией y = x, представляет собой высоту глобулярного выступа в мембране полимерного электролита.
Поскольку рентгеновские микротомографические изображения дают трехмерную информацию о внутренней части образца, можно измерить объем глобулы как функцию осажденного лития, t Li . Объем глобулы, V г , увеличивается квадратично как функция т Li (кривая на рисунке 4b представляет V г = 33 т 2 Li + 915 т Li — 4437).Можно также измерить площадь глобулы на плоской границе раздела нижнего литиевого электрода и электролита. Любопытно, что из рисунка 4c видно, что глобула увеличивалась не только по высоте, но и по площади. Глобула быстро расширялась на начальных стадиях роста, затем начала выравниваться, достигнув площади около 4000–5000 мкм 2 .
Поскольку метод визуализации рентгеновской микротомографии позволяет измерять толщину лития, нанесенного в каждой точке нижнего литиевого электрода, можно использовать закон Фарадея для расчета количества заряда, нанесенного в каждой точке на поверхности нижнего литиевого электрода.С помощью двух последовательных изображений можно отобразить количество заряда, нанесенного на данный пиксель на поверхность лития. Разделение этого значения на временной интервал между изображениями дает локальную плотность тока (уравнение 1). На рис. 5 показаны карты плотности тока для четырех различных стадий роста глобулы лития 2. Карты, показанные в верхнем ряду, дают топографию границы раздела между нижним литиевым электродом и полимерным электролитом. В центре карт видна вершина глобулы лития.Цвет соответствует плотности тока. Общая средняя плотность тока, обеспечиваемая потенциостатом, составляла 0,175 мА / см 2 . Плотность тока 0 мА / см 2 отображается черным на цветовой шкале, а 0,175 мА / см 2 отображается темно-синим. Обратите внимание, что на ранних стадиях роста глобул большая часть текущей карты темно-синего цвета. Это указывает на количественное соответствие между локальным током, определенным с помощью рентгеновской микротомографии, и током, подаваемым потенциостатом.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 5. Локальная плотность тока нанесена на карту для четырех стадий роста глобулы лития 2. a На начальных стадиях возмущение на границе раздела литий / электролит приводило к плотности тока выше средней на вершине маленькой глобулы. Эту плотность тока измеряли между моментами времени 0 C / см 2 и 8,27 C / см 2 . b По мере роста глобулы ток делокализовался от кончика глобулы. Эта карта была измерена между временными точками 8,27 C / см 2 и 16.53 С / см 2 . c Эта делокализация была более выраженной между 16,53 C / см 2 и 35,82 C / см 2 . d Поскольку площадь глобулы увеличивалась на поздних стадиях роста глобулы, текущая концентрация, вызванная глобулами, значительно снижалась. Эта карта была измерена между временными точками 35,82 C / см 2 и 54,72 C / см 2 .
На рисунке 5a плотность тока была сосредоточена на вершине выступающей глобулы лития. Ожидается, что эта текущая концентрация на кончике выступа основана на традиционных теориях роста дендритов. 29,30 Однако по мере роста глобулы плотность тока делокализовалась от кончика выступа к периметру. Это дает ясную картину расширения глобулы лития. В конце концов глобула стала достаточно широкой, так что плотность тока на глобуле лития была лишь немного выше, чем на окружающем ее плоском электроде.
Мы предполагаем, что эффект делокализации тока, показанный на рисунках 5b и 5c, вызван механической жесткостью полимерного электролита.Поскольку блок-сополимерный электролит является жестким, существует штраф за событие восстановления иона лития на кончике глобулы, где полимер сильно деформирован. Чтобы количественно оценить этот эффект, мы используем ранее измеренные значения модулей в сочетании с визуализацией рентгеновской микротомографии, представленной в этом исследовании, для расчета и картирования напряжения в полимере. 13
На рисунке 6 показана карта вертикальной составляющей вектора напряжения на первоначально горизонтальных управляющих поверхностях в полимерном электролите из растущей глобулы лития.Вектор напряжения основан на начальной площади и силе относительно фиксированного количества материала. Одномерный профиль глобулы представляет собой бесцветную область в левой нижней части графика. Кончик глобулы находится в радиальном положении 0 мкм. Этот вектор напряжения, выраженный в Па, показан цветом на графике. Карты напряжений были рассчитаны на основе формы глобулы после осаждения лития 8,27 Кл / см 2 , 16,53 Кл / см 2 , 35,82 Кл / см 2 и 54,72 Кл / см 2 на нижний литий. электрод, как показано на рисунках 6a – 6d.График на рисунке 6d показывает максимальные сжимающие и растягивающие напряжения в полимере в зависимости от пройденного заряда. На ранних стадиях роста глобула росла в основном в высоту, и, следовательно, как сжимающее напряжение на вершине глобулы, так и растягивающее напряжение по периметру глобулы существенно увеличивались между 8,27 Кл / см 2 и 16,53 Кл / см 2 , как показано на рисунке 5e. Эти напряжения ослабляются по мере расширения глобулы на промежуточных стадиях роста. Максимальное сжимающее напряжение возникало на конечном расстоянии над наконечником, а не на наконечнике.Это следствие сильного растяжения электролита.
Увеличить Уменьшить Сбросить размер изображения
Рис. 6. Карты напряжений в полимерном электролите из-за сжатия растущей глобулы лития. Напряжения основаны на модуле электролита 10 6 Па. Полимерный электролит испытывал напряжения сжатия на вершине глобулы лития и напряжения растяжения по периметру.a 8,27 C / см 2 b 16,53 C / см 2 c 35,82 C / см 2 d 54,72 C / см 2 e Максимальные сжимающие (черные кружки) и растягивающие (серые квадраты) напряжения показаны как функция пройденного заряда.
Карты плотности тока, показанные на рисунке 5, были усреднены в радиальном направлении вокруг вершины глобулы, и полученные кривые показаны на рисунке 7a. Пиковая плотность тока смещается от вершины глобулы к периметру по мере роста глобулы. При прохождении заряда было меньше 16.53 Кл / см 2 , плотность тока в радиальных положениях между 20 и 80 мкм от центра глобулы составляла около 0,175 мА / см 2 , как и ожидалось на основе настройки потенциостата. На более поздних стадиях осаждения плотность тока в радиальных положениях между 50 и 80 мкм от центра глобулы увеличивалась до значения 0,3 мА / см 2 . Причина увеличения средней плотности тока неизвестна. Однако стоит отметить, что толщина литиевого слоя, нанесенного на основе настройки потенциостата в этом переходе, составляет 48 мкм, что существенно больше толщины электролита.Небольшие дефекты ячейки могут влиять на локальные плотности тока в этом режиме.
Увеличить Уменьшить Сбросить размер изображения
Рис. 7. a Кривые, показывающие плотность тока как функцию радиального расстояния от кончика глобулы для пяти стадий роста глобулы. b Напряжение на границе раздела литий-полимер как функция радиального расстояния от кончика глобулы. Обратите внимание, что радиальное положение, в котором напряжение становится отрицательным, совпадает с максимальной плотностью тока для последующего временного шага, показанного в части a.На вставке в увеличенном масштабе показаны напряжения около нуля МПа. На этом графике очевидны отрицательные или растягивающие напряжения. c Параболическая подгонка к глобуле лития, используемая для моделирования напряжения в блок-сополимерном электролите (линии) и соответствующих данных о толщине электролита на рентгеновских томограммах (маркеры).
Вертикальная составляющая вектора напряжения на границе раздела литий-полимер представлена как функция радиального положения на рисунке 7b. Напряжение на границе раздела существенно увеличилось по мере того, как глобула значительно выросла в высоту.Эти напряжения в электролите ослабляются по мере расширения глобулы на промежуточных и поздних стадиях роста. На более поздних стадиях напряжение на границе раздела достигло максимума в радиальном положении 6 мкм. Это происходит из-за делокализации максимума напряжения от наконечника, как описано выше. На рис. 7с показано усредненное в радиальном направлении расстояние между электродами, извлеченное из рентгеновских микротомографических изображений, и соответствующие параболические фитинги, используемые для моделирования напряжений в полимере. На рисунке 7b напряжение опускается ниже нуля в радиальных положениях, которые совпадают с краем глобулы, как показано на рисунке 7c.Кроме того, радиальные положения, которые имеют пиковую плотность тока, показанную на рисунке 7a, совпадают с радиальными положениями, которые показывают отрицательные или растягивающие напряжения на рисунке 7b. На последней стадии роста глобулы пройденный заряд равен 54,72 Кл / см 2 , напряжения по периметру глобулы были сжимающими и соответствующего пика плотности тока больше не было (рис. 7а).
Основываясь на теории, разработанной Ньюманом и Монро, можно было бы ожидать, что кинетика осаждения лития будет замедляться в областях напряжения сжатия и ускоряться в областях напряжения растяжения. 37 Мы видим, что глобула расширяется, поскольку литий преимущественно осаждается по периметру глобулы. По мере того как глобула продолжает расти, напряжения на кончике глобулы немного ослабляются, вероятно, из-за уплощения кончика глобулы. Важно отметить, что можно было ожидать, что геометрический эффект концентрации тока на кончике глобулы будет уменьшаться по мере того, как кончик глобулы уплощается. 30
На рисунке 8a мы построили график зависимости локальной плотности тока от местного напряжения. Плотность тока не показывает сильной зависимости от напряжения на этом графике.На ранних стадиях, как и ожидалось, плотность тока уменьшается с увеличением напряжения. Однако на более поздних стадиях роста плотность тока, по-видимому, увеличивается с увеличением напряжения. Важным параметром, который следует учитывать в этом случае, является радиус кривизны растущей глобулы. Глобула расширяется по мере роста, уменьшая движущую силу для роста глобулы, поскольку ток имеет тенденцию концентрироваться в областях с малым радиусом кривизны. Следовательно, важно нормализовать плотность тока для этого изменяющегося радиуса кривизны литиевого электрода.Плотность заряда C на поверхности проводника, как известно, приблизительно пропорциональна четвертому корню из гауссовой кривизны, K , поверхности в электростатической системе. 39,40
Увеличить Уменьшить Сбросить размер изображения
Рис. 8. a Плотность тока не коррелирует напрямую с напряжением на границе раздела литий-полимер. b Радиус кривизны металлического лития на глобуле показан как функция расстояния от кончика глобулы.Он минимален на кончике глобулы и увеличивается с увеличением радиального положения. c Нормализованная плотность тока в заданном радиальном положении отображается в зависимости от соответствующего напряжения в этом положении. d Нормированная плотность тока как функция энергии деформации в заданном радиальном положении.
Кривизна по Гауссу для сферы равна:
, где R — радиус сферы или радиус кривизны. Следовательно, в простейшей модели можно было бы ожидать, что локальная плотность тока в данном радиальном положении, i r , будет пропорциональна плотности заряда, или
, где R r — радиус кривизны в радиальном положении r .Кроме того, можно было бы ожидать, что плотность тока будет обратно пропорциональна расстоянию между электродами, t p , из-за омических потерь. Чтобы учесть эти факторы, мы нормируем локальную плотность тока следующим образом:
Мы предположили, что плотность заряда на поверхности электрода в нашей динамической системе аналогична плотности заряда в электростатической системе. В случае симметричного литий-полимерного элемента электроны движутся через металлический литий значительно быстрее, чем скорость, с которой ионы лития переносятся к поверхности электрода, из-за большого несоответствия электронной проводимости Li (10 7 См / см) и ионной проводимости электролита (10 −4 См / см).Поэтому разумно предположить, что распределение электронов в литиевом электроде определяется электростатикой. В электростатических системах электронный заряд имеет тенденцию концентрироваться на острых краях или областях с малым радиусом кривизны на электронно проводящих материалах в электрическом поле. 39–41 Поскольку плотность тока, используемая в этом исследовании, намного ниже предельного тока ( i L = 12 мА / см 2 ), более высокая концентрация электронов должна привести к увеличению скорости восстановления ионов лития. на кончике глобулы.
Радиус кривизны рассчитывается по параболической подгонке к границе раздела литий-полимер. На рисунке 8b показан радиус кривизны как функция радиального положения. Нормализованная плотность тока показана как функция напряжения на четырех различных стадиях роста глобулы на рисунке 8c. Во всех случаях нормализованная плотность тока уменьшалась по мере увеличения напряжения, что означает, что измеренная плотность тока была ниже, чем геометрические эффекты могли учесть в областях с высоким локальным напряжением.Это согласуется с теорией, которая предполагает, что сжимающие напряжения на границе раздела литий-полимер должны замедлять кинетику осаждения лития. Плотность энергии деформации определяется как:
где σ — напряжение, а — деформация. На рис. 8г показана нормализованная плотность тока как функция плотности энергии деформации. Плотность энергии деформации в электролите, по сути, является величиной, которая, как можно было бы ожидать, повлияет на плотность тока. Если плотность энергии деформации высока, существует большой энергетический штраф за восстановление иона лития в этом месте.Нормализованная плотность тока быстро уменьшалась по мере увеличения плотности энергии деформации, а затем выходила на плато при плотности энергии деформации около 1 пДж / мкм 3 .
Таким образом, существует несколько эффектов компаундирования, которые влияют на кинетику осаждения лития на растущую глобулу лития в мембране из твердого полимерного электролита. Во-первых, по мере увеличения модуля электролита увеличивается энергетический штраф за электроосаждение лития на кончике глобулы. Кроме того, существует энергетическая движущая сила для осаждения по периметру глобулы.Комбинация этих эффектов приводит к расширению глобулы лития, что, следовательно, снижает эффект концентрации тока на кончике глобулы.
Рост глобул лития через блок-сополимерный электролит полистирол — b — поли (этиленоксид) контролировали в симметричной литий — полимер — литиевой ячейке с помощью жесткой рентгеновской микротомографии. Изменение высоты глобулы, объема и площади проекции измеряли в зависимости от количества лития, осажденного в области, локальной для растущей глобулы.Локальная плотность тока была нанесена на карту вблизи растущей глобулы путем измерения количества заряда, нанесенного в каждом месте, в зависимости от времени заряда. Карты плотности тока подчеркивают делокализацию плотности тока от вершины глобулы на ранних стадиях роста к периметру глобулы. На поздних стадиях роста глобула значительно расширилась, что привело к минимальной концентрации тока на глобуле лития.
Профили напряжений в мембране из полимерного электролита были рассчитаны на основе деформации полимера из-за образования глобул и модуля полимера на основе ранее опубликованных реологических измерений. 13 Профили напряжения показали область напряжения сжатия на вершине глобулы и напряжения растяжения на периметре глобулы. Учитывая этот профиль напряжения, можно было бы ожидать замедленной кинетики осаждения на вершине глобулы и более быстрого осаждения по периметру. Это согласуется с экспериментальными картами плотности тока. Кроме того, по мере расширения глобулы можно было ожидать уменьшения геометрического эффекта концентрации тока, вызванного кривизной растущей глобулы. Это также согласуется с минимальной концентрацией тока, показанной на картах плотности тока на поздних стадиях.Следовательно, по мере того, как глобулы лития росли в жесткую мембрану из полимерного электролита, напряжения в электролите не только подавляли вертикальный рост глобулы за счет замедления кинетики осаждения на вершине, но также приводили к делокализации тока по периметру глобулы и последующему расширению глобулы. дальнейшее замедление его роста в вертикальном направлении.
Список символов
| a | Площадь пикселя (см 2 ) |
| А | Изменение объема электролита в контрольном объеме (м 3 ) |
| С | Плотность заряда |
| E | Модуль Юнга (Па) |
| Ф | постоянная Фарадея (Кл / моль) |
| Ф | Градиент деформации |
| I | Тензор идентичности |
| i jk | Плотность тока в пикселе j, k (мА / см 2 ) |
| i L | Предельный ток (мА / см 2 ) |
| i норма | Нормализованная плотность тока (мА / см 2 * мкм 3/2 ) |
| i r | Плотность тока в радиальном положении r (мА / см 2 ) |
| К | гауссова кривизна |
| M Li | Молекулярная масса металлического лития (г / моль) |
| r | Радиальное положение (мкм) |
| R | Исходное радиальное положение (мкм) |
| R | Радиус закругления |
| R R | Радиус кривизны в радиальном положении r |
| т | Время (с) |
| т Li | Толщина нанесенного лития (мкм) |
| т пол | Расстояние между литиевыми электродами (мкм) |
| U | Плотность энергии деформации (пДж / мкм 3 ) |
| V г | Объем глобулы лития (мкм 3 ) |
| V jk | Объем лития, нанесенного на пиксель j, k (см 3 ) |
Греческий
| Штамм | |
| ν | Коэффициент Пуассона |
| ρ | Плотность металлического лития (г / см 3 ) |
| σ | Напряжение (МПа) |
| σ | Тензор напряжений Коши |
Первичное финансирование работы было предоставлено Программой электронной микроскопии мягкого вещества Управления науки, Управления фундаментальных энергетических наук, материаловедения и инженерного отдела США.S. Министерство энергетики по контракту № DE-AC02-05Ch21231 (KC11BN). Эксперименты с жесткой рентгеновской микротомографией проводились в усовершенствованном источнике света, который поддерживается директором отдела науки Управления фундаментальных энергетических наук Министерства энергетики США по контракту № DE-AC02-05Ch21231. Кэтрин Дж. Гарри была поддержана исследовательской стипендией Национального научного фонда. Венката Сринивасана и Кеннета Хига поддержал помощник секретаря по энергоэффективности и возобновляемым источникам энергии Управления автомобильных технологий США.S. Министерство энергетики по контракту № DE-AC02-05Ch21231 в рамках Программы перспективных исследований аккумуляторных материалов (BMR). Мы также хотели бы поблагодарить профессора Брайана МакКлоски и профессора Джона Ньюмана за полезные технические обсуждения и советы.
Дорожная карта для передовых водных аккумуляторов: от дизайна материалов до приложений
Zn-основанные AB (ZnAB), первая электрохимическая батарея, восходящая к гальванической батарее, изобретенной А. Вольта в конце 19 века.С тех пор из-за очень хорошей электрохимической обратимости цинка были разработаны десятки батарей на основе цинка. В настоящее время одна треть мирового рынка аккумуляторов состоит из аккумуляторов на основе цинка, что подчеркивает их важность как источника питания для широкого спектра применений. На основе катода и электролита ZnAB можно разделить на щелочные цинковые батареи (AZAB; такие как Zn-Ni, щелочной Zn-MnO 2 , Zn-Ag и Zn-воздух), почти нейтральные Zn-ионные батареи. батареи (NZIB; такие как Zn-MnO 2 и Zn-V 2 O 5 ZIB и электролитический Zn-Mn аккумулятор) и проточные окислительно-восстановительные батареи на основе цинка (такие как Zn-Br, Zn-V, Zn-Ce и Zn-I).В последние годы были достигнуты некоторые прорывы в области водных аккумуляторов на основе цинка (см. Рис. 4A). Данные о зависимости удельной емкости от рабочего напряжения для различных типов батарей показаны на фиг. 4B в зависимости от массы катода.
Щелочные АКБ на основе цинка . Щелочные батареи на основе Zn, включая Zn-Ni / Co, Zn-MnO 2 , Zn-Ag 2 O и Zn-воздушные батареи, которые зависят от обратимой окислительно-восстановительной реакции Zn / ZnO с окислительно-восстановительным потенциалом −1,35 В по сравнению с SHE, представляют собой старую и зрелую технологию аккумуляторов, но в последнее время они привлекают к себе большое внимание.Это в основном вызвано слабой стабильностью, возникающей из-за неизбежного образования дендрита Zn, изменения формы, коррозии и пассивации. Для решения вышеуказанных проблем используются различные стратегии ( 23 ), включая легирование другими металлами (например, Bi, Sn и In) для подавления коррозии, гибридизации или модификации поверхности с помощью добавок [таких как BaO, Bi 2 O 3 и In (OH) 3 и Ca (OH) 2 ], чтобы подавить эволюцию H 2 , геометрию и конструкцию структуры (например, Zn-волокна, стержни, стержни и листы различной толщины и длины) для смягчения изменения формы и образования дендритов цинка, а также добавок к электролитам (таких как KF, K 2 HPO 4 , K 2 CO 3 , полиэтиленгликоль и насыщенный ZnO) для уменьшения растворения Zn и ингибирования дендрита Zn были использованы.В 2017 году Ролисон и его коллеги ( 52 ) исследовали 3D-губки из цинка в качестве анодных материалов при высокой DoD (DoD Zn ). Как показано на рис. 4C, благодаря монолитной, пористой и непериодической архитектуре Zn-губок такой 3D Zn-анод обеспечивает высокое использование 91% DoD Zn и не содержит дендритов с повторяющимися 50000 циклов при <1% DoD Zn. . Вдохновленный этим случаем, были разработаны различные долговечные аноды из цинка, основанные на стратегии построения трехмерного каркаса (такие как нанопроволока из никеля, углеродная ткань, пена Cu и пена графен).Кроме того, квазитвердотельная конструкция не только наделяет батареи высокой гибкостью, но и стабилизирует Zn-анод, подавляя коррозию и растворение Zn-анода.
Для катодных материалов MnO 2 как нетоксичный, недорогой, землистый и высокоемкий (617 мАч г −1 ) материал является многообещающим кандидатом для AZAB. В щелочных батареях Zn-Mn побочные продукты спинномозговой фазы Mn 3 O 4 (образованные Mn 2+ и материнским MnO 2 ) и ZnMn 2 O 4 [образованные MnOOH и Zn (OH) 4 2-] накапливаются после повторяющихся циклов при глубокой DoD, что приводит к уменьшению емкости и возможному выходу из строя батареи.В общем, легирование элементами Bi, Cu, Ni, Co и т. Д. Или объединение соответствующих оксидов с катодом и использование электролита LiOH является эффективным методом увеличения емкости и перезаряжаемости MnO 2 ( 23 ). В 2017 году Банерджи и его сотрудники ( 74 ) реализовали двухэлектронное использование (617 мАч г -1 ) MnO 2 с 6000 циклами жизни с использованием катода из би-бирнессита с интеркалированной медью. Как показано на рис. 4D, ключ к перезаряжаемости основан на окислительно-восстановительных потенциалах Cu для обратимого внедрения в слоистую структуру би-бирнессита во время процесса растворения и осаждения для стабилизации и улучшения характеристик переноса заряда.Такие стратегии электрохимической настройки беспрецедентно решают основные проблемы использования катода MnO 2 в щелочных батареях, демонстрируя глубокое использование с высокой стабильностью.
Катодные материалы на основе Ni / Co из-за их превосходной электрохимической обратимости и приемлемой теоретической емкости широко используются для изготовления Zn-Ni аккумуляторов с конца 19 века. Среди различных АКБ Zn-Ni / Co батареи особенно выгодны из-за их уникальных достоинств более высокого рабочего напряжения (около 1.От 7 до 1,8 В; см. рис. 4B), впечатляющую теоретическую плотность энергии (~ 372 Вт · ч · кг -1 ), высокую мощность и низкую стоимость. Однако из-за низкого срока службы цинкового анода по прошествии более 100 лет Zn-Ni батареи продавались компанией PowerGenix (теперь называемой ZincFive Inc.) до 2003 года. В целом, коммерческие Zn-Ni батареи, изготовленные из β-фазы Ni. Катод (OH) 2 обеспечивает плотность энергии от 70 до 100 Вт · ч · кг -1 , пиковую плотность мощности 2000 Вт · кг -1 и срок службы около 500 циклов.Общие электрохимические характеристики далеко не удовлетворительны для постоянно растущего спроса на накопители энергии. Помимо плохой стабильности цинкового анода, исследователи склонны объяснять такие плохие электрохимические характеристики реактивной удельной емкостью, необратимостью и низкой электроактивностью катода на основе Ni / Co. К счастью, некоторые достижения в разработке катодных материалов на основе Ni / Co с наноархитектурой в последние годы вселили надежды. В 2014 году Дай и его сотрудники ( 75 ) представили сверхбыструю Zn-Ni-батарею высокой емкости на основе ультратонких слоистых нанопластинчатого катода из двух гидроксидов / углеродных нанотрубок (LDH / CNT) со слоями NiAlCo, в которых стабилизировалось совместное легирование Al и Co. α-Ni (OH) 2 .Благодаря высокой емкости (354 мА · ч · г −1 ), высокому расходу (278 мА · ч · г −1 при 66,7 A · г −1 ) и хорошей стабильности (сохранение емкости 94% после 2000 циклов) Катод NiAlCo LDH / CNT, собранная Zn-Ni батарея обеспечивает плотность энергии 274 Вт · ч · кг −1 и удельную мощность 16,6 кВт · кг −1 вместе с хорошей стабильностью при циклическом изменении (сохранение емкости 85% после 500 циклов). ). До сих пор вдохновленные этой работой, различные материалы на основе Ni и Co, такие как NiAlCo-LDH / CNT ( 75 ), Ni 3 S 2 ( 76 ), Co 3 O 4 ( 77 ) и NiCo 2 O 4 ( 78 ), были тщательно исследованы для Zn-Ni аккумуляторов.
Помимо оптимизации состава, рациональный дизайн наноархитектуры (например, наночастиц, нанопроволок, наностержней и нанолистов) может обеспечить уникальные преимущества в механических и электрических свойствах, таких как большая площадь поверхности и более короткие пути для переноса ионов и электронов, преодолевать присущие объемным материалам проблемы, такие как плохая электропроводность и большое объемное расширение. Кроме того, модификация поверхности, такая как покрытие поверхности PANI и легирование поверхности фосфат-ионами, может дополнительно повысить электрическую проводимость электродов ( 76 , 78 ).Однако следует отметить, что разработанные усовершенствованные автономные катоды все еще далеки от практического применения, хотя они достигли замечательной гравиметрической емкости, высокой скорости и длительного срока службы. Их емкость обычно ниже, чем 1,0 мАч см -2 , что намного ниже емкости промышленного уровня ∼35 мАч см -2 ( 79 ). Поэтому дальнейшее развитие материалов на основе Ni и Co для Ni-Zn или Co-Zn аккумуляторов, которые одновременно обладают высокой гравиметрической емкостью, высокими скоростными характеристиками и длительным сроком службы при большой массовой нагрузке, остается труднодостижимым.
Нейтральные ЗИБ . NZIB, в которых в качестве электролита используются нейтральные или слабокислые водные среды, содержащие Zn 2+ , в последние годы привлекают все большее внимание мировой общественности из-за их потенциала для крупномасштабного накопления электроэнергии. Еще в 1986 г. Ямамото и др. Впервые исследовали перезаряжаемую батарею Zn-MnO 2 с катодом из MnO 2 и анодом из Zn в электролите 2 M ZnSO 4 . ( 80 ), но механизм реакции был неясен.До 2012 года Канг и его сотрудники ( 81 ) обнаружили обратимое интеркалирование Zn 2+ в α-MnO 2 и предложили концепцию объединения NZIB с цинковым анодом и мягким ZnSO 4 или Zn. (NO 3 ) 2 водный электролит. С тех пор интенсивные усилия были посвящены NZIB с целью раскрытия механизма реакции и разработки современных электродных материалов. В отличие от AZAB, накопление заряда в аноде зависит от обратимого покрытия / удаления Zn / Zn 2+ с окислительно-восстановительным потенциалом -0.763 В против ОНА. Хотя сильная коррозия и растворение Zn устранены, самые большие проблемы заключаются в подавлении образования дендрита цинка. До сих пор были изучены различные меры, включая модификацию поверхности, структурную оптимизацию ( 37 ) и оптимизацию электролита ( 47 ) , чтобы исключить образование дендрита цинка. Например, высокоскоростной гибкий квазитвердотельный ZIB, сконструированный из анода с массивом Zn, поддерживаемого графеновой пеной, и гелевого электролита может обеспечить долговечность в 2000 циклов при 89% начальной емкости ( 37 ).Более того, недавно Арчер и его коллеги ( 82 ) указали, что графен с низким рассогласованием кристаллической решетки для Zn эффективен при осаждении Zn с заблокированной кристаллографической ориентацией, что обеспечивает исключительную обратимость Zn анод.
Другой проблемой, которая препятствует применению NZIB, является отсутствие прочных катодных материалов-хозяев для быстрого и обратимого хранения Zn 2+ из-за высокой плотности заряда и большого гидратированного ионного радиуса Zn 2+ .До сих пор, хотя были предложены различные катодные материалы, такие как оксиды марганца, V на основе, PBA и органические материалы ( 14 ), разработка катодных материалов для ZIB все еще находится на начальной стадии. Это в основном объясняется следующими четырьмя аспектами: (i) механизм реакции все еще остается спорным, (ii) быстрое снижение производительности, (iii) неудовлетворительная удельная производительность и (iv) низкая производительность. Соединения на основе V, особенно оксиды ванадия, являются привлекательными материалами-хозяевами для хранения Zn 2+ .Из-за присущих им свойств множественных валентных состояний ванадия и большой структуры открытого каркаса материалы на основе V обладают достоинствами высокой емкости (даже до 400 мАч g -1 ), быстрой динамикой и низкой стоимостью. Что касается механизма реакции, его обычно рассматривают как введение / извлечение Zn 2+ в исходные материалы во время соответствующего процесса разряда / заряда. Недавно, при наблюдении сульфата гидроксида цинка [Zn 4 (SO 4 ) (OH) 6 · nH 2 O, ZHS] в системах Zn-V, H + также рассматривается как носитель заряда для участия в электрохимической реакции ( 83 ).На основе одновременного процесса введения / извлечения H + и Zn 2+ , батарея Zn / NaV 3 O 8 · 1,5H 2 O предложена Ченом и его коллегами ( 51 ) обеспечивает превосходную обратимую емкость (380 мАч g −1 ) и высокую долговечность (сохранение емкости 82% после 1000 циклов). Помимо изучения механизма, необходимы дополнительные работы по усовершенствованным материалам для улучшения удельной емкости, скоростных характеристик и продолжительности цикла V-образного катода.До сих пор некоторые стратегии оптимизации, включая морфологический и структурный контроль (например, проектирование различных наноархитектур; предварительное введение Li, Na, K, Zn, Ca и т. Д., Ионов металлов; и корректировка структурной воды), интеграция с проводящими добавками, были предприняты попытки разработки электродов без связующего и оптимизации электролитов ( 83 ). Десятки соединений на основе V, таких как V 2 O 5 · nH 2 O ( 84 ), Zn 0,25 V 2 O 5 · nH 2 O ( 85 ) и Zn 2 (OH) VO 4 ( 37 ).В общем, оксиды на основе V могут иметь сверхвысокую разрядную емкость, превышающую 400 мАч г -1 , в то время как их рабочее напряжение относительно ниже, чем у материалов на основе Mn (рис. 4B). Например, батарея Zn / Zn 0,3 V 2 O 5 · 1,5H 2 O, изготовленная Wang et al. ( 86 ) обеспечивает среднее напряжение разряда 0,8 В и высокую удельную емкость 426 мАч g −1 при 0,2 A g −1 вместе с беспрецедентной стабильностью цикла (поддерживает 214 мАч g — 1 после 20000 циклов при 10 А г −1 ).
PBA, как и системы LiAB, NaAB и KAB, также могут использоваться в качестве катодных материалов для NZIB. В 2015 году Лю и его коллеги впервые предложили NZIB на основе PBA, построенный на ZnHCF ( 87 ), с относительно высоким рабочим напряжением ~ 1,7 В, разрядной емкостью ~ 65,4 мА · ч g -1 и плотность энергии 100 Вт · ч кг -1 . С тех пор различные другие NZIB на основе PBA, такие как CuHCF-Zn (56 мАч г -1 , 1,73 В), FeHCF-Zn (120 мАч г -1 , 1.1 В), NiHCF-Zn (56 мАч, -1 , 1,2 В) и MnHCF-Zn (137 мАч, -1 , 1,7 В) ( 14 ). Однако обратите внимание, что из-за низкой емкости плотность энергии NZIB на основе PBA все еще неконкурентоспособна. Помимо неорганических материалов, упомянутых выше, некоторые органические, такие как ПАНИ (191 мАч г -1 , 1,0 В) ( 88 ) и каликс [4] хинон (335 мАч г -1 , 1,0 В) ( 89 ), были разработаны. До сих пор разработка органических катодных материалов для NZIB все еще находится на начальной стадии.Благодаря широкому выбору функциональных групп и молекулярной массы остается огромный потенциал для оптимизации электрохимических характеристик органических электродов.
Оксиды марганца, с достоинствами обильных кристаллографических полиморфов (α, β, γ, δ, λ, ε и типы тодорокита), высокой теоретической емкостью (308 мАч г -1 ), низкой стоимостью и обилием земли , были расценены как многообещающие кандидаты в катод для NZIB. В целом, при соответствующем исследовании различных полиморфов MnO 2 для NZIB, в основном существуют четырехпоточные концепции, как показано на рис.4E о механизме накопления энергии: (i) введение / извлечение Zn 2+ , (ii) введение / извлечение H + , сопровождаемое осаждением ZHS, (iii) совместное введение / извлечение как H + , так и Zn 2+ на различных этапах заряда / разряда и (iv) электролиз / электроосаждение MnO 2 / Mn 2+ , которые систематически обобщались в отчетах ( 14 , 41 ).
Хотя механизм реакции остается спорным, первые три механизма предполагают, что сильное растворение Mn 2+ в процессе разряда ответственно за быстрое падение емкости.До сих пор использовались некоторые эффективные стратегии, включая предварительное добавление соли Mn в электролит ( 50 ), покрытие поверхности [например, легированный азотом углерод ( 90 ) и PEDOT ( 91 )] и включение тесно связанных ионов [например, K 0,8 Mn 8 O 16 ( 92 )], были использованы для подавления растворения Mn 2+ и повышения устойчивости NZIB к циклированию. В частности, устойчивость батареи Zn-MnO 2 к циклическому режиму может быть значительно улучшена за счет предварительного добавления Mn 2+ , что обеспечивает срок службы в 10 000 циклов без очевидного снижения емкости ( 93 ).Следует отметить, что такая превосходная циклическая стабильность объясняется не только стабилизированным MnO 2 за счет подавления растворения Mn 2+ , но и дополнительной емкостью, обеспечиваемой повторно нанесенным MnO 2 в процессе загрузки ( 94 ). Кроме того, большое изменение объема и структурный коллапс, вызванные повторным введением гидратированных ионов Zn 2+ , также приводят к быстрому ослаблению емкости. Таким образом, были исследованы различные усилия, такие как морфологический контроль пористой структуры ( 90 ), связывание с графеном и УНТ ( 95 ) и стабилизация структуры катионным легированием и интеркаляцией PANI ( 96 ).Например, нанослой MnO 2 , интеркалированный PANI, может обеспечивать стабильную разрядную емкость около 125 мАч g -1 в течение 5000 циклов ( 96 ).
Хотя был достигнут большой прогресс, как видно из рис. 4A, текущие щелочные батареи на основе Zn и нейтральные или слабокислые батареи Zn 2+ показали ограниченное выходное напряжение (<1,8 В) и разрядную емкость ниже 450 мАч г −1 . В наших последних исследованиях мы обнаружили скрытый высоковольтный процесс электролиза MnO 2 в обычном ZIB и предложили ранее неизвестную электролитическую систему Zn-Mn (см.рис.4F) через активную протонную и электронную динамику ( 41 ). Четырехступенчатый процесс электролиза MnO 2 был впервые проанализирован расчетами по теории функционала плотности. Эта Zn-Mn электролитическая система обеспечивает выходное напряжение до 1,95 В, внушительную гравиметрическую емкость около 570 мА · ч · г -1 и плотность ~ 409 Вт · ч · кг -1 на основе как анодных, так и катодных активных материалов. Опытный образец проточной окислительно-восстановительной батареи был также построен в нашей электролитической батарее Zn-Mn.Таким образом, выходное напряжение (~ 2 В), энергоэффективность (88%) и стоимость электролита [от 3 до 5 долларов США (кВт · ч) -1 ] превосходят другие системы с окислительно-восстановительными парами, интегрированные в AB-системы (рис. 4G). ), такие как Zn-Fe, Zn-Br 2 , Zn-Ce и все ванадиевые проточные батареи ( 41 ). Ожидается, что с дальнейшими судебными разработками, такими как использование более селективного электролита, повышение эффективности Zn и эффективная конструкция проточной батареи, эта конструкция Zn-Mn электролитической проточной батареи будет применима для практического хранения энергии и, в частности, для крупномасштабного сетевого хранения энергии.
Анализ потерь напряжения в проточной батарее с кислотным окислительно-восстановительным потенциалом хинона (Журнальная статья)
Чен, Цин, Герхард, Майкл Р. и Азиз, Майкл Дж. Анализ потерь напряжения в проточной кислотно-восстановительной батарее с хиноном . США: Н. П., 2017.
Интернет. DOI: 10.1149 / 2.0721706jes.
Чен, Цин, Герхард, Майкл Р., & Азиз, Майкл Дж. Анализ потерь напряжения в проточной батарее с кислотным окислительно-восстановительным потенциалом хинона . Соединенные Штаты. https://doi.org/10.1149/2.0721706jes
Чен, Цин, Герхард, Майкл Р. и Азиз, Майкл Дж. Ту.
"Рассмотрение потерь напряжения проточной батареи кислотного окислительно-восстановительного потенциала хинона". Соединенные Штаты. https://doi.org/10.1149/2.0721706jes. https: // www.osti.gov/servlets/purl/1422403.
@article {osti_1422403,
title = {Анализ потерь напряжения проточной батареи кислотного окислительно-восстановительного потенциала хинона},
author = {Чен, Цин и Герхардт, Майкл Р. и Азиз, Майкл Дж.},
abstractNote = {Мы измеряем поляризационные характеристики проточной батареи хинон-бромидного окислительно-восстановительного потенциала с встречно-штыревыми полями потока, используя спектроскопию электрохимического импеданса и вольтамперометрию полной ячейки и полуэлемента относительно электрода сравнения.Мы обнаружили линейную поляризацию при 50% -ном состоянии заряда вплоть до плотности тока короткого замыкания 2,5 А / см2. Мы однозначно идентифицируем удельное сопротивление поляризации (ASR) каждого электрода, ASR мембраны к ионному току и ASR электронного контакта. Мы используем датчики напряжения, чтобы определить плотность электронного тока через каждый лист копировальной бумаги в хиноносодержащем электроде. Также интерпретируя результаты с использованием одномерной модели пористого электрода Ньюмана, мы вычисляем объемную плотность тока обмена пористого электрода.Мы однозначно оцениваем рассеиваемую мощность и определяем соответствие вкладов в ASR электрода от фарадеевских, электронных и ионных процессов переноса. Мы обнаружили, что внутри электрода в фарадеевском процессе рассеивается больше энергии, чем в процессах электронной и ионной проводимости вместе взятых, несмотря на наблюдаемое поведение линейной поляризации. Мы исследуем чувствительность ASR к значениям параметров модели. Наибольшее улучшение характеристик ожидается за счет увеличения объемной плотности тока обмена.},
doi = {10.1149 / 2.0721706jes},
url = {https://www.osti.gov/biblio/1422403},
journal = {Journal of the Electrochemical Society},
issn = {0013-4651},
число = 6,
объем = 164,
place = {United States},
год = {2017},
месяц = {3}
}
Понимание ограничивающих факторов производительности толстых электродов применительно к литий-ионным батареям с высокой плотностью энергии
Yoshino A (2012) Рождение литий-ионной батареи. Angew Chem Int Ed 51: 5798
CAS Статья Google Scholar
Yoshino A, Sanechika K, Nakajima T (1985) Вторичный аккумулятор. Патент США 4668595
Delmas C, Saadoune I (1992) Электрохимические и физические свойства фаз Li x Ni 1 – y Co y O 2 фаз. Ионика твердого тела 53–56: 370
Статья Google Scholar
Guilmard M, Croguennec L, Delmas C (2003) Термическая стабильность производных оксида лития-никеля. Часть II: Li x Ni 0,70 Co 0,15 Al 0,15 O 2 и Li x Ni 0,90 Mn 0,10 O 2 (x = 0,50 и 0,30). Сравнение с Li x Ni 1,02 O 2 и Li x Ni 0,89 Al 0,16 O 2 . Chem Mater 15: 4484
CAS Статья Google Scholar
Lu Z, Dahn JR (2005) Катодные композиции для литий-ионных аккумуляторов. Патент США 6964828
Рохан Дж. Ф., Хасан М., Патил С., Кейси Д. П., Клэнси Т. (2014) Накопление энергии: материалы и архитектура батарей на наноуровне. В: Fagas G (ed) Концепции ИКТ-энергии к информационным и коммуникационным технологиям с нулевым энергопотреблением. InTech. DOI: 10,5772 / 57139. ISBN: 978-953-51-1218-1
Моштев Р. (2000) Современное состояние коммерческих литий-ионных аккумуляторов. Источники питания J 91:86
CAS Статья Google Scholar
Обровац М.Н. (2015) Новый химический состав металло-ионных аккумуляторов. Семинар по энергетике, передовым материалам и устойчивости 29 мая, стр. 2015, Галифакс, NS Канада
Yu DYW, Donoue K, Inoue T., Fujimoto M, Fujitani S (2006) Влияние параметров электрода на LiFePO 4 катоды. J Electrochem Soc 153: A835
CAS Статья Google Scholar
Tran HY, Greco G, Taeubert C, Wohlfahrt-Mehrens M, Haselrieder W, Kwade A (2012) Влияние подготовки электродов на электрохимические характеристики LiNi 0.8 Co 0,15 Al 0,05 O 2 композитных электрода для литий-ионных аккумуляторов. J Источники питания 210: 276
CAS Статья Google Scholar
Лу В., Янсен А., Дис Д., Нельсон П., Веселка Н. Р., Хенриксен Г. (2011) Исследование высокоэнергетических электродов для подключаемых гибридных электромобилей. J Источники питания 196: 1537
CAS Статья Google Scholar
Zheng H, Li J, Song X, Liu G, Battaglia VS (2012) Исчерпывающее понимание влияния толщины электродов на электрохимические характеристики катодов литий-ионных аккумуляторов. Электрохим Акта 71: 258
CAS Статья Google Scholar
Дойл М., Фуллер Т.Ф., Ньюман Дж. (1993) Моделирование гальваностатического заряда и разряда литиево-полимерного / вставляемого элемента. J Electrochem Soc 140: 1526
CAS Статья Google Scholar
Newman J, Thomas-Alyea KE (2004), Глава 22 пористые электроды. В кн .: Электрохимические системы, 3-е изд. Уайли, Хобокен
Google Scholar
Newman J (1995) Оптимизация пористости и толщины электрода батареи с помощью модели реакционной зоны. J Electrochem Soc 142: 97
CAS Статья Google Scholar
Сринивасан В., Ньюман Дж. (2004) Модель разряда для литиево-железо-фосфатного электрода.J Electrochem Soc 151: A1530
CAS Статья Google Scholar
Yu S, Kim S, Kim TY, Nam JH, Cho WI (2013) Прогнозирование модели и эксперименты по оптимизации конструкции электродов LiFePO 4 / графитовые электроды в литий-ионных батареях большой емкости. Bull Korean Chem Soc 34:79
CAS Статья Google Scholar
Gallagher KG, Trask SE, Bauer C, Woehrle T, Lux SF, Tschech M, Lamp P, Polzin BJ, Ha S, Long B, Wu Q, Lu W, Dees DW, Jansen AN (2016) Оптимизация емкости за счет понимания ограничений литий-ионных электродов.J Electrochem Soc 163: A138
CAS Статья Google Scholar
Фуллер Т.Ф., Дойл М., Ньюман Дж. (1994) Моделирование и оптимизация двойной ионно-литиевой ячейки. J Electrochem Soc 141: 1
CAS Статья Google Scholar
МакМуллин Р.Б., Муччини Г.А. (1956) Характеристики пористых пластов и структур. AIChE J 2: 393
CAS Статья Google Scholar
Landesfeind J, Hattendorff J, Ehrl A, Wall WA, Gasteiger HA (2016) Определение извилистости аккумуляторных электродов и сепараторов методом импедансной спектроскопии. J Electrochem Soc 163 (7): A1373
CAS Статья Google Scholar
Эбнер М., Вуд В. (2015) Инструмент для оценки извилистости пористых электродов литий-ионных аккумуляторов. J Electrochem Soc 162 (2): A3064
CAS Статья Google Scholar
Kehrwald D, Shearing PR, Brandon NP, Sinha PK, Harris SJ (2011) Локальные неоднородности извилистости в композитном электроде литиевой батареи. J Electrochem Soc 158 (12): A1393
CAS Статья Google Scholar
Dees D, Gunen E, Abraham D, Jansen A, Prakash J (2005) Электрохимическое моделирование импеданса переменного тока литий-ионных положительных электродов. J Electrochem Soc 152 (7): A1409
CAS Статья Google Scholar
Kumaresan K, Sikha G, White RE (2008) Тепловая модель литий-ионного элемента. J Electrochem Soc 155 (2): A164
CAS Статья Google Scholar
Valøen LO, Reimers JN (2005) Транспортные свойства электролитов литий-ионных аккумуляторов на основе LiPF6. J Electrochem Soc 152 (5): A882
Артикул Google Scholar
Lundgren H, Behm M, Lindbergh G (2015) Электрохимические характеристики и температурная зависимость масс-транспортных свойств LiPF6 в EC: DEC.J Electrochem Soc 162 (3): A413
CAS Статья Google Scholar
Klett M, Giesecke M, Nyman A, Hallberg F, Lindström RW, Lindbergh G, Furó I (2012) Количественная оценка массопереноса во время поляризации в электролите литий-ионной батареи с помощью визуализации 7Li ЯМР in situ. J Am Chem Soc 134 (36): 14654
CAS Статья Google Scholar
Gallagher KG, Goebel S, Greszler T., Mathias M, Oelerich W., Eroglu D, Srinivasan V (2014) Количественная оценка перспективности литий-воздушных батарей для электромобилей.Energy Environ Sci 7: 1555
CAS Статья Google Scholar
Атлунг С., Вест К., Якобсен Т. (1979) Динамические аспекты твердорастворных катодов для электрохимических источников энергии. J Electrochem Soc 126: 1311
CAS Статья Google Scholar
Wang M, Li J, He X, Wu H, Wan C (2012) Влияние локальной плотности тока на конструкцию электродов для литий-ионных батарей.J Источники питания 207: 127
CAS Статья Google Scholar
Valoen LO, Reimers JN (2005) Транспортные свойства литий-ионных аккумуляторных электролитов на основе LiPF 6 . J Electrochem Soc 152: A882
CAS Статья Google Scholar
Yamada Y, Furukawa K, Sodeyama K, Kikuchi K, Yaegashi M, Tateyama Y, Yamada A (2014) Необычная стабильность суперконцентрированных электролитов на основе ацетонитрила для быстрой зарядки литий-ионных аккумуляторов.J Am Chem Soc 136: 5039
CAS Статья Google Scholar
Yamada Y, Yaegashi M, Abe T, Yamada A (2013) Сверхконцентрированный эфирный электролит для быстрой зарядки литий-ионных аккумуляторов. Chem Commun 49: 11194
CAS Статья Google Scholar
Chiang YM, Hellweg B (2009) Структуры батарей с сетчатой и контролируемой пористостью. Патент США 7553584
Ramadesigan V, Methekar RN, Latinwo F, Braatz RD, Subramanian VR (2010) Оптимальное распределение пористости для минимизации омического падения на пористом электроде. J Electrochem Soc 157: A1328
CAS Статья Google Scholar


