Плотность электролита зимой и летом
Всем привет! С Вами аккумуляторщик. Сегодня я бы хотел развеять миф про плотность электролита зимой и летом. Многие люди, особенно старой «советской» закалки, которые приходят в магазин или просто приходят со своим аккумулятором и просят им сделать зимнюю или летнюю плотность. Сразу скажу, сейчас это уже не актуально.Сейчас во все аккумуляторные батареи, в частности для наших широт заливают электролит плотностью 1,27- 1,28 г/см3. И менять её не требуется, это запрещено вообще! Коррекцию электролита самостоятельно тоже нельзя делать ни в коем случае. Это может сделать только специалист по ремонту аккумуляторов, и то в крайнем случае, например, при восстановлении АКБ.
Если Вы измерите плотность на новом полностью заряженном аккумуляторе, то плотность в нем будет 1,27 ровно. Ничего подливать туда не надо! Дело в том, что многие люди думают что на зиму надо сделать поядрёнее такой покрепче электролит. На самом деле, этого не требуется. При плотности 1,27 г/см
Слишком большая плотность делает среду чрезмерно агрессивной. И соответственно, идет быстрее осыпания пластин аккумулятора. Потому что аккумуляторная батарея на автомобиле – это сбалансированное устройство, вмешиваться в его электролит значит выводить из баланса АКБ. Как некоторые делают по старинке: доливают дистиллированную воду на лето, а зимой доливают электролит. Ничего этого делать не нужно!
Лучше позаботьтесь о другом. Например, качественно зарядите аккумулятор перед холодами хорошим зарядным устройством. Для того, чтобы плотность выровнялась по банкам АКБ и вышла у Вас к номинальной 1,27- 1,28 г/см3. С такой плотностью электролита можно ездить и летом и зимой, так скажем всесезонный аккумулятор.
Вот поэтому никогда не проводите самостоятельно манипуляций с электролитом. Только корректируем уровень дистиллированной водой. То есть, подливая воду в банки до номинального уровня. Напомню, для легковых АКБ это полтора сантиметра над свинцовыми пластинами аккумулятора, для грузовых 2-3 см. Вот и все! Ну и соответственно, заряжаем для того, чтоб достигнуть рабочей плотности.
Надеюсь наши советы по эксплуатации автомобильного аккумулятора помогут Вам в жизни. Не совершайте ошибок.
Также на эту тему:
Таблица плотности электролита в аккумуляторе
Любой водитель иногда сталкивается с проблемой неожиданно севшей АКБ, однако, мало, кто знает, что причиной этого явления чаще всего является недостаточная плотность электролита.
Стоит отметить, что сразу же после приобретения новой батареи плотность субстанции до первой зарядки составляет не менее, чем то, которое установил производитель для конкретной климатической полосы в стране.
Необходимо обращать внимание на этот показатель, поскольку плотность напрямую зависит от определенной температуры, как и моторное масло.
Узнай время зарядки своего аккумулятора
Так АКБ, плотность электролита которой высока, легко эксплуатируется при самых сильных морозах, что позволяет сохранить нормальный заряд и уверенный запуск мотора.
При этом, если плотность субстанции в аккумуляторе низкая, то применять ее в холодном климате не представится возможным, поскольку это грозит:
- плохой запуск в условиях морозной зимы;
- стабильным недозарядом АКБ, что понижает срок ее эксплуатации.
Как правильно замерить плотность электролита
Замер плотности электролита
Стоит понять, что в процессе использования аккумуляторной батареи меняется плотность и объем электролита, а эти параметры придется контролировать собственноручно. Для того, чтобы замерить плотность электролита аккумулятора следует:
- измерять ее только на 100% заряженной АКБ;
- нельзя снимать аккумулятор с авто или выключать зажигание;
- перед проверкой обязательно корректируется уровень электролита;
- добавить в электролит воду, чтобы его объем был нормальным;
- зарядка аккумулятора производится в течение всей ночи, но только небольшим током;
- после того, как термин зарядки окончился, АКБ следует отключить от зарядного устройства и оставить его для отдыха;
- после отстоя в шесть часов производят измерение плотности электролита, поскольку этот показатель будет самым точным;
- проверять плотность субстанции следует не реже, чем одного раза в три месяца, однако, исключительно с замерами выводного напряжения;
- для того, чтобы измерить плотность, стоит демонтировать, очистить и осмотреть АКБ;
- после этого взять прибор для измерения уровня электролита и полую трубочку из стекла;
- измерения проводятся только после установки аккумулятора на ровную поверхность и вывертывания его банок;
- полая трубка опускается одним концом в баночку, а второй кончик зажимается одним из пальцев, после чего прибор осматривается на уровень электролита (норма – 12 или 15 сантиметров).

Понять в норме ли плотность субстанции поможет только лишь таблица плотности электролита в аккумуляторе при различных температурах и степени зарядки, приведенная ниже.
| Степень зарядки | Темпера | тура |
| Выше 25 градусов | Ниже 25 градусов | |
| Зарядка на 100% | 1.210 – 1.230 | 1.270 -1.290 |
| Заряженная на 70% | 1.170 — 1.190 | 1.230 – 1.250 |
| Полностью разряженная | 1.050 – 1.070 | 1.110 – 1.130 |
Мифы о зимней и летней плотности электролита
Профессионалы указывают на то, что плотность электролита в аккумуляторе согласно таблице зимой и летом практически неизменна. Ни в одном автомобильном магазине человеку не продадут АКБ с электролитом для зимнего или летнего периода.
Электролит плотностью в 1.27 или 1.28
В наши дни практически во всех аккумуляторах для всех регионов России применяется электролит плотностью в 1.27 или 1.28 грамм на кубический сантиметр. Самостоятельно корректировку электролита проводить категорически запрещено, поскольку это может вывести из строя даже новую рабочую АКБ. Как правило, повысить плотность электролита в аккумуляторе зимой или летом смогут только специалисты по ремонту данного агрегата и то только при его восстановлении.
Таблица плотности электролита в аккумуляторе позволяет понять в рабочем ли состоянии находится АКБ или же реанимировать ее не получится. Согласно данным таблицы можно понять, что плотность электролита 1.27 не позволит субстанции замерзнуть, пока температура не опустится до шестидесяти градусов, что в условиях российской зимы маловероятно.
В том случае, если сильно повысить плотность электролита летом или зимой, среда станет невероятно агрессивной, а значит, мгновенно выходят из строя пластины АКБ. Категорически запрещено в том случае, если показатели слегка больше или меньше, указанных в таблице, доливать электролит зимой, а дистиллированную воду летом.
Как повысить плотность электролита в домашних условиях
Для того, чтобы нормализировать плотность электролита до данных, указанных в таблице, зачастую достаточно будет просто зарядить аккумуляторную батарею. При этом слишком уж повышенная плотность электролита негативно будет влиять на состояние АКБ.
Перед тем, как повышать уровень плотности электролита до нормального уровня зимой или летом следует проделать простые манипуляции, чтобы повышенная плотность не повысилась еще больше, как это показано на видео:
- приготовить таблицу значений для определенной АКБ при использовании ее в конкретном российском регионе;
- взять ареометр и выдавить из груши воздух;
- погрузить наконечник прибора в банку № 1 и набрать немного субстанции в него;
- пождать несколько секунд и приступить к оцениванию результата, понимая, что он будет одинаковым летом и в зимнюю пору года.
При этом повышенная плотность будет определяться красным цветом индикатора, нормальная – зеленым. Потом стоит проделать вышеуказанные процедуры со второй банкой аккумуляторной батареи автотранспортного средства, чтобы определить повышенная или нет плотность электролита в ней.
Если же автомобилист все-таки собрался повысить плотность электролита в АКБ, ему придется по старинке разбавлять его дистиллированной водой. Однако в целях соблюдения мер безопасности вода наливается в емкость, куда тонкой струйкой понемногу добавляется кислота. Иначе, может произойти взрыв, поэтому обязательно следует надевать очки и резиновые перчатки.
Таблица плотности электролита
Чтобы исключить повышенную плотность, после доливки смеси аккумуляторную батарею следует подзарядить в течение тридцати минут для перемешивания.
Проблемы с электролитом связаны с тем, что при работе аккумулятора, он нагревается, а дистиллированная вода из него быстро испаряется.
Стоит отметить, что для получения самых точных результатов прибор следует промывать не проточной, а дистиллированной водой сразу же после применения. Неисправный ареометр может привести к неправильным результатам, а манипуляции с ним приведут к поломке аккумулятора.
Когда после всех процедур плотность электролита АКБ не приходит в норму, то его следует поменять в определенном объеме, иначе аккумулятор попросту выйдет из строя окончательно.
Практически каждый автомобилист знает, насколько важно держать аккумуляторную батарею своего автомобиля в порядке. От ее состояния зависит не только возможность пуска двигателя, но и нормальная работа всего электрооборудования машины. К сожалению, далеко не всем известно, что исправность и «боеготовность» батареи зависит не только от своевременной и качественной ее зарядки, но и от нормальной плотности электролита в аккумуляторе.
Устройство и принцип работы АКБ
Для того чтобы качественно провести обслуживание аккумулятора и обеспечить правильную его работу, необходимо хотя бы приблизительно представлять, что у него внутри и как все это работает. Поэтому, прежде чем перейти к вопросам об электролите, необходимо понять, как устроен автомобильный аккумулятор и по какому принципу он работает.
Конструкция батареи
Практически все свинцово–кислотные батареи имеют одинаковую конструкцию. Состоят они из отдельных секций (банок), каждая из которых имеет набор положительных и отрицательных пластин. Первые называются катодными и выполнены из металлического свинца. Вторые, анодные, сделаны из диоксида свинца. Пластины собраны в пакет и помещены в кислотостойкую емкость, в которую впоследствии заливается рабочая жидкость – водный раствор серной кислоты или так называемый электролит.
Устройство секции свинцово-кислотного аккумулятора:
- 1 – крышка банки;
- 2 – корпус банки;
- 3 – ребристый отстойник;
- 4 – пластины, собранные в пакет;
- 5 – отрицательный (анодный) вывод;
- 6 – отрицательный (анодные) пластины;
- 7 – диэлектрическая прокладка – сепаратор;
- 8 – положительный (катодный) вывод;
- 9 – положительные (катодные) пластины.

Готовые секции, соединенные последовательно, и являются аккумуляторной батареей. В шестивольтовых АКБ таких секций три, в 12-ти вольтовых – шесть.
Как это работает
Итак, конструкция АКБ достаточно проста, но каким образом на ее выводах появляется напряжение? Действительно, если взять батарею прямо из магазина и подключить к ней вольтметр, то прибор покажет «0». Отсутствие тока обусловлено тем, что электролит не заливается в батарею сразу после изготовления, и в стоящем на магазинной полке аккумуляторе пластины сухие. Рабочая жидкость заливается в АКБ уже после покупки.
Самое время выяснить, для чего нужен электролит. Поскольку положительные и отрицательные пластины имеют различный химический состав, между ними, погруженными в кислотный раствор, возникает разность потенциалов (примерно 2 В на секцию, чем и обусловлено количество секций в батарее). При подключении к клеммам АКБ нагрузки между пластинами, благодаря высокой электропроводности электролита, начинает течь ток. Одновременно начинается химический процесс преобразования диоксида свинца в сульфат свинца с участием серной кислоты. Как только количество диоксида и серной кислоты упадет до определенного уровня, процесс прекратится, и батарея перестанет вырабатывать ток – разрядится.
В процессе разрядки серная кислота и диоксид свинца расходуются на образование сульфата свинца
Но аккумуляторы, в отличие от гальванических элементов (батареек), могут восстанавливать свои химические свойства. Если подключить АКБ к источнику постоянного тока, то под его действием сульфат начнет разлагаться на диоксид свинца и серную кислоту. Батарея начнет заряжаться, преобразуя электрическую энергию в химическую. Как только количество диоксида и кислоты достигнет исходных величин, батарею можно считать заряженной.
Химические процессы, возникающие в батарее при ее разрядке и зарядке
Серная кислота, входящая в состав электролита, играет одну из основных ролей в работе АКБ.
Именно от ее свойств будет зависеть качественная и долговременная работа батареи в целом.
Понятие плотности электролита
Вполне понятно, что количество серной кислоты и диоксида свинца в батарее должно быть сбалансированным – ведь они расходуются вместе. Поскольку количество диоксида свинца определяется производителем, автомобилисту после покупки аккумулятора остается лишь заправить АКБ необходимым количеством кислоты. Емкость секций батареи тоже фиксирована, поэтому в нее больше нормы не зальешь.
Остается единственный вариант – разбавить кислоту нейтральной к свинцу жидкостью, что и делается. Разбавляется кислота обычной водой, но дистиллированной, чтобы соли, содержащиеся в обычной воде, не нарушили чистоту раствора и не вывели АКБ из строя. Обычно автолюбитель покупает уже готовый электролит нужной плотности в автомагазине, хотя приготовить его можно и самостоятельно.
Процентное отношение воды к кислоте в полностью заряженном аккумуляторе составляет 70/30. Но при составлении электролита и его измерениях намного удобнее пользоваться единицами плотности – г/см. куб. или кг/м. куб. Удельный вес воды и кислоты различен, а значит, по общей плотности раствора можно судить о процентном соотношении его составляющих – концентрации.
Оптимальная концентрация кислоты
Пониженная концентрация, как правило, приводит к ускоренной сульфатации пластин – образованию на них нерастворимого сульфата свинца, который уже не может разложиться на кислоту и диоксид. В результате емкость батареи катастрофически падает, КПД уменьшается, а внутреннее сопротивление увеличивается (сульфат – диэлектрик).
Даже полностью заряженная, но сульфатированная батарея, выдающая, казалось бы, нормальное напряжение, садится после первого пуска, а то и вообще не в состоянии провернуть стартер. Кроме того, электролит с низкой плотностью замерзает при более высоких температурах, а значит, на стоянке даже при легком морозе батарею попросту разорвет льдом.
Чрезмерно высокая плотность электролита в аккумуляторной батарее не менее опасна, поскольку излишняя кислотность сокращает ресурс батареи в разы, буквально съедая пластины. Конечно, аккумулятор, залитый одной кислотой, будет крутить «как зверь», но сколько проживет такая АКБ? Сутки, может неделю. Если повезет – месяц.
А теперь пора вернуться к оптимальной плотности. В сети можно увидеть множество таблиц «рекомендованной» плотности, в зависимости от климатических условий. Если тепло – пониже, если мороз – повыше. Чем грозят эти «повыше» и «пониже», было описано в предыдущих абзацах. Поэтому не стоит изобретать велосипед, поскольку все эксперименты уже провели производители АКБ, а рекомендованная плотность приводится в сопроводительной документации.
С новым, сухим (сухозаряженным) аккумулятором все просто – в него заливается электролит комнатной температуры с плотностью 1.28 г/см. куб. Через час концентрация упадет до 1.26 – 1.27 г/см. куб., и батарея готова к работе. Далее, в процессе заряда/разряда аккумулятора и в зависимости от температуры окружающей среды, плотность раствора будет все время колебаться. Больше разряд – ниже плотность, идет заряд – плотность повышается. В нормально функционирующей АКБ отношение плотности к степени заряда и напряжению на клеммах выражается следующими показателями:
- 1.265 кг/м. куб. — 12.6 … 12.7 В — полностью заряжена;
- 1.225 кг/м. куб. — 12.3 … 12.4 В — 75%;
- 1.190 кг/м. куб. — 12.0 … 12.1 В — 50%;
- 1.115 кг/м. куб. — 11.8 … 11.9 В — 25%;
- 1.120 кг/м. куб. — 11.6 … 11.7 В — разряжена;
- ниже 1.120 кг/м. куб. — ниже 11.6 В — глубокий разряд.
Стоит обратить внимание на то, что все параметры батареи, включая плотность и напряжение, сильно зависят от температуры. Поэтому значения справедливы только при 26.7 градусах Цельсия. Если нужно провести измерения при другой температуре окружающей среды, то дополнительно придется воспользоваться таблицей плотности электролита от температуры, которую несложно найти в сети.
Выяснив зависимость плотности от выходного напряжения батареи, а значит, и от степени ее заряда, контролировать концентрацию электролита несложно. Достаточно замерить напряжение на клеммах отключенного аккумулятора любым вольтметром, затем измерить плотность и проверить их соответствие.
Проверка плотности рабочей жидкости
Для измерения плотности жидкостей существуют специальные приборы – ареометры или плотномеры. Есть такой и для автомобильных аккумуляторов. Выполнен он в виде большого шприца, внутри которого расположен поплавок со специально отградуированной шкалой.
Поплавок автоареометра комплектуется специальным «шприцем» для работы в узкогорлых секциях аккумуляторов.
Для того чтобы измерить плотность в аккумуляторе, со всех его секций сворачиваются пробки. Далее грушу ареометра сжимают, а его иглу погружают в секцию. Отпустив грушу, набирают в шприц электролит. При этом поплавок прибора всплывает. Плотность жидкости считывают со шкалы по тому уровню, до которого всплыл поплавок.
Поплавок всплыл до уровня 1.200. Плотность электролита – 1.2 г/см. куб.
После измерения грушу вновь сжимают, а после слива электролита обратно в батарею ареометр промывают проточной водой и сушат. Не следует забывать, что каждая секция – отдельная, независимая часть АКБ, поэтому плотность нужно измерить в каждой.
Когда и чем доливают аккумулятор
Необходимость доливки рабочей жидкости в батарею возникает нечасто, но она бывает необходимв. Что, сколько и в каких случаях нужно доливать? Всего таких случаев два: низкий уровень электролита и ненормальная кислотность рабочей жидкости.
Низкий уровень в секциях
Эта ситуация возникает часто, поскольку в процессе работы батареи вода испаряется или, как принято говорить, выкипает.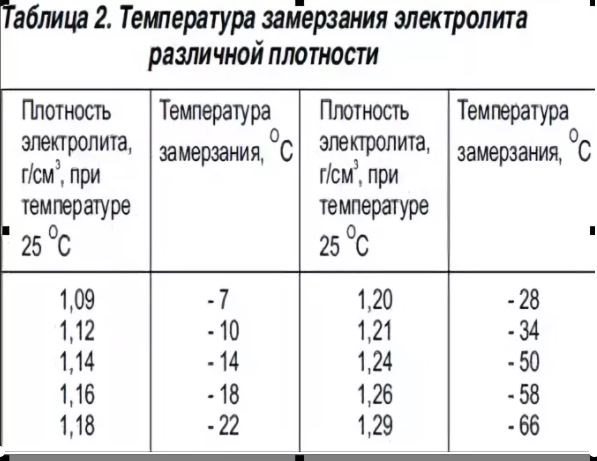 При этом уровень раствора в секциях уменьшается, и края пластин оказываются сухими. Определить это можно визуально, просто свинтив пробки с секций и заглянув в заливные горловины. Нормальный уровень жидкости в секции должен быть примерно на 1 см выше уровня среза пластин. В некоторых АКБ даже имеется специальная метка, отштампованная на корпусе. Если уровень низкий, то ситуация хоть и серьезна, но устранить ее легко. Для этой операции понадобятся:
При этом уровень раствора в секциях уменьшается, и края пластин оказываются сухими. Определить это можно визуально, просто свинтив пробки с секций и заглянув в заливные горловины. Нормальный уровень жидкости в секции должен быть примерно на 1 см выше уровня среза пластин. В некоторых АКБ даже имеется специальная метка, отштампованная на корпусе. Если уровень низкий, то ситуация хоть и серьезна, но устранить ее легко. Для этой операции понадобятся:
- медицинский шприц без иглы или автомобильный ареометр;
- дистиллированная вода;
- средства защиты (очки и резиновые перчатки).
Дистиллированная вода набирается в шприц и заливается в соответствующие секции, до нужного уровня. После доливки жидкости в аккумулятор его ставят на зарядку. В этом плане автоареометр намного предпочтительней, поскольку, долив воду, тут же можно проконтролировать плотность раствора.
Следует соблюдать осторожность: нельзя работать с кислотой, если глаза не защищены.
Ненормальная кислотность
Если изначально батарея была заправлена как положено, то чрезмерно большая плотность электролита в аккумуляторе может появиться только в случае, если выкипела вода или измерения проводились при сильном морозе (с понижением температуры плотность повышается, и это нормально). В первом случае достаточно просто долить воду, во втором – произвести перерасчет или, что проще и правильнее, заняться измерениями в отапливаемом помещении.
А вот падение концентрации кислоты – ситуация реальная. Обычно это происходит из-за неправильной эксплуатации АКБ или ввиду ее «преклонного возраста». Причина – появление нерастворимого сульфата, который при своем образовании использовал кислоту, но уже не разлагается при зарядке, а значит, вернуть ее обратно в раствор не может. Ситуация не особо радостная, но восстановить плотность необходимо хотя бы для того, чтобы дотянуть до покупки новой батареи.
Прежде чем принять решение о доливке кислоты, необходимо еще раз убедиться в том, что плотность действительно ниже положенной при текущем состоянии АКБ. Если решение принято, то понадобятся ареометр, перчатки, очки и корректирующий электролит плотностью 1.35 — 1.40 г/см. куб. (в продаже есть и такой).
Если решение принято, то понадобятся ареометр, перчатки, очки и корректирующий электролит плотностью 1.35 — 1.40 г/см. куб. (в продаже есть и такой).
Корректирующий электролит для доливки в автомобильный аккумулятор
В крайнем случае подойдет и стандартный 1.28 г/см. куб., но, возможно, придется отобрать лишнюю жидкость из секции в отдельную емкость, чтобы освободить место для более «крепкого».
Методика доливки та же, что и воды, но при этом плотность в банке постоянно контролируется тем же ареометром.
Категорически запрещается поднимать концентрацию раствора доливкой чистой серной кислоты. Во-первых, это очень опасно, во-вторых, даже нескольких грамм концентрированной кислоты достаточно, чтобы кардинально изменить плотность раствора в секции, а значит, выставить нужную плотность пол-литровым ареометром исключительно сложно.
Плотность электролита в аккумуляторе очень важный параметр у всех кислотных АКБ, и каждый автовладелец должен знать: какая плотность должна быть, как её проверить, а самое главное, как правильно поднять плотность аккумулятора (удельный вес кислоты) в каждой из банок со свинцовыми пластинами заполненных раствором h3SO4.
Проверка плотности – это один из пунктов процесса обслуживания аккумуляторной батареи, включающий так же проверку уровня электролита и замер напряжения АКБ. В свинцовых аккумуляторах плотность измеряется в г/см3. Она пропорциональна концентрации раствора, а обратно зависима, относительно температуры жидкости (чем выше температура, тем ниже плотность).
По плотности электролита можно определить состояние батареи. Так что если батарея не держит заряд, то следует проверить состояние её жидкости в каждой его банке.
Плотность электролита влияет на емкость аккумулятора, и срок его службы.
Проверяется денсиметром (ареометр) при температуре +25°С. В случае, если температура отличается от требуемой, в показания вносятся поправки, как показано в таблице.
Итак, немного разобрались, что это такое, и что нужно регулярно делать проверку. А на какие цифры ориентироваться, сколько хорошо, а сколько плохо, какой должна быть плотность электролита аккумулятора?
Выдерживать оптимальный показатель плотности электролита очень важно для аккумулятора и стоит знать, что необходимые значения зависят от климатической зоны. Поэтому плотность аккумулятора должна быть установлена исходя из совокупности требований и условий эксплуатации. К примеру, при умеренном климате плотность электролита должна находиться на уровне 1,25-1,27 г/см3 ±0,01 г/см3. В холодной зоне, с зимами до -30 градусов на 0,01 г/см3 больше, а в жаркой субтропической — на 0,01 г/см3 меньше. В тех регионах, где зима особо сурова (до -50 °С), дабы аккумулятор не замерз, приходится повышать плотность от 1,27 до 1,29 г/см3.
Много автовладельцев задаются вопросом: «Какой должна быть плотность электролита в аккумуляторе зимой, а какой летом, или же нет разницы, и круглый год показатели нужно держать на одном уровне?» Поэтому, разберемся с вопросом более подробно, а поможет это сделать, таблица плотности электролита в аккумуляторе с разделением на климатические зоны.
Нюанс, который следует знать — чем меньше плотность электролита в полностью заряженном аккумуляторе, тем он дольше прослужит.
Также нужно помнить, что, как правило, аккумуляторная батарея, находясь на автомобиле, заряжена не более чем на 80-90 % её номинальной ёмкости, поэтому плотность электролита будет немного ниже, чем при полном заряде. Так что, требуемое значение, выбирается чуть-чуть повыше, от того, которое указано в таблице плотности, дабы при снижении температуры воздуха до максимального уровня, АКБ гарантированно оставался работоспособным и не замерз в зимний период. Но, касаясь летнего сезона, повышенная плотность может и грозить закипанием.
Но, касаясь летнего сезона, повышенная плотность может и грозить закипанием.
Высокая плотность электролита приводит к снижению срока службы аккумуляторной батареи. Низкая плотность электролита в аккумуляторе приводит к снижению напряжения, затрудненному пуску двигателя.
Таблица плотности электролита в аккумуляторе
Таблица плотности составляется относительно среднемесячной температуры в январе-месяце, так что климатические зоны с холодным воздухом до -30 °C и умеренные с температурой не ниже -15 не требуют понижения или повышения концентрации кислоты. Круглый год (зимой и летом) плотность электролита в аккумуляторе не стоит изменять, а лишь проверять и следить, чтобы она не отклонялась от номинального значения, а вот в очень холодных зонах, где столбик термометра часто на отметке ниже -30 градусов (в плоть до -50), корректировка допускается.
Плотность электролита в аккумуляторе зимой
Плотность электролита в аккумуляторе зимой должна составлять 1,27 (для регионов с зимней температурой ниже -35 не менее 1.28 г/см3). Если будет значение ниже, то это приводит к снижению электродвижущей силы и трудного запуска двигателя в морозы, вплоть до замерзания электролита.
Снижение плотности до 1,09 г/см3, приводит к замерзанию АКБ уже при температуре -7°С.
Когда в зимнее время плотность в аккумуляторной батареи понижена, то не стоит сразу бежать за корректирующим раствором дабы её поднять, гораздо лучше позаботится о другом – качественном заряде АКБ при помощи зарядного устройства.
Получасовые поездки от дому к работе и обратно не позволяют электролиту прогрется, и, следовательно, хорошо зарядится, ведь аккумулятор принимает заряд лишь после прогрева. Так что разряженность изо дня в день увеличивается, и в результате падает и плотность.
Проводить самостоятельные манипуляции с электролитом крайне нежелательно, допускается только корректировка уровня дистиллированной водой (у легковых – 1,5 см над пластинами, а грузовых до 3 см).![]()
Для новой и исправной АКБ нормальный интервал изменения плотности электролита (полный разряд – полный заряд) составляет 0,15-0,16 г/см3.
Помните, что эксплуатация разряженного аккумулятора при минусовой температуре приводит к замерзанию электролита и разрушению свинцовых пластин!
По таблице зависимости температуры замерзания электролита от его плотности, можно узнать минусовой порог столбика термометра, при котором образовывается лед в вашем аккумуляторе.
Как видите, при заряженности на 100% аккумуляторная батарея замерзнет при -70 °С. При 40% заряде замерзает уже при -25 °С. 10% не только не дадут возможности запустить двигатель в морозный день, но и напрочь замерзнет в 10 градусный мороз.
Когда плотность электролита не известна, то степень разряженности батареи проверяют нагрузочной вилкой. Разность напряжения в элементах одной батареи не должна превышать 0,2В.
Показания вольтметра нагрузочной вилки, B
Степень разряженности батареи, %
Если АКБ разрядилась более чем на 50% зимой и более чем на 25% летом, её необходимо подзарядить.
Плотность электролита в аккумуляторе летом
Летом аккумулятор страдает от обезвоживания, поэтому учитывая то, что повышенная плотность плохо влияет на свинцовые пластины, лучше если она будет на 0,02 г/см3 ниже требуемого значения (особенно касается южных регионов).
В летнее время температура под капотом, где зачастую находится аккумулятор, значительно повышена. Такие условия способствуют испарению воды из кислоты и активности протекания электрохимических процессов в АКБ, обеспечивая высокую токоотдачу даже при минимально допустимом значении плотности электролита (1,22 г/см3 для теплой влажной климатической зоны). Так что, когда уровень электролита постепенно падает, то повышается его плотность, что ускоряет процессы коррозионного разрушения электродов. Именно поэтому так важно контролировать уровень жидкости в аккумуляторной батарее и при его понижении добавить дистиллированной воды, а если этого не сделать, то грозит перезаряд и сульфация.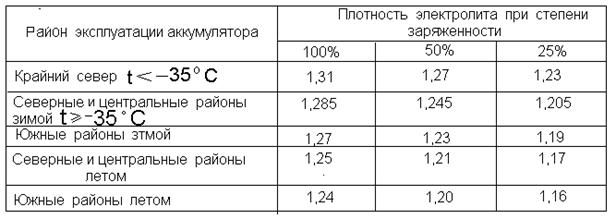
Стабильно завышенная плотность электролита приводит к снижению срока службы АКБ.
Если аккумулятор разрядился по невнимательности водителя или другим причинам, следует попробовать вернуть ему его рабочее состояние при помощи зарядного устройства. Но перед тем как заряжать АКБ, смотрят на уровень и по надобности доливают дистиллированную воду, которая могла испариться в процессе работы.
Через некоторое время плотность электролита в аккумуляторе, из-за постоянного разбавления его дистиллятом, снижается, и опускается ниже требуемого значения. Тогда эксплуатация батареи становится невозможной, так что возникает необходимость повысить плотность электролита в аккумуляторе. Но для того, чтобы узнать насколько повышать, нужно знать как проверять эту самую плотность.
Дабы обеспечить правильную работу аккумуляторной батареи, плотность электролита следует проверять каждые 15-20 тыс. км пробега. Измерение плотности в аккумуляторе осуществляется при помощи такого прибора как денсиметр. Устройство этого прибора состоит из стеклянной трубки, внутри которой ареометр, а на концах — резиновый наконечник с одной стороны и груша с другой. Чтобы произвести проверку, нужно будет: открыть пробку банки аккумулятора, погрузить его в раствор, и грушей втянуть небольшое количество электролита. Плавающий ареометр со шкалой покажет всю необходимую информацию. Более детально как правильно проверить плотность аккумулятора рассмотрим чуть ниже, поскольку есть еще такой вид АКБ, как необслуживаемые, и в них процедура несколько отличается — вам не понадобится абсолютно никаких приборов.
Разреженность батареи определяется по плотности электролита – чем меньше плотность, тем более разряжена батарея.
Индикатор плотности на необслуживаемой АКБ
Плотность необслуживаемого аккумулятора отображается цветовым индикатором в специальном окошке. Зеленый индикатор свидетельствует, что все в норме (степень заряженности в пределах 65 — 100%), если плотность упала и требуется подзарядка, то индикатор будет черный. Когда в окошке отображается белая или красная лампочка, то нужен срочный долив дистиллированной воды. Но, впрочем, точная информация о значении того или иного цвета в окошке, находится на наклейке аккумуляторной батареи.
Когда в окошке отображается белая или красная лампочка, то нужен срочный долив дистиллированной воды. Но, впрочем, точная информация о значении того или иного цвета в окошке, находится на наклейке аккумуляторной батареи.
Теперь продолжаем далее разбираться, как проверять плотность электролита обычного кислотного аккумулятора в домашних условия.
Проверка плотности электролита, с целью выяснения необходимости её корректировки, производится только у полностью заряженной батареи.
Проверка плотности электролита в аккумуляторе
Итак, чтобы можно было правильно проверить плотность электролита в аккумуляторной батарее, первым делом проверяем уровень и при необходимости его корректируем. Затем заряжаем аккум и только тогда приступаем к проверке, но не сразу, а после пары часов покоя, поскольку сразу после зарядки или долива воды будут недостоверные данные.
Следует помнить, что плотность напрямую зависит от температуры воздуха, поэтому сверяйтесь с таблицей поправок, рассматриваемой выше. Сделав забор жидкости из банки аккумулятора, держите прибор на уровне глаз – ареометр должен находиться в состоянии покоя, плавать в жидкости, не касаясь стенок. Замер производится в каждом отсеке, а все показатели записываются.
Таблица определения заряженности аккумулятора по плотности электролита.
Приготовление электролита для аккумуляторных батарей
Какова зависимость плотности электролита от климатической зоны?
Электролит приготовляется путём разведения аккумуляторной серной кислотыплотностью 1,83-1,84 г/см3 (ГОСТ 667–73) в дистиллированной воде с допустимыми примесями.
Химическая чистота электролита оказывает существенное влияние наработоспособность и срок службы батарей. Загрязнение электролита такими вредными примесями, как железо, марганец, хлор и другие, приводит к повышенному саморазряду батарей, снижению отдаваемой ёмкости, разрушению электродов ипреждевременному выходу батареи из строя. Поэтому для приготовления электролита запрещается применять техническую серную кислоту и загрязненную (недистиллированную) воду. При приготовлении электролита, приведении батарей в рабочее состояние и техническом обслуживании батарей в процессе эксплуатациинеобходимо пользоваться только специальной посудой (стойкой к действию серной кислоты) и соблюдать чистоту.
Поэтому для приготовления электролита запрещается применять техническую серную кислоту и загрязненную (недистиллированную) воду. При приготовлении электролита, приведении батарей в рабочее состояние и техническом обслуживании батарей в процессе эксплуатациинеобходимо пользоваться только специальной посудой (стойкой к действию серной кислоты) и соблюдать чистоту.
В исключительных случаях при отсутствии дистиллированной воды для приготовления электролита допускается использование снеговой или дождевой воды, предварительно профильтрованной через чистое полотно для очистки от механических загрязнений. Нельзя собирать воду с железных крыш и в железные сосуды.
Электролит следует готовить в стойкой к действию серной кислоты посуде (эбонитовой, фаянсовой, керамической и т.п.), соблюдая при этом особую осторожность и правила техники безопасности. Применение железной, медной или цинковой посуды категорически запрещается!
Аккумуляторные батареи в зависимости от климатической зоны заливаются электролитом, имеющим плотность, указанную в графе 4 таблицы №1: «Плотность электролита при приведении аккумуляторных батарей в рабочее состояние с учётом климатических зон». Электролит требуемой плотности может быть приготовлен непосредственно из кислоты плотностью 1,83-1,84 г/см3 и дистиллированной воды. Однако при непрерывном вливании кислоты в воду происходит сильный разогрев раствора (80-90°C) и требуется длительное время для его остывания. Поэтому для приготовления электролита требуемой плотности более удобно применять раствор кислоты промежуточной плотности 1,40 г/см3, так как в этом случае значительносокращается время охлаждения электролита.
Раствор серной кислоты плотностью 1,40 г/см3, приведённой к 25°C, должен готовиться заранее и после охлаждения храниться в стеклянной или полиэтиленовой посуде.
Количество воды, кислоты или её раствора плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита, указано в таблице №2: «Количество дистиллированной воды, кислоты или её раствора плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита требуемой плотности при температуре 25°C».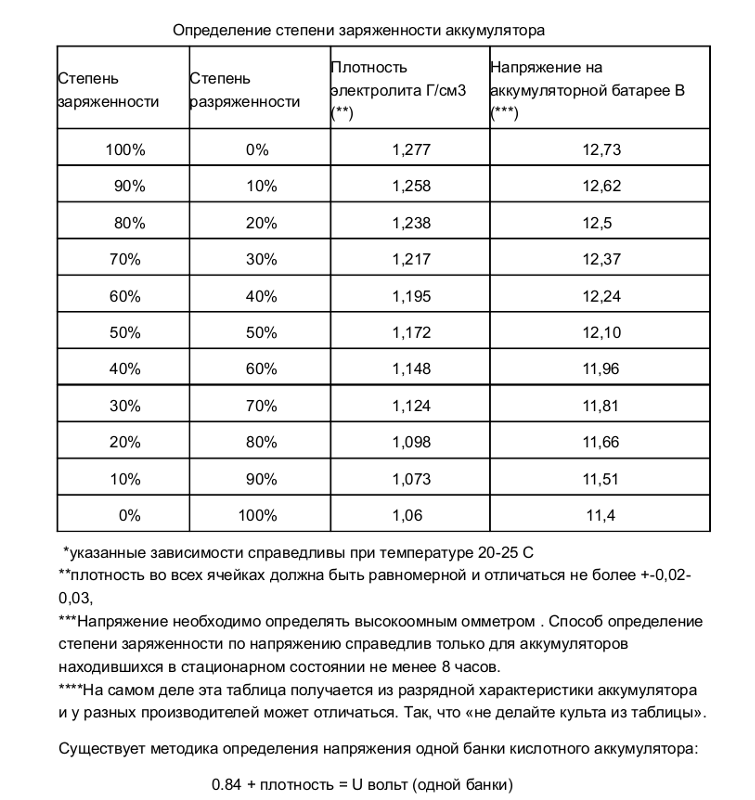
Таблица №1:
Плотность электролита при приведении аккумуляторных батарей
в рабочее состояние с учётом климатических зон
| Климатические зоны и районы | Средняя месячная температура воздуха в январе, °C | Время года | Плотность электролита, приведённая к 25°C, г/см3 | |
| заливаемого | полностью заряженной батареи | |||
| 1 | 2 | 3 | 4 | 5 |
| очень холодная | от –50 до –30 | зима | 1,28 | 1,30 |
| лето | 1,24 | 1,26 | ||
| холодная | от –30 до –15 | круглый год | 1,26 | 1,28 |
| умеренная | от –15 до –4 | круглый год | 1,24 | 1,26 |
| тёплая и влажная | от +4 до + 6 | круглый год | 1,20 | 1,22 |
| жаркая | от –15 до +4 | круглый год | 1,22 | 1,24 |
Расчёт проводится в такой последовательности: определяется общий объём электролита для заливки нужного числа батарей, затем подсчитывается количество дистиллированной воды и раствора кислоты плотностью 1,40 г/см3, нужное для приготовления электролита заданной плотности для заливки всех батарей.
Таблица №2:
Количество дистиллированной воды, кислоты или её раствора
плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита
требуемой плотности при температуре 25°C
| Требуемая плотность электролита, г/см3 | Количество воды, л | Количество серной кислоты плотностью 1,83 г/см3 | Количество воды, л | Количество раствора серной кислоты плотностью 1,40 г/см3, л |
|
| л | кг | ||||
| 1,20 | 0,859 | 0,200 | 0,365 | 0,547 | 0,476 |
| 1,21 | 0,849 | 0,211 | 0,385 | 0,519 | 0,500 |
| 1,22 | 0,839 | 0,221 | 0,405 | 0,491 | 0,524 |
| 1,23 | 0,829 | 0,231 | 0,424 | 0,465 | 0,549 |
| 1,24 | 0,819 | 0,242 | 0,444 | 0,438 | 0,572 |
| 1,25 | 0,809 | 0,253 | 0,464 | 0,410 | 0,601 |
| 1,26 | 0,800 | 0,263 | 0,484 | 0,382 | 0,624 |
| 1,27 | 0,791 | 0,274 | 0,503 | 0,357 | 0,652 |
| 1,28 | 0,781 | 0,285 | 0,523 | 0,329 | 0,679 |
| 1,29 | 0,772 | 0,295 | 0,541 | 0,302 | 0,705 |
| 1,31 | 0,749 | 0,319 | 0,585 | 0,246 | 0,760 |
1).
 Если требуется приготовить электролита больше или меньше одного литра, необходимо взять количество воды и кислоты или раствора, кратное или долевое к указанному в таблице. Например, для приготовления 5 л электролита количество воды и кислоты, приведённое в таблице, нужно умножить на 5, а для приготовления 0,5 л – умножить на 0,5.
Если требуется приготовить электролита больше или меньше одного литра, необходимо взять количество воды и кислоты или раствора, кратное или долевое к указанному в таблице. Например, для приготовления 5 л электролита количество воды и кислоты, приведённое в таблице, нужно умножить на 5, а для приготовления 0,5 л – умножить на 0,5.2). Аккумуляторная серная кислота учитывается на складах и выдаётся потребителям не в литрах, а в килограммах, поэтому при составлении заявки и получении кислоты со склада надо знать потребное её количество в килограммах. Можно также определить нужное количество кислоты в килограммах, умножив рассчитанное её количество в литрах на 1,83.
При возникновении сомнений относительно температуры замерзания электролита обратитесь к таблице №3
Таблица №3:
Температура замерзания электролита
| Плотность электролита при 25°C, г/см3 |
Температура замерзания, °C |
Плотность электролита при 25°C, г/см3 |
Температура замерзания, °C |
| 1,09 | –7 | 1,22 | –40 |
| 1,10 | –8 | 1,23 | –42 |
| 1,11 | –9 | 1,24 | –50 |
| 1,12 | –10 | 1,25 | –54 |
| 1,13 | –12 | 1,26 | –58 |
| 1,14 | –14 | 1,27 | –68 |
| 1,15 | –16 | 1,28 | –74 |
| 1,16 | –18 | 1,29 | –68 |
| 1,17 | –20 | 1,30 | –66 |
| 1,18 | –22 | 1,31 | –64 |
| 1,19 | –25 | 1,32 | –57 |
| 1,20 | –28 | 1,33 | –54 |
| 1,21 | –34 | 1,40 | –37 |
Заливка батарей электролитом
Температура электролита, заливаемого в аккумуляторные батареи, должна быть не выше 30°C и не ниже 15°C. Непосредственно перед заливкой электролита вывёртывают вентиляционные пробки и удаляют детали или элементы пробки, герметизирующие вентиляционные отверстия. Если в горловине под пробкой имеется герметизирующий диск, его необходимо удалить. Затем постепенно, небольшой струёй заливают электролит до тех пор, пока поверхность электролита не коснётся нижнего торца тубуса горловины крышки.
Непосредственно перед заливкой электролита вывёртывают вентиляционные пробки и удаляют детали или элементы пробки, герметизирующие вентиляционные отверстия. Если в горловине под пробкой имеется герметизирующий диск, его необходимо удалить. Затем постепенно, небольшой струёй заливают электролит до тех пор, пока поверхность электролита не коснётся нижнего торца тубуса горловины крышки.
Заниженная плотность электролита приводит к снижению ЭДС и затруднению пуска двигателя, а также к повышению опасности замерзания электролита в зимний период эксплуатации.
Приготовление электролита | Аккумуляторные батареи
Страница 14 из 26
4.3. Приготовление электролита для свинцовых аккумуляторов
Электролит для свинцовых аккумуляторов приготовляется путем разбавления чистой серной кислоты чистой водой. Кислота продается обычно концентрированной, удельного веса от 1,835 до 1,840. При разбавлении концентрированной кислоты раствор сильно нагревается. Во избежание опасности для лица, производящего смешивание, всегда необходимо наливать кислоту в воду, но не наоборот.
Хотя количество теплоты, развиваемой в обоих случаях, одно и то же, однако удельные теплоты воды и концентрированной кислоты совершенно различны. Струя воды, попадая в концентрированную кислоту, освобождает большое количество теплоты, которая благодаря низкой удельной теплоте кислоты вызывает сильное местное повышение температуры. Кислота, приливаемая к воде, не может вызвать столь же большого повышения температуры в силу того, что удельная теплота воды очень высока. Необходимо непрерывно перемешивать раствор все время, пока кислота подливается в воду, для того, чтобы помешать более тяжелой кислоте опуститься на дно сосуда, не смешавшись с водой.
Для смешивания и хранения небольших количеств электролита наиболее подходят сосуды фарфоровые, гончарные или стеклянные; но так как они легко дают трещины, то им следует предпочесть чаны, выложенные свинцом, особенно для более значительных количеств.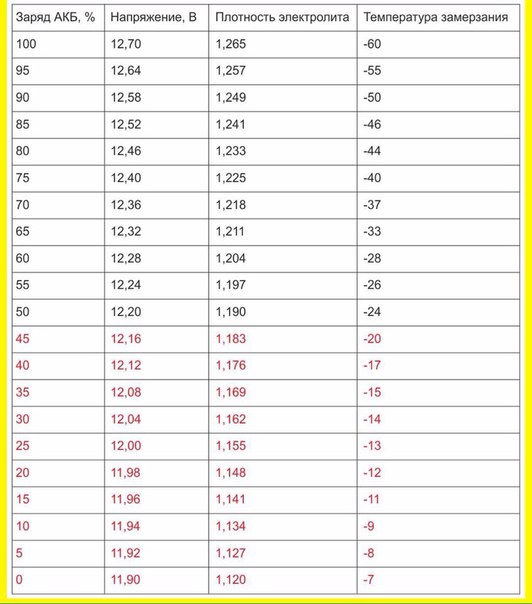
Никакие другие металлические сосуды, кроме свинцовых, непригодны.
После разбавления кислоты, до заливки ее в батарею, необходимо подождать, пока она остынет, для того чтобы избежать повреждений пластин и сепараторов.
Охлаждение можно ускорить, пользуясь струей сжатого воздуха, но воздух при этом должен быть чистым.
Избежать сильного повышения температуры при смешивании кислоты с водой можно, применяя вместо воды лед, приготовленный из дистиллированной воды. Понижение температуры происходит вследствие того, что скрытая теплота плавления льда приблизительно равна количеству теплоты, освобождающемуся при растворении серной кислоты. Лед, свободный от воды, можно прибавлять к кислоте непосредственно. Избыток поглощенной теплоты показывает, что раствор должен получить температуру ниже нуля, что и наблюдалось в действительности.
Чтобы облегчить приготовление электролитов любой требуемой концентрации, на рис. 4.1 приведены необходимые пропорции кислоты и воды. Аккумуляторные заводы обычно сообщают сведения о том, какой крепости кислоту следует применять для каждой данной батареи.
Рис. 4.1. Приготовление электролита любого удельного веса из концентрированной кислоты удельного веса 1,835.
1- содержание серной кислоты, %; 2 – требующаяся добавка воды по объему; 3 – то же по весу.
4.4. Приготовление электролита для кадмиевоникелевых и железоникелевых аккумуляторов
Для кадмиевоникелевых и железоникелевых аккумуляторов в качестве электролита служит раствор в дистиллированной воде едкого калия (КОН) или едкого натрия (NaOH).
В зависимости от температуры окружающего воздуха в аккумуляторах (табл. 4.1) применяется раствор соответствующей плотности (концентрации) основного компонента электролита в чистом виде или с добавкой едкого лития (LiOH).
Кадмиевоникелевые аккумуляторы рассчитаны на работу на холоде при температуре до – 40°С, причем при температурах +35…– 19°С с составным электролитом, а при более низких температурах, например, – 20. ..– 40°С с электролитом без добавки едкого лития.
..– 40°С с электролитом без добавки едкого лития.
При температурах – 20…– 40°С при отсутствии чистого едкого калия допускается как исключение применять составной электролит из едкого калия и едкого лития повышенной плотности, при этом емкость аккумулятора снижается на 10 – 15%. При отсутствии составного электролита из едкого калия и едкого лития при температуре – 19…+35°С можно воспользоваться составным электролитом из едкого натрия повышенной плотности 1,17 – 1,19 г/см3 с добавкой на 1 л раствора 20 г едкого лития, но при этом следует учесть, не гарантируется.
Таблица 4.1.
Рекомендуемые состав и плотность электролита для кадмиевоникелевых и железоникелевых аккумуляторов при различной температуре окружающего воздуха
Температура воздуха, °С | Рекомендуемый состав электролита | Плотность, г/см3 |
– 19… +35 | Составной раствор едкого калия с добавкой на 1 л раствора 20 г едкого лития аккумуляторного (моногидрата лития) | 1,19 – 1,21 |
– 20… – 40 | Раствор едкого калия | 1,25 – 1,27 |
+10…+50 | Раствор едкого натрия с добавкой на 1 л раствора 15 – 20 г едкого лития (моногидрата лития) | 1,1 – 1,12 |
Не гарантируется также долговечность аккумуляторов при работе их с электролитом из раствора чистого едкого калия плотностью 1,19 – 1,21 г/см3, т. е. без добавки едкого лития при температуре –19… + 10°С. При работе при температуре + 10…+50°С с рекомендуемым составным электролитом плотностью 1,1–1,12 г/см3 (табл. 5.1) емкость аккумуляторов также снижается по сравнению с номинальной, а долговечность не гарантируется.
Железоникелевые аккумуляторы рассчитаны на работу в тех же условиях и с тем же электролитом, что и кадмиевоникелевые, но они более чувствительны к низким температурам, поэтому могут применяться при температурах не ниже –20° С.
В процессе эксплуатации температурные условия в зависимости от времени года резко изменяются, поэтому для более эффективного использования емкости аккумуляторов их следует заливать электролитом, по составу и плотности соответствующим этим условиям.
Кроме того, необходимо систематически контролировать количество электролита, т. е. следить за уровнем последнего и поддерживать его в установленных пределах.
В аккумуляторах, находящихся в эксплуатации, уровень электролита постепенно снижается вследствие испарения, поэтому его необходимо периодически измерять и при необходимости дополнять до нормы дистиллированной водой. Не реже чем через 10 циклов нужно проверять плотность электролита и также доводить ее до нормы добавлением раствора плотностью 1,41 г/см3 или дистиллированной воды.
Уровень электролита в аккумуляторах должен постоянно находиться выше края пластин не менее чем на 5 мм и не более чем на 12 мм.
Снижение уровня электролита ниже верхнего края пластин или сетки, а также повышение плотности электролита при положительных температурах окружающего воздуха снижают емкость и долговечность последних. Уровень электролита необходимо проверять и доводить до указанной нормы перед каждым зарядом. Он проверяется с помощью стеклянной трубки диаметром 5 – 6 мм с метками на высоте 5 и 12 мм от конца. Для установления уровня электролита в аккумуляторе надо конец трубки с метками ввести через заливное отверстие до упора в пластины или сетку, после чего другой конец трубки закрыть пальцем. Вынув трубку из аккумулятора по высоте столбика электролита в ней, определим уровень электролита над верхним краем пластин или сетки в аккумуляторе. Для снижения уровня электролита в аккумуляторе можно пользоваться пипеткой или резиновой грушей со стеклянным или пластмассовым наконечником длиной около 100 мм. Доливку электролита или дистиллированной воды в аккумуляторы можно производить с помощью пипетки, резиновой груши или кружки через стеклянную воронку, размеры которых подбирают в зависимости от вместимости аккумуляторов. Проверка плотности электролита производится при помощи сифонного ареометра.
Доливку электролита или дистиллированной воды в аккумуляторы можно производить с помощью пипетки, резиновой груши или кружки через стеклянную воронку, размеры которых подбирают в зависимости от вместимости аккумуляторов. Проверка плотности электролита производится при помощи сифонного ареометра.
Проверку плотности электролита необходимо производить по возможности перед каждым зарядом, в каждом аккумуляторе, хотя и допускается выборочный контроль в 2 – 3 аккумуляторах батареи. В крайнем случае проверка должна проводиться не реже чем через 10 циклов во всех аккумуляторах батареи.
Таким образом, электролит необходим не только для первой заливки аккумуляторов при формировке, но и для замены, поддержания плотности и уровня электролита в действующих аккумуляторах, поэтому его требуется приготовлять и всегда иметь запас.
Для приготовления электролита поставляются следующие исходные материалы:
а) едкий калий аккумуляторный марки А (твердый) или марки В (жидкий) и едкий литий аккумуляторный;
б) составная щелочь сорта А – готовая смесь едкого калия и едкого лития в отношении едкий литий/едкий калий = 0,04…0,045;
в) едкий натрий аккумуляторный (сода каустическая) сорта А и едкий литий аккумуляторный;
г) составная щелочь сорта Б – готовая смесь едкого натрия и едкого лития в соотношении едкий литий/едкий натрий = 0,028…0,032.
Перед приготовлением электролита необходимо удостовериться, что имеющиеся в наличии химические ‘компоненты соответствуют приведенным выше требованиям и ГОСТам. Хранить эти материалы необходимо в герметически закрытой таре. Данные материалы могут поставляться как в жидком, так и в твердом состоянии в виде гранул, чешуек, кусков или слитка.
Приготовление электролита следует начинать с определения потребности в нем согласно норме расхода на один аккумулятор при первой заливке, указанной в табл. 4.2.
Определив требуемое количество электролита, приготовим примерно 3/4 этого объема свежей дистиллированной воды. При отсутствии последней допускается применение дождевой воды, собранной с чистой поверхности, или воды, полученной при таянии снега, а также конденсата.
При отсутствии последней допускается применение дождевой воды, собранной с чистой поверхности, или воды, полученной при таянии снега, а также конденсата.
Таблица 4.2
Ориентировочная норма расхода электролита на один аккумулятор при первой заливке
Тип | Норма расхода электролита при первой заливке, л | Тип | Норма расхода электролита при первой заливке, л |
АКН-2,25 | 0,04 | КН-60 | 0,75 |
Примечание. При приготовлении электролита желательно норму увеличить на 10 – 15 % для создания резерва на отход и другие непредвиденные случаи.
В крайнем случае можно использовать любую сырую чистую питьевую воду (кроме минеральной).
Затем, пользуясь данными табл. 5.3, определяем необходимое количество химических компонентов: едкого калия или едкого натрия, а также едкого лития для добавки. Расход дистиллированной воды на 1 кг твердой и на 1 л жидкой щелочи для приготовления электролита необходимой плотности приведен в табл. 4.3.
Таблица 4.3
Расход дистиллированной воды, необходимой для приготовления электролита для кадмиевоникелевых и железоникелевых аккумуляторов
Щелочь | Плотность, г/смз3 | Количество воды, л | |
на 1 кг твердой щелочи | на 1 кг жидкой щелочи плотностью 1,41 г/см3 | ||
Калиевая или готовая составная, т. Калиево-литиевая Натриевая или готовая составная натриево-литиевая |
1,19 – 1,21 1,25 – 1,27
1,17– 1,19 |
3 2
5 |
1 0,55
1,5 |
Для определения массы твердых щелочей, необходимой по норме, приведенной в табл. 19, достаточно разделить:
на три требуемое количество воды, если необходимо приготовить калиевый или составной калиево-литиевый раствор плотностью 1,19 – 1,21 г/см3;
на два, если необходимо приготовить калиевый электролит для работы при температуре
– 20…– 40° С или составной калиево-литиевый плотностью 1,25 –1,27 г/см3;
на пять, если необходимо приготовить натриевый или составной натриево-литиевый электролит плотностью 1,17 – 1,19 г/см3.
Если составная калиево-литиевая или натриево-литиевая щелочь отсутствуют, а имеется едкий калий, едкий натрий и едкий литий, то расчет потребности в твердых щелочах производится по тому же принципу, как указано выше. Следует иметь в виду, что в частном, полученном в результате деления, учитывается и масса едкого лития.
Приготовление электролита для щелочных аккумуляторов!
Исходным материалом для приготовления электролита для щелочных аккумуляторов являются:
- вода дистиллированная, нормируемая по ГОСТ 6709-72
В случае крайней необходимости допускается применять любую питьевую отстоянную воду, кроме минеральной.
- кали едкое КОН (ГОСТ 9285-69) сорт А или В;
- лития, гидрат окиси технический Li(ОН)3 (ГОСТ 8595-75).

Наличие в растворе электролита едкого лития повышает срок службы аккумулятора в 3 раза и обеспечивает для никель-кадмиевых аккумуляторов 1000 циклов заряд-разряд.
Допускается использовать:
- электролит калиево-литиевый щелочной жидкий ТУ № 6-18-84-70;
- электролит калиево-литиевый твердый ТУ № 6-18-58-69.
Едкие щелочи должны быть герметически укупорены во избежание порчи из-за поглощения углекислого газа из воздуха:
- твердые — в железных запаянных банках;
- жидкие — в стеклянных бутылях, закрытых резиновыми пробками и дополнительно залитых парафином.
Употребление кусков едкой щелочи, окрашенных в бурый или желтый цвет, ЗАПРЕЩАЕТСЯ.
Приготовление электролита должно производиться в чистой железной, чугунной или пластмассовой посуде с плотно закрывающимися крышками.
ЗАПРЕЩАЕТСЯ применение оцинкованной, луженной, медной, алюминиевой, свинцовой, керамической и стеклянной посуды, а также посуды, используемой для приготовления электролита кислотных аккумуляторов.
Рекомендуемые плотность и состав электролита в зависимости от температуры эксплуатации, а также соотношения компонентов для приготовления электролита необходимой плотности приведены в соответствующих таблицах инструкции по эксплуатации АКБ.
Приготовление электролита необходимо производить в следующей последовательности:
- влить в сосуд необходимое количество воды;
- с помощью чистых стальных щипцов опускать в воду небольшими порциями куски твердой щелочи или тонкой струйкой вливать жидкую щелочь;
- для ускорения растворения щелочи раствор перемешивать пластмассовой, эбонитовой, стальной или стеклянной мешалкой;
- откорректировать плотность электролита
При всех измерениях плотности электролита должна быть измерена и его температура. В случаях, когда она отличается от + 15°С, в результат измерения плотности необходимо внести поправку, имея ввиду, что повышение температуры на каждый 1°С вызывает уменьшение плотности электролита на 0,005 г/см
3.
В случаях, когда она отличается от + 15°С, в результат измерения плотности необходимо внести поправку, имея ввиду, что повышение температуры на каждый 1°С вызывает уменьшение плотности электролита на 0,005 г/см
3.
- посуду с электролитом прикрыть от доступа воздуха и дать ему остыть до температуры не более 300°С и отстояться в течение 3-6 часов до полного осветления;
- осторожно слить осветленную часть электролита и использовать ее для заливки аккумуляторов.
При использовании для приготовления электролита калиево-литиевой щелочи плотностью 1,41 г/см 3, имеющей белый осадок не растворившегося лития едкого аккумуляторного, необходимо разбавлять щелочь водой до требуемой плотности, одновременно помешивая раствор электролита до растворения осадка.
Для хранения электролит разлить в стеклянные бутыли, которые закрыть резиновыми пробками и залить парафином. На бутыли укрепить бирки с указанием состава, плотности и даты приготовления электролита.
Рекомендуем ознакомиться со следующими материалами:
Почему автомобильные аккумуляторы плохо работают в холодную погоду?
Процесс запуска автомобильного двигателя морозным зимним утром может доставить вам массу хлопот, если не позаботиться о нем с вчера. Часто двигатель незапускается из-за аккумуляторной батареи (АКБ). Почему АКБ чувствительнее к внешним условиям, чем другие узлы и системы автомобиля? Ответ кроется в способности АКБ преобразовывать химическую энергию в электрическую с минимальным выделением тепла и в малом объеме тепловой энергии, доступной при низкой температуре.
Приступая к работе
Помню, как пару лет назад я осенью купил себе машину. Зима оказалась одной из самых холодных за последние несколько лет. На протяжении двух недель столбик садового термометра не поднимался выше -10°C.
Мы отдыхали на шведском горнолыжном курорте.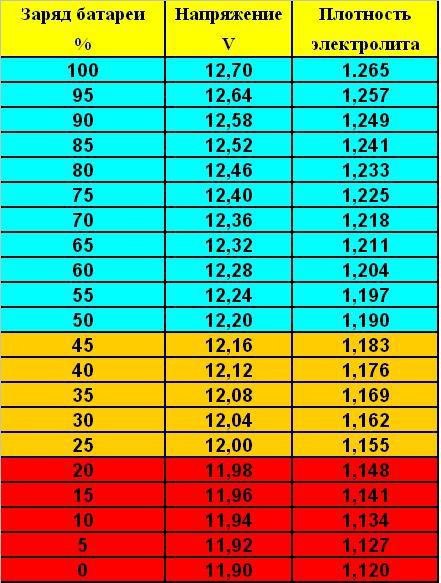 И вот одним февральским утром я вышел на улицу завести машину, рассчитывая с комфортом довезти семью до подъемника. Поворот ключа зажигания… Машина едва завелась. Судя по звуку, все шесть цилиндров работали не так плавно как обычно. Прежде чем двигатель заурчал как раньше, прошла почти целая минута. Меня это насторожило, ведь машина была новой. ЖК-экран между спидометром и тахометром медленно ожил. -35°C за бортом! Этим утром обойдемся без лыж!
И вот одним февральским утром я вышел на улицу завести машину, рассчитывая с комфортом довезти семью до подъемника. Поворот ключа зажигания… Машина едва завелась. Судя по звуку, все шесть цилиндров работали не так плавно как обычно. Прежде чем двигатель заурчал как раньше, прошла почти целая минута. Меня это насторожило, ведь машина была новой. ЖК-экран между спидометром и тахометром медленно ожил. -35°C за бортом! Этим утром обойдемся без лыж!
Поскольку я по специальности инженер-электрохимик, мысли мои от заснеженных склонов плавно обратились к старому доброму свинцово-кислотному аккумулятору, который к тому моменту уже выдавал на стартер пиковый ток, так что двигатель запускался с пол-оборота.
Проблема не ограничивается АКБ, работа любого двигателя внутреннего сгорания в условиях крайне низких температур будет неустойчивой. Масло системы смазки густеет, реакции сгорания замедляются, а в важных участках системы подачи топлива может замерзнуть конденсат. Однако, моя машина завелась. А вот автомобиль с электрическим двигателем вряд ли удалось бы завести, если не подключать его на ночь к розетке.
В чем разница? Ответ кроется в том, как именно химическая энергия преобразуется в механическую:
- ДВС преобразует содержащуюся в топливе химическую энергию в тепло, которое затем преобразуется в механическую энергию.
- Двигатель электромобиля преобразует химическую энергию АКБ в электрическую, которая в дальнейшем преобразуется в механическую электромотором. В сравнении с ДВС количество выделяемого тепла гораздо меньше.
Процесс преобразования ДВС тепловой энергии в механическую приводит к образованию большого количества тепла, прогревающего двигатель, уже на первом такте, что обеспечивает практически мгновенное начало движения. В двигателе электромобиля тепло при низкой температуре образуется медленно, поэтому прогрева не происходит. Как говорил Лес Гроссман: «Законы физики. Их не остановить».
Обратите внимание, что КПД при преобразовании химической энергии в механическую в электромобиле гораздо выше, так как потери энергии в АКБ и электродвигателе относительно невелики.
Оставим в стороне проблемы КПД и теплообразования и, прежде чем перейти к разговору об АКБ, давайте сравним процессы, осложняющие запуск двигателя электромобиля и обычного автомобиля в условиях низкой температуры.
Сравнение процессов, протекающих в транспортных средствах
Начнем сравнение с двигателей: электрического и ДВС. Мы можем предположить, что электродвигатель в меньшей степени подвержен влиянию низких температур по сравнению с ДВС. Количество движущихся компонентов в электродвигателе меньше, а между ними находится воздух, поэтому они должны требовать меньше смазки и быть не столь чувствительны к воздействию низких температур.
Конструктивно трансмиссия электромобиля менее сложна, чем трансмиссия автомобиля, оснащенного ДВС, так как электродвигатель может работать с большим диапазоном нагрузок, выдавая превосходный крутящий момент. Кроме того, в электромобиле может быть установлено несколько двигателей (например, один в передней, а второй в задней части), поэтому ему не требуется сложной силовой передачи для использования полного привода. Таким образом, электромобилю не нужна сложная коробка передач, требующая смазки. Соответственно, электромобиль должен быть менее восприимчив к фактору температуры.
Не забывайте и том, что электромобиль не нуждается в сложной системе подачи топлива с насосами, клапанами, датчиками, форсунками и т.д. Это также положительно скажется на чувствительности электромобиля к холодной погоде в сравнении с обычным автомобилем, ведь у него меньше компонентов, где возможно образование льда.
Самым слабым звеном в условиях холода ожидаемо является АКБ. Вообще-то влияние низких температур на работу аккумулятора можно наблюдать на множестве примеров: от военного и космического оборудования до мобильных телефонов и домашних охранных систем. Для автомобиля, оснащенного ДВС, данный компонент гораздо менее важен, так для его запуска требуется лишь кратковременный пиковый ток. Электромобилю для работы, напротив, необходим постоянный ток. Давайте поближе взглянем на работу АКБ и влияние на нее температуры.
Характеристики АКБ, зависящие от температуры
В состав АКБ входят два пористых электрода: положительный и отрицательный. Электропроводящий материал электрода состоит из частиц с большой плотностью. Пористость электродов вызвана пустотами между частицами (см. иллюстрацию ниже).
Два электрода отделены друг от друга электролитом. Кроме того, поры обоих электродов содержат электролит, заполняющий пустоты между частицами материала. Иллюстрация ниже демонстрирует процесс разряда в АКБ, причем размер частиц сильно преувеличен.
Потери в АКБ при указанном уровне заряда изображены на следующей иллюстрации, демонстрирующей вольтамперные кривые для положительного (красный) и отрицательного (синий) электродов. Рабочие точки электродов помечены как i1 и -i1. Предположим, что потенциал положительного и отрицательного электродов замеряется с помощью эталонного электрода по центру емкости с электролитом (см. иллюстрацию выше). Это необходимо для выяснения потенциала электродов по отдельности, а также для того, чтобы учесть активные потери на обоих концах эталонного электрода.
Напряжение гальванического элемента ниже по сравнению c напряжением разомкнутого (см. ниже) из-за потерь на активацию (вследствие кинетики электромеханической реакции) и массообмен, а также активных потерь. Обратите внимание, что катодный ток на положительном электроде определяется как отрицательно заряженный, в то время как анодный ток на отрицательном электроде — как положительно заряженный. Дело в том, что полярность электролита внутри АКБ обратна полярности внешней цепи.
Напряжение разомкнутого элемента
Разность потенциалов электродов при нулевой плотности тока называется напряжением разомкнутого элемента при заданном состоянии заряда, как показано на иллюстрации выше.
Это напряжение для АКБ в виде функции температуры при заданном состоянии заряда рассчитывается с помощью следующего выражения:
(1)
E_T^0 \approx E_{T^0}^0 + \frac{{\Delta S}}{{zF}}\left( {T -{T^0}} \right)
где E — напряжение элемента, {\Delta S} — изменение энтропии реакции АКБ, z — количество переданных электронов, F — постоянная Фарадея. Это значит, что для АКБ, в которой суммарная реакция разряда вызывает положительное изменение энтропии ({\Delta S}), рост температуры приведет к увеличению напряжения гальванического элемента. Для АКБ с отрицательным изменением энтропии это приведет к понижению напряжения.
Большая часть литий-ионных батарей, используемых в современных электрических устройствах, обладает небольшим отрицательным изменением энтропиии, что означает небольшой рост напряжения разомкнутого элемента при уменьшении температуры. Этого уже будет достаточно для улучшения работы в условиях низких температур. Однако, изменение напряжения открытого элемента в зависимости от температуры в сравнении с прочими параметрами относительно невелико и составляет около 0-0,4 мВ/К —менее 30 мВ в диапазоне от крайне низкой температуры (-35°C) до комнатной. Таким образом, причиной ухудшения эксплуатационных характеристик АКБ при низких температурах является термодинамика суммарной реакции ее разряда.
Физические характеристики электролита и электродов
Физические характеристики электролита оказывают значительное влияние на работу АКБ. Температура влияет на проводимость и диффузивность электролита и, соответственно, на эффективную проводимость и диффузивность электролита в порах электродов.
Проводимость электролита может увеличиваться на один или более порядков при изменении температуры от очень холодной (-35°C) до комнатной. Если мы построим логарифмический график проводимости электролита как функции 1/T, то получим линейную зависимость, представленную на иллюстрацию ниже. Данная иллюстрация демонстрирует уровень проводимости при низкой температуре и его рост в геометрической прогрессии при ее повышении.
Таки образом, активные (реостатные) потери в электролите АКБ возрастают при понижении температуры, что приводит к низкому напряжению гальванических элементов при заданной силе тока и низкой температуре. Кроме того, недостаточная проводимость электролита приводит к менее однородной плотности тока при распределении в пористых электродах, что, в свою очередь, снижает емкость АКБ. Емкость определяется как количество ампер-часов, которое можно извлечь из АКБ до быстрого падения напряжения. Емкость АКБ остается неизменной и при низких температурах, однако слабая проводимость и, соответственно, неравномерное распределение плотности тока не позволяют задействовать полную емкость АКБ до тех пор, пока она не нагреется.
Более того, диффузивность химических компонентов электролита, крайне важная для протекания электрохимических реакций, снижена в той же мере, что и проводимость электролита. Уменьшение диффузивности увеличивает перегрузку, что ведет к уменьшению напряжения гальванического элемента. Пониженная диффузивность также ведет к уменьшению емкости АКБ, так как крупные фракции частиц электродов АКБ становятся недоступными в результате ограничений массообмена.
Обратите внимание, что и проводимость, и диффузивность электролита связаны с подвижностью (см. соотношение Нернста — Эйнштейна).
С точки зрения физики пониженная подвижность является результатом того, что в электролите сокращается количество доступной тепловой энергии, следовательно ионам и молекулам становится сложнее преодолевать силу взаимодействия или трения. Подвижность в электролитических растворах как функция температуры описывается уравнением Аррениуса, в котором энергия активации (Ea на иллюстрации выше) представляет собой энергию необходимую для того, чтобы молекулы смогли преодолеть силу взаимодействия с соседними молекулами и начать двигаться в электролитическом растворе.
Твердый материал электрода, как правило, обладает проводимостью, на несколько порядков превышающей проводимость электролита в порах. Степень изменения проводимости в твердых материалах с изменением температуры обычно не оказывает влияния на эксплуатационные характеристики АКБ. Однако зарядка некоторых АКБ в условиях низкой температуры может стать проблематичной, так как приведет к образованию дендритов, разрушающих АКБ.
Кинетика электродов
Последним компонентом неустойчивой работы АКБ при низкой температуре является медленная кинетика анодных и катодных реакций, что приводит к перегрузке по напряжению при запуске. С точки зрения физики медленная кинетика электродов является следствием того, что энергию активации становится сложнее преодолеть, поскольку при низких температурах в системе доступно меньше тепловой энергии.
Иллюстрация ниже демонстрирует общее влияние роста потерь при запуске, активных потерь и затрат на массообмен на эксплуатационные характеристики АКБ. Мы видим, как рост общей перегрузки на двух электродах приводит к снижению напряжения гальванического элемента при указанной силе тока и состоянии заряда АКБ.
Эти кривые основываются на уравнениях Аррениуса для подвижности и кинетики электродов, которые для обратимых электрохимических реакций представляются в виде соответствующих уравнений Батлера — Вольмера.
Терморегулирование
Современные аккумуляторные системы электромобилей оснащаются сложными системами терморегуляции. Эти системы охлаждают АКБ при повышенных нагрузках или, напротив, нагревают ее при подключении к розетке холодной зимней ночью.
Система терморегуляции позволяет поддерживать АКБ в оптимальном диапазоне рабочих температур (см. иллюстрацию выше). Обратите внимание, что на графике показана не температура окружающей среды, а рабочая температура АКБ. Система терморегуляции также снижает риск возникновения термической нестабильности в литий-ионных АКБ.
Обогрев АКБ в условиях низких температур также приводит к снижению КПД электродвигателя и уменьшению максимальной дальности поездки, так как часть электроэнергии или регенерирующей мощности необходимо преобразовывать в тепловую энергию для поддержания температуры АКБ в оптимальном диапазоне. Кроме того, часть этой мощности может использоваться для обогрева кабины, что также негативно сказывается на КПД автомобиля и максимальной дальности поездки.
На иллюстрации выше представлены результаты моделирования автомобильной литий-ионной АКБ, оснащенной каналами для охлаждения и обогрева. Подобные модели широко используются при проектировании систем терморегуляции АКБ.
Заключение
Невозможность быстрого самостоятельного нагрева АКБ электромобиля после очень холодной зимней ночи, является следствием высокого КПД электродвигателя, а также того факта, что ему не требуется вырабатывать тепловую энергию, которая преобразуется в механическую работу. Поэтому в ночь перед лыжными вылазками вроде моей электромобиль нужно обязательно подключить к розетке, чтобы поддерживать температуру АКБ в пределах допустимого диапазона.
Если вы будете следовать этому совету, ваш электромобиль легко заведется даже в горах Швеции. На самом деле, большинство открытых парковок в условиях Севера (например, на Аляске, в Канаде, Швеции или Норвегии) оснащены электрическими розетками, а большинство бензиновых автомобилей оснащаются средствами обогрева двигателя. В таких условиях не стоит рисковать, даже если у вас автомобиль с двигателем внутреннего сгорания.
Если же вы забыли подключить машину к розетке на горнолыжном курорте, то лучше вернуться в уютный коттедж и вспомнить о Сванте Аррениусе, шведском ученом, который первым разработал количественное описание температурной зависимости скорости химических реакций от характеристик переноса.
Эксплуатация АКБ в зимний период — «БеларусЮгСервис»
Наверное, никому не надо объяснять, насколько исправная и стабильно работающая аккумуляторная батарея важна для успешной зимней эксплуатации автомобиля. Это и уверенный пуск двигателя в мороз, и нормальная работа сигнализации на стоянке, и возможность использования отопителя, и прочие составляющие комфортной и безопасной езды. Поговорим обо всем этом. А тем, кто автомобилем зимой не пользуется, мы подскажем, как лучше хранить батарею, чтобы она не потеряла своих эксплуатационных свойств.
Зимняя эксплуатация автомобиля сопровождается следующими неприятными для аккумуляторной батареи факторами:
-
понижается температура электролита, то есть возрастает его вязкость, снижается скорость диффузии в поры активного материала пластин, уменьшается электропроводность, что ведет к снижению эффективности процесса зарядки батареи от генератора при тех же величинах зарядного напряжения;
-
запуск холодного двигателя требует от АКБ большей мощности и энергии из-за увеличения значения разрядного тока и более продолжительной работы стартера, что приводит к более глубокому разряду батареи;
-
увеличивается число потребителей электроэнергии, предназначенных как для обеспечения комфорта в салоне, так и для безопасного движения, и если на высоких оборотах двигателя их питание происходит от генератора, то на холостых со всеми потребителями он уже не справляется и энергия берется от АКБ, что также снижает степень ее заряженности;
-
короткие зимние поездки по городу с частыми остановками, холодными пусками и последующим прогревом двигателя также становятся причиной постоянного недозаряда АКБ;
-
постоянные изменения температуры и высокая влажность воздуха в подкапотном пространстве приводят к ухудшению работы элементов электрооборудования, возникновению утечек тока по влажным проводам, которые разряжают АКБ, даже если зажигание выключено.
Кроме того, длительное воздействие предельных температур, постоянный недозаряд и холодные пуски двигателя способствуют снижению не только работоспособности стартерной батареи, но и ее ресурса.
Влияние всех перечисленных факторов на степень заряженности АКБ объективно усиливается, если генератор автомобиля по причине износа деталей или неисправности других элементов электрооборудования не обеспечивает номинальных показателей напряжения и тока нагрузки.
Если владелец автомобиля годами не проверяет генератор, не следит за исправностью электроприборов, за уровнем и плотностью электролита, не проверяет напряжение разомкнутой цепи (одна клемма снята) на аккумуляторе и периодически не подзаряжает его стационарно, то в зимнее время он оказывается заложником наполовину (а то и больше) разряженной АКБ, неспособной запустить холодный двигатель.
Исходя из всего вышесказанного, чтобы устранить влияние негативных факторов зимней эксплуатации АКБ, полезно проводить следующие мероприятия:
-
попытки пуска холодного двигателя производить в течение не более 5—10 секунд и с интервалом 30—60 секунд, а после трех неудачных попыток искать неисправность, чтобы окончательно не разрядить батарею;
-
контролировать натяжение ремня привода генератора согласно инструкции по эксплуатации автомобиля, чтобы обеспечить полную отдачу энергии для питания включенных потребителей и зарядки АКБ;
-
не допускать длительную работу потребителей на автомобиле при неработающем двигателе и минимизировать их количество при работающем;
-
периодически контролировать отсутствие утечки тока от АКБ на различные элементы электрооборудования при постановке на стоянку и отключать АКБ, если нет необходимости в работе, например, сигнализации или подогревателя;
-
дополнительно подсоединить «массовый» провод напрямую от АКБ к двигателю (если это не предусмотрено конструкцией автомобиля) с целью уменьшения потерь напряжения на стартере при пуске двигателя, поскольку переход от клеммы на кузов, а с кузова на двигатель приводит к потере мощности, потребляемой от АКБ;
-
обеспечить подогрев АКБ во время движения, подведя к ней тепло от радиатора или выпускного коллектора;
-
защитить АКБ от воздействия предельных температур, влаги и грязи с помощью теплоизоляционных материалов при условии соблюдения противопожарных требований и обеспечении ее нормальной вентиляции.
Кстати, в продаже имеются специальные «термосейфы» для АКБ, которые как раз и призваны защитить аккумуляторную батарею от переохлаждения зимой, от перегрева летом, от излишнего загрязнения поверхности и газоотводных отверстий, оптимизируя тем самым температурные условия ее эксплуатации, снижая испарение воды из электролита, вероятность разрушения АКБ от избытка давления и продлевая в конечном итоге срок ее службы.
Наконец, периодически (а не только в начале зимы) нужно контролировать плотность электролита (при наличии пробок на крышке АКБ) и замерять напряжение на полюсных клеммах батареи не ранее чем через 8—10 часов после остановки двигателя.
Что касается замера плотности, то тут нужно учитывать температуру окружающего воздуха и вводить соответствующую поправку к показаниям денсиметра, приводя их к занчению плотности электролита при +25°С. Примерные значения поправки даны в таблице.
Из графика на рис. 1 вы можете примерно определить степень разряженности АКБ в зависимости от плотности электролита, а также зависимость от нее НРЦ батареи и температуры замерзания электролита. Да-да, электролит в банках может замерзнуть, если плотность его будет слишком низкой! И батарею может если не разорвать льдом, то покоробить пластины или разрушить изоляцию между ними, вызвав короткое замыкание! По этой же причине доливать дистиллированную воду в АКБ зимой для обеспечения нормального уровня нужно только непосредственно перед зарядкой или длительной поездкой, чтобы она успела перемешаться с электролитом.
Рис. 1
Тем же, кто не собирается эксплуатировать автомобиль зимой, следует полностью зарядить АКБ перед длительным хранением и довести плотность электролита до номинальных значений, опять-таки чтобы батарея не замерзла.
Кстати, существует заблуждение, что нельзя в процессе эксплуатации добавлять в АКБ электролит, а только дистиллированную воду. Дескать, серная кислота отсюда никуда не девается и ее должно хватить на весь период эксплуатации. Но опыт показывает, что девается. Ведь электрохимические процессы в АКБ идут непрерывно, кислота вступает в реакцию с различными материалами и газами, образуя с ними новые химические соединения.
К тому же плотность электролита даже после заливки и полной зарядки самим производителем может не соответствовать условиям, принятым по ГОСТу для данного региона. И как еще устранить разницу в плотности в разных банках, если порой она достигает 0,02 г/куб. см и более?
Еще одно заблуждение касается условий хранения АКБ. Говорят, чтобы электролит не замерз, лучше принести ее из неотапливаемого гаража или стоянки домой, в тепло. Однако не следует забывать и про то, что чем выше температура окружающего воздуха, тем выше саморазряд батареи.
Рис. 2
Рис. 3
Так что при нормальной плотности на длительное хранение батарею лучше, наоборот, поместить в холодное место, но все же не забывать следить за ее напряжением и плотностью электролита. Ведь чем дольше время хранения, тем выше будет саморазряд батареи, зависимость которого примерно показана в виде графиков на рисунках 2 (для напряжения) и 3 (для плотности электролита).
Минимальный саморазряд характерен для батарей с пластинами из свинцово-кальциевых сплавов при температуре не выше нуля градусов, но по мере старения у АКБ любой конструкции саморазряд увеличивается. За время бездействия АКБ не должна разряжаться более чем на 30% от номинальных значений, поэтому периодически ее нужно подзаряжать.
Если вы храните батарею непосредственно на транспортном средстве, то следует отключить ее от бортовой сети, а если это невозможно (например, необходимо оставить машину под охраной сигнализации), то замеры плотности и напряжения следует делать чаще и своевременно подзаряжать ее.
Полюсные клеммы батареи на время хранения необходимо смазать нейтральной консистентной смазкой для защиты их от окисления.
Батареи в пластмассовых моноблоках следует хранить в закрытых помещениях с минимальной освещенностью, так как яркий свет ускоряет процесс старения полимерного материала.
Кроме того, следует внимательно изучить рекомендации самого производителя АКБ как по эксплуатации, так и по условиям хранения и придерживаться их по мере возможности.
Твердотельный Na-аккумулятор, работающий при комнатной температуре, с комплексным гидридом в качестве электролита
Основные характеристики
- •
Na 4 (CB 11 H 12 ) 2 (B 12 H 12 ) твердый электролит позволяет покрывать / снимать натрий с ограниченной поляризацией в течение> 500 часов работы.
- •
Гальваностатический цикл при 25 ° C Na | Na 4 (CB 11 H 12 ) 2 (B 12 H 12 ) | NaCrO 2 ячеек обеспечивают удельную емкость 100 мАч г — 1 — .
- •
Тест возможности скорости показывает хорошее сохранение емкости до C / 5. Более быстрые C-коэффициенты обеспечивают хорошую пропускную способность только при разряде 1 st .
- •
In situ EIS подтверждает, что емкость падает при высоких скоростях C из-за частичной потери контакта между Na-электродом и электролитом.
Abstract
Полностью твердотельные натриевые батареи потенциально могут изменить правила игры при переходе к обществу без ископаемого топлива.Они сочетают в себе лучшую экологичность, переход с лития на широко доступный натрий с повышенной безопасностью, заменяя легковоспламеняющийся жидкий электролит более термостойким твердым материалом. Тем не менее, несколько проблем мешают разработке высокопроизводительных ячеек, таких как электрохимическая стабильность твердого электролита по сравнению с как натриевого, так и положительного электрода, а также хрупкий межфазный контакт между компонентами ячейки. На основе проводника Na + , недавно разработанного нашей группой, Na 4 (CB 11 H 12 ) 2 (B 12 H 12 ), здесь мы сообщаем о его превосходных характеристиках. в качестве твердого электролита в аккумуляторах, работающих при комнатной температуре.Этот материал на основе гидробората carba closo — closo демонстрирует стабильное покрытие / удаление натрия с ограниченной поляризацией. Гальваностатические испытания в Na || NaCrO 2 Ячейки демонстрируют хорошие электрохимические характеристики благодаря удельной емкости около 100 мАч / г — 1 до поставляемой плотности тока 24 мА (изб.) — 1 . Эти результаты представляют собой шаг вперед на пути к надежным твердотельным батареям на основе натрия, работающим безопасно, сохраняя при этом высокую производительность даже при комнатной температуре.
Ключевые слова
Твердотельный аккумулятор Na
Твердый электролит
Комплексный гидрид
Смешивание анионов
In situ EIS
Рекомендуемые статьи Цитирующие статьи (0)
© 2019 Авторы. Опубликовано Elsevier BV
Рекомендуемые статьи
Цитирующие статьи
Печатные высокоэффективные пленки из твердотельного электролита
ВВЕДЕНИЕ
Потребность в более безопасных перезаряжаемых батареях, в которых не используется горючий жидкий органический электролит, побудила к развитию твердого электролита. -государственные электролиты (SSE) ( 1 — 3 ), такие как оксинитрид фосфора лития (LiPON) ( 4 , 5 ) и керамические соединения на основе граната ( 5 — 7 ).Пленки SSE (<10 мкм) с высокой ионной проводимостью> 10 -4 См / см обычно необходимы для достижения высоких плотностей энергии и мощности. Однако современные методы производства таких SSE-пленок имеют серьезные проблемы. Например, процесс радиочастотного (ВЧ) напыления в вакууме, используемый для нанесения LiPON на батареи, является непомерно дорогостоящим ( 8 — 10 ), что ограничивает его широкое применение. Аналогичным образом, другие вакуумные методы, используемые для изготовления различных керамических пленок SSE, такие как осаждение атомных слоев (ALD) ( 11 — 13 ), импульсное осаждение слоев (PLD) ( 14 , 15 ) химическое осаждение из паровой фазы (CVD) ( 16 , 17 ) требует больше времени и менее масштабируемо по сравнению с процессом с рулона на рулон.Кроме того, керамические SSE, полученные этими методами, обычно демонстрируют низкую ионную проводимость от ~ 10 -8 до 10 -4 См / см ( 17 — 19 ) из-за осажденной аморфной структуры или высокой потери летучих ионов. (например, Ли и На).
Для устранения этих ограничений были разработаны более экономичные и масштабируемые методы на основе решений для синтеза керамических пленок SSE (например, граната), но с ограниченным успехом из-за огромных проблем при спекании пленок электролита ( 11 , 20 , 21 ).В этих процессах SSE необходимо спекать при высоких температурах (от 600 до 1100 ° C) в течение нескольких часов, чтобы получить кристаллическую структуру, необходимую для высокой ионной проводимости. Однако продолжительное спекание также вызывает серьезные потери Li и Na и соответствующую низкую ионную проводимость из-за летучести этих легких элементов при высокой температуре ( 22 — 25 ). В результате керамические пленки SSE обычно демонстрируют либо плохую кристалличность, либо заметные потери лития с максимальной зарегистрированной ионной проводимостью ~ 10 -6 См / см ( 26 , 27 ).Снижение температуры обработки для предотвращения серьезных потерь Li ( 2 ) или добавление избыточного Li для компенсации ( 11 ) было обычной стратегией в традиционных методах осаждения керамической пленки. Однако это приводит к плохому контролю состава и потенциально пористой структуре. Кроме того, эти низкотемпературные спеченные SSE имеют аморфную структуру, что приводит к ограниченному улучшению проводимости до 2,9 × 10 -5 См / см ( 2 ), что далеко от объемного значения (~ 10 −3 См / см) ( 28 ).В то время как твердотельные пленочные батареи с низкой плотностью тока от 50 до 800 мкА / см 2 были успешно коммерциализированы в электронике ( 17 , 29 ), этот успех невозможно перенести на крупномасштабные приложения ( например, электромобили), для которых требуется плотность тока от 3 до 10 мА / см 2 ( 30 ). В результате существует постоянная потребность в масштабируемом методе синтеза керамических SSE с отличным контролем состава и кристалличностью для достижения необходимой высокой ионной проводимости.
В этой работе мы разработали нелогичный подход к синтезу керамических пленок SSE непосредственно из прекурсоров, в котором мы значительно увеличиваем температуру спекания (до 1500 ° C), но только на короткий период времени (~ 3 с). Такой быстрый нагрев позволяет формировать плотную поликристаллическую пленочную структуру, но с незначительными потерями летучих элементов из-за короткого времени спекания. Мы называем этот метод «печатью и радиационным нагревом» (PRH), основанный на растворе и пригодный для печати метод синтеза керамических SSE-пленок.В типичном процессе пленка-предшественник печатается на подложке с толщиной, точно настроенной путем управления концентрацией чернил и влажной толщиной. Затем высушенная на воздухе пленка прекурсора помещается в тесный контакт с полосой радиационного нагрева (обычно ~ 1500 ° C) для быстрого спекания в непосредственной близости (рис. 1A). Эта нагретая Джоуля полоса проходит через исходную пленку с зазором ~ 0,5 мм и общей продолжительностью нагрева несколько секунд для завершения процесса спекания, что потенциально позволяет производить обработку рулонов.Рисунок 1B и фиг. S1 представляет собой типичную керамическую SSE-пленку из сплава Li 6,5 La 3 Zr 1,5 Ta 0,5 O 12 (LLZTO) на монокристаллической подложке MgO, которая имеет полупрозрачную и плотную структуру. шероховатость поверхности <1 мкм (рис. 1С). Этот метод также не зависит от материала и позволяет спекать целый ряд высокоэффективных твердотельных пленок.
Рис. 1 PRH процесс синтеза пленки.( A ) Схема методики печати на пленке, в которой используются чернила-предшественник керамики и процесс быстрого спекания, при котором материал нагревается до высокой температуры (1500 ° C) в течение ~ 3 секунд.( B ) Спеченная пленка граната LLZTO на монокристаллической подложке MgO. ( C ) Соответствующая профилометрическая кривая спеченной пленки. Фото: Вэйвэй Пинг, Мэрилендский университет, Колледж-Парк.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для демонстрации метода PRH мы синтезировали керамическую пленку LLZTO SSE (подробности см. В дополнительных материалах). Вкратце, мы смешали порошок прекурсора (Li 2 CO 3 , La 2 O 3 , ZrO 2 и Ta 2 O 5 ) с помощью шаровой мельницы с последующим диспергированием в этаноле. путем обработки ультразвуком для приготовления чернил-прекурсоров (рис.2А). Чернила-предшественник LLZTO демонстрируют хорошую текучесть и смачиваемость на различных подложках (рис. 2B), таких как стекло, металлическая фольга и керамика, что позволяет создавать многофункциональные устройства. Кроме того, концентрация и вязкость чернил-предшественников могут быть изменены для адаптации к различным методам печати, таким как нанесение покрытия распылением и метод ракельного ножа. Мы использовали распылительное покрытие для нанесения чернил-предшественников, чтобы (i) достичь широкого диапазона толщин спеченных пленок LLZTO (от 1 до 100 мкм) и (ii) создать узорчатые пленки с использованием теневой маски, которая позволяет генерировать различные электролиты и электродные конструкции для изготовления будущих устройств (рис.2C и рис. S2). Для более толстых пленок без рисунка мы применили метод ракельного ножа для нанесения суспензии прекурсора на металлическую фольгу (30 см на 10 см) в окружающей среде (рис. 2D), создавая гладкую и однородную пленку (рис. 2Е и рис. S3).
Рис. 2 Оптимизация условий печати и спекания керамической пленки.( A ) Чернила-предшественник SSE, полученные диспергированием предшественников смешанных оксидов (Li 2 CO 3 , La 2 O 3 , ZrO 2 и Ta 2 O 5 ) в этаноле.( B ) Чернила SSE обладают хорошей текучестью. ( C ) Печать чернил-предшественников граната путем нанесения покрытия распылением через маску. ( D ) Печать чернил-предшественников SSE методом ракельного ножа. ( E ) Пленка SSE с печатью масштабируема и гибка. (От F до H ) Схематическое изображение и морфология поперечного сечения пленок граната LLZTO, спеченных при различных температурах и времени, при которых требуется адекватная температура спекания с соответствующим временем спекания для получения плотной пленки граната с ограниченными потерями Li и однородными гранулометрический состав.Рентгенограммы пленок LLZTO, спеченных при температурах от ( I ) от 800 до 1300 ° C и времени выдержки от 1 до 180 с и при ( J ) от 1400 ° до 1700 ° C и времени выдержки от 1 до 10 с. а.е., условные единицы. Фото: Вэйвэй Пинг, Мэрилендский университет, Колледж-Парк.
В типичном процессе PRH мы быстро спекали напечатанную пленку-предшественник в атмосфере аргона, перемещая нагретую Джоуля углеродную полосу по образцу в течение ~ 3 с (рис. S4).Чтобы продемонстрировать большую пленку на металлических подложках, мы изготовили гибкую композитную пленку LLZTO / LiBO 2 на фольге из нержавеющей стали размером 5 см на 2 см (рис. S5, A и B). LiBO 2 [30 мас.% (Мас.%)] Был добавлен для снижения температуры спекания композитной пленки SSE, чтобы подложка из нержавеющей стали не плавилась. Поверхность пленки LLZTO / LiBO 2 осталась конформной и плоской без каких-либо явных трещин или точечных отверстий при спекании, что демонстрирует превосходную однородность полученной большой пленки SSE (рис.S5, от C до E). Мы исследовали влияние температуры и времени спекания на полученные пленки LLZTO с помощью сканирующей электронной микроскопии (SEM) и дифракции рентгеновских лучей (XRD). При более низкой температуре спекания (~ 1000 ° C) полученная пленка имеет чистую фазу граната (рис. S6), но с пористой структурой даже при более продолжительном времени спекания, составляющем 10 с (рис. 2F). При более высокой температуре спекания (~ 1700 ° C) спеченная пленка показывает аномальный рост зерен (рис. 2H), значительную потерю Li (рис. S6) и побочную реакцию с подложкой (рис.S7), даже если время спекания ограничено всего 1 с. Однако мы обнаружили, что оптимизированное сочетание высокой температуры и короткого времени обработки (1500 ° C, 3 с) позволило получить плотную структуру граната с минимальными потерями Li и побочными реакциями (рис. 2G и рис. S6).
Чтобы лучше понять эволюцию пленки-предшественника LLZTO во время спекания PRH, мы спекали пленки при температурах от ~ 800 ° до 1700 ° C и временах от 1 до 180 с. Мы измерили дифрактограммы спеченных пленок, чтобы охарактеризовать потенциальные фазовые изменения, связанные с потерей лития (рис.2I). Согласно рентгенограммам, прекурсоры начинают реагировать и образовывать кубическую гранатовую фазу при низких температурах от 800 ° до 1000 ° C через ~ 30 с. Однако мы наблюдали, что низкотемпературные спеченные пленки оставались непрозрачно-белыми, что указывало на пористую структуру, что мы также подтвердили с помощью SEM (рис. S8). Пористая структура граната сохранялась даже при повышении температуры до ~ 1200 ° C и времени спекания до 180 с, где также наблюдалась небольшая потеря Li из-за появления небольшой частицы La 2 Zr 2 O 7 пик (рис.2I). Однако при повышении температуры до 1300-1500 ° C напечатанные пленки-предшественники стали прозрачными, что указывает на плотную структуру. При дальнейшем повышении температуры скорость испарения Li также быстро увеличивалась, о чем свидетельствует заметный фазовый переход до La 2 Zr 2 O 7 из-за значительных потерь Li (рис. 2, I и J). .
На основе дополнительных экспериментов по спеканию и рентгеноструктурных исследований мы построили диаграмму квазивремя-температура-превращение (TTT), чтобы определить оптимальные условия спекания, которые будут определять будущий синтез (рис.S9). На квази-TTT-диаграмме есть четыре основных участка, указывающих на различные плотности и фазы спеченных пленок LLZTO. Согласно диаграмме квази-ТТТ, спекание от 3 до 10 с при температуре от 1300 до 1500 ° C является предпочтительным для получения прочной пленки с минимальными потерями Li и плотной структурой. Когда температура спекания ниже 1200 ° C, требуется длительное время спекания для достижения плотной структуры пленки. Однако увеличенные потери Li во время такого длительного спекания приведут к образованию фазы La 2 Zr 2 O 7 , особенно для пленок граната, из-за низкого исходного содержания Li и более коротких расстояний диффузии.Следовательно, температура и время спекания должны быть хорошо оптимизированы для получения плотной пленки SSE с чистой фазой граната и минимальными потерями Li.
Как показано на СЭМ-изображении поперечного сечения (рис. 3A), высокая температура 1500 ° C может обеспечить достаточно энергии для спекания пленки LLZTO и получения однородной структуры без явных пор (рис. S10, A и B). . Даже при толщине всего ~ 1,5 мкм пленка все еще имеет плотную структуру без явных точечных отверстий на изломанной поверхности (рис. S10C). Рентгенограмма пленки LLZTO также соответствует стандартной кубической фазе граната (PDF № 01-080-4947; рис.S10D), что указывает на минимальные потери Li. Кроме того, в традиционных методах спекания Al 2 O 3 может легко легироваться в SSE на основе граната в процессе спекания ( 31 , 32 ), что может влиять на ионную проводимость и химическую стабильность SSE. Картирование поперечного сечения энергодисперсионной рентгеновской спектроскопии (EDS) PRH-спеченного LLZTO (рис. 3B) показывает четкую границу раздела с подложкой Al 2 O 3 , что подтверждает отсутствие очевидного кроссоверного легирования между LLZTO. пленка и подложка.Отсутствие перекрестного легирования дополнительно демонстрирует преимущество сочетания высокой температуры и короткого времени спекания, которое стало возможным благодаря технологии PRH. Кроме того, быстрый процесс спекания предотвращает аномальный рост зерен при высокой температуре, что демонстрируется равномерным распределением зерен по размерам (~ 1,6 ± 0,7 мкм) на изображениях СЭМ вида сверху (рис. 3, C и D).
Рис. 3 Характеристики пленки LLZTO, спеченной методом PRH.( A ) СЭМ-изображение поперечного сечения и ( B ) EDS-отображение спеченной пленки LLZTO на подложке из Al 2 O 3 .( C ) Морфология поверхности спеченной пленки LLZTO на подложке Al 2 O 3 . ( D ) Статистика гранулометрического состава спеченной пленки LLZTO. ( E ) Энергия активации спеченной с помощью PRH пленки LLZTO, согласованная с соотношением Аррениуса. ( F ) Профили напряжения и тока симметричной ячейки Li / LLZTO / Li с плоскими Li-электродами для испытания критической плотности тока. ( G ) Сравнение потерь Li в пленках, спеченных PRH и традиционными методами.( H ) Сравнение ионной проводимости при комнатной температуре пленок SSE, синтезированных методом PRH и другими известными методами ( 2 , 8 , 9 , 11 , 35 — 41 ) .
Мы оценили ионную проводимость пленок граната LLZTO, спеченных методом PRH, с помощью спектроскопии электрохимического импеданса (EIS) в диапазоне температур от 30 ° до 140 ° C (рис. S11) с использованием плоских Li-электродов (рис. S12). Энергия активации переноса лития, соответствующая аррениусовскому поведению литий-ионной проводимости, составляла 0.34 эВ (рис. 3E), аналогично массивному гранату, в то время как ионная проводимость при комнатной температуре достигала ~ 1.0 × 10 −3 См / см, что сравнимо с проводимостью массивного граната ( 23 , 33 ). Мы также оценили критическую плотность тока пленки LLZTO, проводя осаждение / зачистку Li в плоскости пленки Li / LLZTO / симметричной ячейки Li. Симметричная ячейка подвергалась циклическому циклу при плотностях тока от 0,2 до 5 мА / см 2 с продолжительностью 10 мин (рис. 3F). Пленка LLZTO, спеченная с помощью PRH, показала плотность критического тока 5 мА / см 2 (рис.3F и рис. S12), что является одним из самых высоких заявленных значений даже для массивных гранатовых SSE ( 28 , 34 ). Чтобы лучше охарактеризовать устойчивость к циклированию пленки LLZTO, спеченной методом PRH, для симметричной ячейки Li / LLZTO пленка / Li также было проведено испытание на длительное циклирование (фиг. S13 и S14). Пленка Li / LLZTO / симметричная ячейка Li может успешно работать в течение более 140 часов при плотностях тока от 0,2 до 3 мА / см 2 , что свидетельствует о превосходной стабильности при циклировании пленки LLZTO, спеченной методом PRH.
Мы приписываем отличные электрохимические свойства спеченных с помощью PRH пленок LLZTO строгому контролю содержания Li, плотной морфологии и высокой кристалличности, которые достигаются во время чрезвычайно высокотемпературного и сверхбыстрого процесса спекания. Напротив, обычные процессы спекания обычно занимают часы при температуре> 1000 ° C, что приводит к значительным потерям Li. Это особенно верно для пленок (например, толщиной ~ 1 мкм) по сравнению с обычными толстыми гранулами (например, ~ 1000 мкм), поскольку количество Li намного ниже, а удельная площадь поверхности намного выше, что приводит к большим потерям Li. в обычных процессах спекания (рис.3G). Однако высокая скорость метода PRH ограничивает потери Li в таких пленочных структурах, что позволяет нам получить пленку граната LLZTO, которая демонстрирует самую высокую ионную проводимость среди тонкопленочных SSE (рис. 3H) ( 2 , 8 , 9 , 11 , 35 — 41 ).
Метод спекания PRH основан на радиационном нагреве, который не зависит от материала и может применяться для спекания широкого диапазона составов. Чтобы продемонстрировать универсальность этой методики, мы успешно изготовили Li 0.3 La 0,567 TiO 3 (LLTO), Li 1,3 Al 0,3 Ti 1,7 (PO 4 ) 3 (LATP) и β-Al 2 O 3 пленки из растворов чернил-предшественников (рис. 4A), все из которых содержат летучие компоненты. LLTO, LATP и β-Al 2 O 3 — это высокоэффективные литий-ионные и Na-ионные проводники, пленки которых также сталкиваются с проблемой контроля потерь Li / Na во время синтеза ( 19 , 42 , 43 ).В нашем методе мы напечатали краски LLTO, LATP и β-Al 2 O 3 на подложке из Al 2 O 3 путем нанесения покрытия распылением с последующим высокотемпературным (1500 ° C) спеканием. в течение ~ 3–5 с, что приводило к однородным и плотным пленкам толщиной от 5 до 10 мкм (рис. 4Б). Пленки LATP и LLTO спекались на воздухе, чтобы предотвратить возможное восстановление Ti 4+ . Как и в случае с пленкой LLZTO, в соответствии с картированием EDS не наблюдалось явного перекрестного легирования или побочных реакций между слоем SSE и подложкой (рис.4Б). Границы зерен спеченных пленок также хорошо сливались из-за эффекта плавления при высокой температуре спекания. Кроме того, благодаря быстрому процессу спекания в течение 3 с, потери Li / Na в SSE LATP, LLTO и β-Al 2 O 3 были минимизированы, что мы подтвердили с помощью чистых фаз на рентгенограммах ( фиг. S15 — S17).
Рис. 4 Другие пленки SSE, спеченные на PRH.( A ) Печатные краски на основе прекурсоров LLTO, LATP, β-Al 2 O 3 и LiBO 2 -LLZTO.( B ) Слева: морфология поперечного сечения и результаты элементарного картирования пленок LLTO, LATP, β-Al 2 O 3 , спеченных с помощью PRH. Справа: Схема сравнения потерь летучих элементов между PRH и традиционными методами спекания. ( C ) Слева: морфология поперечного сечения и результаты картирования пленки LiBO 2 -LLZTO, спеченной методом PRH. Справа: Схема сравнения контроля побочной реакции между PRH и традиционными методами. Фото: Вэйвэй Пинг, Мэрилендский университет, Колледж-Парк.
Помимо однокомпонентных пленок, нашу технологию PRH можно также использовать для быстрого спекания композитных пленок, так как короткое время спекания может эффективно предотвратить побочные реакции между материалами. Чтобы продемонстрировать эту способность, мы спекали композитную SSE-пленку LiBO 2 -LLZTO (рис. 4, A и C). Полученный материал содержал LiBO 2 , равномерно распределенный между зернами LLZTO с конформными поверхностями раздела и без явного совместного легирования, вероятно, из-за короткого времени спекания, составляющего 3 секунды, даже при высокой температуре спекания 1200 ° C.Напротив, когда мы спекали те же материалы в обычной печи в течение 1 часа, мы получали пористую структуру с крупными прореагировавшими зернами, а не плотный композит (рис. S18). Часовое спекание в обычной печи приводит к заметной перекрестной диффузии и побочным реакциям между компонентами, в то время как метод PRH позволяет избежать таких побочных реакций с образованием композитных структур (рис. 4C, справа). Эта способность производить широкий спектр как однокомпонентных, так и многокомпонентных компаундов указывает на универсальность нашего быстрого процесса печати и спекания для производства высококачественных керамических пленок.
Технология PRH также может применяться для изготовления твердотельных батарей со слоистой структурой посредством послойной печати и спекания. Раствор предшественника LiCoO 2 (рис. S19) был напечатан на тонкой, быстро спеченной таблетке LLZTO с последующим спеканием PRH при ~ 800 ° C (из-за низкой температуры реакции) в течение ~ 3 с для синтеза LiCoO in situ. 2 катод. Затем мы покрыли металлический Li-анод с другой стороны таблетки, чтобы сформировать твердотельную батарею LiCoO 2 / LLZTO / Li для езды на велосипеде (рис.5А). Получение изображений поперечного сечения с помощью SEM и EDS (рис. 5, B и C) показывает, что катод LiCoO 2 был равномерно спечен на поверхности LLZTO с конформной и четкой границей раздела. LiCoO 2 , синтезированный методом PRH, также показывает пики XRD, хорошо соответствующие стандартной фазе LiCoO 2 без большого количества вторичной фазы, что указывает на успешный синтез в течение 3-секундного времени спекания (рис. S20). Из-за высокой температуры и короткого времени спекания спеченный LiCoO 2 имеет нанопористую структуру с размером зерна ~ 200 нм (рис.S21) и четко определенный конформный интерфейс без явного перекрестного легирования с гранатом LLZTO (рис. 5C). Чтобы облегчить перенос Li в пористом слое LiCoO 2 и избежать снижения емкости из-за изменения объема катода во время циклирования, мы использовали LiBO 2 в качестве твердотельного связующего, смешанного с катодом LiCoO 2 ( 44 ). Поскольку LiBO 2 может плавиться при ~ 850 ° C, мы непосредственно напечатали и спекали прекурсор LiBO 2 в течение 3 с в пористом слое LiCoO 2 с использованием метода PRH, что привело к однородной структуре композита (рис.5, Г и Д). Затем мы охарактеризовали электрохимические характеристики полученной послойно напечатанной и спеченной твердотельной батареи LiBO 2 -LiCoO 2 / LLZTO / Li.
Рис. 5 Полностью твердотельный аккумулятор LiBO 2 -LiCoO 2 / LLZTO / Li, спеченный методом PRH.( A ) Процесс печати и спекания твердотельной батареи, изготовленной с помощью PRH. ( B ) СЭМ-изображение поперечного сечения и ( C ) EDS-отображение спеченного с помощью PRH катода LiCoO 2 на поверхности LLZTO.( D ) Поперечное сечение и ( E ) увеличенные SEM-изображения интерфейса LiBO 2 -LiCoO 2 / LLZTO. ( F ) Спектры ЭИС твердотельной батареи (LiBO 2 -LiCoO 2 / LLZTO / Li) до цикла и после цикла 450 th . ( G ) Профили напряжения полностью твердотельной батареи, изготовленной на месте, при различных плотностях тока. ( H ) Циклические характеристики и кулоновская эффективность LiBO 2 -LiCoO 2 Полностью твердотельный аккумулятор / LLZTO / Li при 60 ° C.
Из-за конформных интерфейсов межфазное сопротивление этой спеченной PRH батареи было всего лишь ~ 100 Ом · см 2 при 60 ° C (рис. 5F), что значительно меньше, чем у других спеченных совместно спеченных элементов. твердотельные батареи ( 44 — 46 ). Профили напряжения напечатанной батареи показали типичные плато катода LiCoO 2 (рис. 5G), что еще раз демонстрирует успешный синтез LiCoO 2 с помощью метода быстрого PRH.Кроме того, емкость аккумулятора и его характеристики при циклическом использовании демонстрируют хорошее сохранение емкости и отличную стабильность при циклическом использовании в течение ~ 450 циклов (рис. 5H). В частности, начальная удельная емкость составляла ~ 87 мА · час / г при плотности тока 30 мА / г, что лучше, чем в большинстве предыдущих отчетов с использованием совместно спеченного LiCoO 2 и граната ( 37 , 43 , 44 ). Емкость немного уменьшается с увеличением плотности тока, но мало изменяется за циклы при каждой плотности тока (рис.5H). После ~ 450 циклов межфазное сопротивление немного увеличилось до ~ 170 Ом · см 2 (рис. 5F), что дополнительно демонстрирует превосходную стабильность спеченного катода in situ и поверхности раздела, синтезированных методом PRH.
Благодарности: Мы выражаем признательность за поддержку наноцентру Мэриленда, включая его Центр анализа поверхности и AIMLab. Финансирование: Этот проект не финансируется напрямую. Вклад авторов: L.H., C.W. и W.П. разработал эксперименты. W.P. и R.W. проводили эксперименты. З.Л. и J.D. создали трехмерные иллюстрации. L.H., W.P., C.W., Q.D., A.H.B. и J.L. совместно написали статью. Все авторы прокомментировали окончательный вариант рукописи. Конкурирующие интересы: Авторы подали предварительную заявку на патент через Университет Мэриленда (предварительный патент США 62/849578). Авторы заявляют, что у них нет других конкурирующих интересов. Доступность данных и материалов: Все данные, необходимые для оценки выводов в статье, представлены в документе и / или дополнительных материалах.Дополнительные данные, относящиеся к этой статье, могут быть запрошены у авторов.
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Твердотельный литий-серный аккумулятор на основе композитного электрода и двухслойного твердого электролита, работоспособный при комнатной температуре
Мы сообщаем об уникальном твердотельном литий-серном элементе на основе двухслойного электролита и композитного твердотельного катода. Двухслойный электролит, который содержит слой мембраны со смешанной проводимостью и слой полимерного электролита, исключает использование органических легковоспламеняющихся жидких электролитов и сепараторов. Серный электрод также представляет собой уникальный композит серы с ионопроводящими интеркалирующими наночастицами.В отличие от многих других твердотельных батарей, этот элемент может циклически работать при комнатной температуре, чтобы использовать 85% активного материала серного электрода. Низкое внутреннее сопротивление элемента сравнимо с сопротивлением литий-серного элемента на основе жидкого электролита. Исследования импеданса показывают, что низкое внутреннее сопротивление является результатом высокой ионной проводимости интеркалирующих материалов из наночастиц и тонкого слоя полимерного электролита. В то время как изменение объема на катоде приводит к потере контакта между частицами при повторяющихся циклах, добавление оксида алюминия к полимерному слою улучшает сохранение емкости.Эта уникальная конфигурация твердотельных элементов открывает новый путь к более безопасным литиевым батареям высокой энергии.
Это был доклад 270, представленный на заседании Общества в Далласе, штат Техас, 26–30 мая 2019 г.
Литий-серные (Li-S) аккумуляторымогут стать кандидатами в системы накопления энергии следующего поколения для замены литий-ионных аккумуляторов из-за высокой теоретической удельной емкости серного электрода (1672 мАч г -1 ), высокая теоретическая удельная энергия элемента (2600 Вт · ч, −1 ) и относительно низкая стоимость активных материалов. 1–6 Тем не менее, широкое практическое применение Li-S аккумуляторов сдерживается техническими проблемами, которые ограничивают реализацию жизненного цикла аккумуляторов, удельной энергии, плотности энергии и скоростных характеристик. Эти ограничения производительности возникают из-за низкой проводимости активных материалов, изменений объема серного электрода, образования дендритов в литиевом электроде, воспламеняемости органического электролита и эффектов внутреннего перемещения растворимых полисульфидов. 7,8 Органические жидкие электролиты, обычно используемые в Li-S батареях, такие как 1,3-диоксолан (DOL), 1,2-диметоксиметан (DME) и тетрагидрофуран (THF), легко воспламеняются и потенциально опасны, особенно когда батарея эксплуатируется при высоких температурах, с перезарядкой или при любых механических повреждениях. 9 Кроме того, использование органических жидких электролитов приводит к хорошо известному перемещению полисульфидов, включающему растворение, перераспределение и осаждение полисульфидных активных материалов во время цикла, что влияет на обратимость и эффективность батареи. 10–12
Использование твердотельных электролитов (SSE) — привлекательный подход, позволяющий избежать воспламенения жидких электролитов, подавить эффект челнока и подавить рост дендритов лития. 13–16 Соответственно, сообщалось о различных подходах к использованию SSE для Li-S батарей. 17–23 SSE могут быть как неорганическими, так и полимерными. Тем не менее, некоторые из основных проблем, связанных с неорганическими SSE, заключаются в их плохих механических свойствах, таких как хрупкость, плохой межфазный контакт между твердым электродом и твердым электролитом, нестабильность на воздухе и необходимость повышения температуры для достижения приемлемых значений ионной проводимости. 24,25 С другой стороны, полимерные SSE обычно стабильны на воздухе, и присущая им гибкость может снизить межфазное сопротивление твердое / твердое тело и приспособиться к изменениям объема, которые происходят в ячейке. 26 Тем не менее, полимерные SSE обычно не обладают механической прочностью, чтобы остановить рост дендритов, и требуют использования повышенных температур для достижения желаемых значений ионной проводимости. Кроме того, использование SSE требует включения в серный электрод ионопроводящих материалов.Регулировка структуры и состава серного электрода представляет собой сложную задачу, учитывая изолирующую природу серы и объемное расширение, которое происходит во время разряда. Эти ограничения дополнительно предполагают компромисс между достижением высокой плотности энергии и высокой скорости. 27–30 Учитывая преимущества и ограничения обоих типов SSE, гибридный композит полимера и неорганических материалов представляет собой реальную стратегию преодоления проблем, возникающих в Li-S батареях. 31 Есть много отчетов, связанных с использованием двойных слоев SSE в качестве бифункциональных сепараторов для улучшения характеристик Li-S. 32–39 Например, Zhu et al. сообщили о двойном слое SSE, состоящем из серо-углеродных нановолокон и композитного электролита Li 0,33 La 0,557 TiO 3 (LLTO) -поли (этиленоксид) (PEO) с емкостью до 400 мАч г -1 при C / 20. 35 Также Fu et al. сообщили о двухслойном гранатовом SSE с высоким содержанием серы 7 мг / см -2 , достигающим до 600 мАч г -1 . 36
В исследовании, представленном здесь, мы демонстрируем новый смешанный проводник c сложный твердотельный e lectrode / b ilayer solid-state e lectrolyte configuration (CEBE), который направлен на преодоление описанных проблем выше, чтобы реализовать твердотельный Li-S аккумулятор, который может работать при комнатной температуре.
Ячейка состоит из композитного серного электрода, двухслойного твердого электролита и металлического литиевого отрицательного электрода (рис.1). Композитный серный электрод изготовлен из серы, проводящего углерода и материала, интеркалирующего ионы лития, такого как литированный оксид кобальта (LCO). Двухслойный слой состоит из интеркалирующего иона лития слоя и полимерного электролита. Материал с интеркаляцией ионов лития служит твердым электролитом, позволяя легко переносить ионы лития в матрицу активного материала. О введении литиевых интеркалирующих материалов в серный электрод ранее сообщали Чжан и Ма. 40,41 Они обнаружили, что добавление LCO приводит к значительному улучшению скоростных характеристик и стабильности цикла, что связано с быстрой транспортировкой литий-ионов и подавлением челночного перемещения. Концепция использования интеркалирующего материала в качестве электролита также основана на нашей предыдущей работе с Li-S батареей, где мы продемонстрировали интеркалирующую мембрану со смешанной проводимостью (MCM), которая позволяет исключительно транспортировать ионы лития и подавляет полисульфидный челнок. 42 Вкратце, литий-ионный интеркалирующий материал проводит ионы лития, когда происходит реакция интеркаляции. Ионы лития диффундируют через основную часть материала, выполняя функцию ионного проводника. Электронная проводимость материала позволяет эффективно протекать электрохимической реакции интеркаляции и сопутствующей диффузии ионов лития.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 1. Схематическое изображение литий-серной батареи с твердым композитным электродом и двухслойным электролитом.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияМы решили использовать LCO в качестве интеркалирующего материала, потому что окно равновесного потенциала для интеркаляции положительно по отношению к полностью заряженному серному электроду (> 2,7 В против Li / Li + ). В этих условиях серный электрод может быть полностью заряжен, при этом LCO не принимает на себя никакого заряда.Кроме того, мы выбрали LCO «наночастицы», чтобы увеличить площадь поверхности межфазной реакции с частицами серы в катоде. Важно отметить, что жидкий электролит в ячейку не добавлялся, и мы полагались на ионную проводимость LCO для транспортировки ионов лития в катод и из катода.
«Двухслойный твердый электролит» состоит из 30-микронного слоя LCO (также называемого здесь далее мембраной со смешанной проводимостью или MCM), покрытого 10-30-микронным слоем полимерного электролита.Полимерный электролит состоит из полиэтиленоксида, смешанного с солью LiTFSI. Слой полимерного электролита находится в прямом контакте с литиевым электродом, где он служит литий-ионным проводником и разделителем для предотвращения внутреннего электронного короткого замыкания.
Конфигурация двухслойного электролита использует преимущества литий-ионных механизмов внедрения и извлечения в интеркалирующем материале слоя MCM. По сравнению с использованием обычных твердых электролитов, которые обладают только ионной проводимостью, использование литий-ионного интеркалирующего материала в качестве твердого электролита имеет три основных преимущества: 1) он имеет относительно быструю проводимость иона лития 2) он транспортирует исключительно ионы лития и 3) он не вносит значительного вклада в общее сопротивление клетки.Например, литированный оксид кобальта (LiCoO 2 ) имеет электронную проводимость 43,44 , равную 1 × 10 −3 См · см −1 , и коэффициент самодиффузии ионов лития 45 из 2 × 10 −9 см 2 с −1 . Следовательно, легкая диффузия ионов объясняется реакцией интеркаляции и самодиффузией ионов с процессом переноса ионов, управляемым электрическим полем через слой MCM, которое создается во время заряда и разряда.Слой MCM между композитным катодом и полимерным электролитом является важным компонентом ячейки, поскольку он устанавливает путь для переноса ионов между катодом и полимерным электролитом. Кроме того, MCM обладает хорошими механическими свойствами (прочными и гибкими) и, таким образом, служит подложкой для покрытия тонкого слоя полимерного электролита с образованием двухслойного твердого электролита. Полимерное покрытие соответствует MCM, обеспечивая хороший физический контакт, позволяющий использовать тонкие слои полимерного электролита.Использование тонкого слоя полимерного электролита важно для снижения общего внутреннего сопротивления ячейки, предотвращения короткого замыкания между анодом и катодом и повышения производительности при комнатной температуре.
Одним из ключевых преимуществ предлагаемой конфигурации композитный двухслойный электрод является отсутствие горючих органических электролитов. Кроме того, Li-S элементы с жидким электролитом представляют собой процесс саморазряда, который в основном объясняется потерей активного материала с катода из-за эффекта полисульфидного челнока, когда сера растворяется в электролите с образованием полисульфидов высокого порядка, которые имеют тенденцию к диффузии. к литиевому электроду, уменьшая емкость ячейки. 46,47 Использование твердого электролита позволяет избежать эффекта челнока, поскольку активные материалы остаются в композитном электроде в виде твердых частиц. Кроме того, включение слоя полимерного электролита, который является относительно стабильным во времени, предотвращает любой перенос материалов. 48 Кроме того, бислой потенциально может блокировать рост дендритов лития во время повторяющихся циклов. 49,50 Мы показываем, что элементы можно циклировать при комнатной температуре, что доказывает преимущество использования интеркалирующих катодных материалов в качестве ионных проводников.С производственной точки зрения двухслойный слой является гибким, устойчивым к воздуху и может быть разрезан на любую желаемую форму, что позволяет создать гибкую Li-S батарею без жидкого органического электролита. С точки зрения серного электрода использование интеркалирующих частиц в качестве твердого электролита решает проблемы, связанные с распределением и проникновением электролита, которые являются преобладающими проблемами при использовании толстых электродов с жидкими электролитами. Это равномерное распределение твердого электролита и отсутствие разделителей в ячейке открывает возможность создания Li-S батарей с высокой плотностью энергии.Кроме того, в слой полимерного электролита можно добавлять неорганические наполнители для повышения его ионной проводимости и модуля сдвига. В качестве примера мы добавили оксид алюминия в виде наночастиц в слой полимерного электролита, который улучшает ионную проводимость и снижает поляризацию во время работы. В сумме компоненты экспериментальной версии Li-S элемента CEBE дают удельную энергию 70,7 Вт · ч · кг -1 (Таблица I). Это значение плотности энергии может быть значительно увеличено за счет уменьшения толщины бислоев в пять-шесть раз и трехкратного уменьшения доли материала наночастиц в катоде.Однако мы не сосредоточились на демонстрации этих улучшений в этой работе. Наконец, двухслойная композитная конфигурация дает низкое внутреннее сопротивление по сравнению с другими твердотельными подходами из-за смешанной проводимости интеркалирующих материалов и использования очень тонких слоев полимерного электролита.
Таблица I. Удельная энергия на уровне элемента для элемента CEBE Li-S.
| Катод | Электролит | Анод | Масса катода (мг) | Загрузка серы (мг) | Масса твердого электролита (мг) | Масса анода (мг) | Емкость (мАч г −1 ) | Среднее напряжение (В) | Удельная энергия (Втч кг −1 ) |
|---|---|---|---|---|---|---|---|---|---|
| Сера | LiCoO 2 / PEO-Al 2 O 3 (двухслойный) | Li | 14.4 | 2,6 | 39,86 | 46 | 1481 | 1,84 | 70,7 |
Приготовление композитного серного электрода
Смесь серы (Aldrich, чистота 99,5%) с черным Ketjen (KB, Akzo Nobel EC-600JD) в массовом соотношении 72:28 была приготовлена путем настаивания расплава при 155 ° C для 12 ч. Приготовили суспензию смеси сера-KB, порошка оксида лития-кобальта (чистота Alfa Chemistry 99,9%, средний размер частиц <100 нм) и связующего на основе поливинилиденфторида (ПВДФ) (MTI) в массовом соотношении 60: 33: 7. в растворителе N-метил-2-пирролидон (NMP) (безводный, 99.5%, Олдрич). Полученную суспензию перемешивали в течение ночи и наносили на алюминиевую фольгу с помощью ракельного ножа и частично сушили в вакуумной печи при 70 ° C в течение 2 часов. Электрод был разрезан на диски по 2 см 2 . Любой остаточный растворитель удаляли промокательной салфеткой до того, как пленка начинала трескаться, оставив 10-15 мкл NMP перед сборкой (объем измеряли по разнице веса высушенного электрода и с использованием плотности NMP). Мы не позволяли растворителю полностью испариться, чтобы избежать растрескивания электродной пленки и обеспечить хороший контакт твердой / твердой границы раздела фаз за счет адгезии между композитным электродом и двухслойным электролитом.Контрольные электроды были приготовлены таким же образом, как сера была расплавлена в Ketjen Black (KB) в массовом соотношении 75:25. Затем была приготовлена суспензия из смеси серы-KB, угля Super P и связующего PVDF в массовом соотношении 80:10:10, растворенных в NMP. Суспензию покрывали с помощью ракельного ножа и сушили в вакуумной печи при 70 ° C в течение ночи. Конечная концентрация серы для всех электродов составляла от 1,2 до 1,7 мг / см -2 .
Приготовление двухслойного твердого электролита
Литированный оксид кобальта (Aldrich, оксид лития-кобальта (III), молекулярная формула LiCoO 2, 99.8% на основе следов металлов) и ПВДФ в соотношении 95: 5 по массе, соответственно, превращали в суспензию с NMP. Суспензию наносили на алюминиевую фольгу с помощью ракельного ножа, испытывали разную толщину в диапазоне от 30 до 80 микрометров, и покрытие сушили в вакуумной печи при 70 ° C в течение ночи. Затем алюминиевую фольгу с покрытием прессовали в горячем прессе при 140 ° C и давлении 0,5 кг / см -2 .
Раствор получали растворением соли поли (этиленоксида) (PEO, Aldrich, MW 300000) и бис (трифторметансульфонил) имида (LiTFSI, Aldrich) в молярном соотношении 8: 1 в тетрагидрофуране (HPLC, ≥99.9%). Раствор полимера наносили на спрессованный слой литированного оксида кобальта с помощью ракельного ножа до толщины, которая находилась в диапазоне от 10 до 30 мкм мкм. Полученный бислой сушили в вакууме при 40 ° C в течение ночи и перфорировали на 2 см 2 дисков. Затем подложку из алюминиевой фольги снимали, получая отдельно стоящий бислой из литированного оксида кобальта и ПЭО. Загрузка LCO составляла приблизительно 15,5 мг / см -2 . Слой полимерного электролита с оксидом алюминия был приготовлен по той же методике, что и выше, за исключением того, что раствор содержал порошок оксида алюминия (Aldrich, нанопорошок, размер частиц <50 нм), который составлял 10 мас.% От массы ПЭО и LiTFSI, все растворенных в тетрагидрофуране ( Степень чистоты для ВЭЖХ ≥99.9%).
Изготовление монетных ячеек
Монетные ячейки типа 2032 с алюминиевыми банками (MTI) были собраны в перчаточном боксе, заполненном аргоном (MTI, менее 2 ppm влаги) с использованием композитных дисковых электродов в качестве положительного электрода. и литиевая фольга (MTI) в качестве противоэлектрода. Двухслойный слой помещали между электродами, где сторона полимерного электролита бислоя контактировала с литиевым электродом, а сторона MCM, содержащая LCO, обращена к композитному электроду.Никакого сепаратора или жидкого электролита не добавляли.
Контрольные элементы с жидким электролитом были собраны с использованием литиевой фольги в качестве отрицательного электрода, полипропилена (Celgard 2500) в качестве пористого сепаратора и контрольных электродов Sulphur-KB-Super P-PVDF, описанных в предыдущем разделе. Жидкий электролит представлял собой 1 М бис (трифторметансульфонил) имид лития (LiTFSI, Aldrich), растворенный в смеси 1: 1 (по объему) диоксолана и диметоксиэтана (Aldrich). Количество электролита составило 20 мкл л на 1 мг серы.
Электрохимическая характеристика
Цикл гальваностатического заряда / разряда плоских элементов был проведен с использованием испытательной станции для батарей BST8-MA (MTI) и потенциостата PAR VMC-4 при комнатной температуре (23 ° C). Клетки подвергались циклам при скоростях C / 50, C / 30, C / 20, C / 14 и C / 8, где 1C соответствовал 1675 мАг -1 . Зарядка прекращалась при 2,8 В относительно Li / Li + , в то время как разряд отключался при 1,4 В. Измерения спектроскопии электрохимического импеданса (EIS) проводили с использованием потенциостата / анализатора импеданса PAR VMC-4.Отклик EIS был измерен в диапазоне частот от 0,01 Гц до 100 кГц и при синусоидальной амплитуде возбуждения ± 3 мВ (от пика до пика). Импедансный отклик анализировали с помощью программного обеспечения ZSimpWin.
Сканирующая электронная микроскопия (SEM)
Двухслойный слой замораживали в жидком азоте и затем разрушали. Поперечное сечение получали с помощью сканирующей электронной микроскопии (SEM, JEOL 661 SEM).
Двухслойный электролит
На рис. 2а показана фотография бислоя после покрытия MCM электролитом на основе ПЭО.На микрофотографии поперечного сечения (рис. 2b) мы можем наблюдать плотно упакованные частицы LCO с приблизительной толщиной 80 микрометров, покрытые однородным тонким слоем PEO-LiTFSI толщиной около 30 микрометров.
Увеличить Уменьшить Сбросить размер изображения
Рис. 2. (a) MCM, покрытый PEO, пример двухслойного твердого электролита. (б) Изображение двойного слоя, полученное с помощью сканирующей электронной микроскопии.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияПрофиль разряда и импедансная характеристика элемента CEBE Li-S
Профиль разряда в состоянии равновесия элемента CEBE Li-S представляет собой небольшое плато, за которым следует наклонная область относительно низкой емкости, а затем более продолжительное плато (рис. 3a) . Область между 2,6 В и 2,5 В была связана с образованием полисульфидов высокого порядка, а вторая часть, начиная с 2,05 В по сравнению с Li / Li + , связана с превращением серы в полисульфиды низкого порядка.Наличие первой области объясняется разделением фаз между серой и полисульфидами более высокого порядка. Второе более широкое плато с более низким напряжением было связано с восстановлением и разделением фаз на Li 2 S 2 и Li 2 S. Наблюдаемый профиль разряда аналогичен описанному для других квазитвердотельных литий-серных батарей. . 51–53 Отметим, что напряжение первой части разряда примерно на 300 мВ выше, чем у типичного Li-S элемента с жидким электролитом (рис.3а). Кроме того, второе плато напряжения Li-S ячейки CEBE при 2,1 В ниже, чем у ячейки с жидким электролитом, примерно на 50–100 мВ. Мы связываем эти различия в напряжении ячейки с различиями в активности и растворимости окислительно-восстановительных материалов в ячейке с жидким электролитом по сравнению с твердотельной ячейкой.
Увеличить Уменьшить Сбросить размер изображения
Рис. 3. (a) Сравнение кривой разряда при C / 60 между элементом CEBE Li-S и элементом Li-S с жидким электролитом во время первого цикла.(b) Трехмерное представление отклика импеданса, полученного на графиках Найквиста, как функция состояния заряда для Li-S-элемента с жидким электролитом и (c) для Li-S-элемента CEBE. (d) Предложены эквивалентные схемы для описания Li-S элементов Liquid и CEBE.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияИмпедансная характеристика (графики Найквиста) как функция состояния заряда (SOC) для жидкой ячейки (рис. 3b) может быть развернута в две полукруглые дуги в начале процесса разряда.Ниже 60% SOC полукруг на высокой частоте сменяется одиночным полукругом и наклонной линией. Это изменение импедансной характеристики может быть связано с осаждением растворимых полисульфидов в высоких состояниях заряда с образованием полисульфидов более низкого порядка. Эта конкретная эволюция импедансной характеристики с SOC соответствует ранее описанной EIS-характеристике Li-S жидкостной ячейки. 54,55 Для жидкостной ячейки мы предлагаем использовать две электрические эквивалентные схемы для анализа импеданса как функции SOC (рис.3d). Схема 1 используется для описания области перед вторым плато, где происходит восстановление серы и растворение полисульфидов высокого порядка. Цепь 1 состоит из R 0 , омического сопротивления электрода и электролита, R 2 , межфазного контактного сопротивления, связанного с электронной проводимостью между токосъемником (углеродом, алюминием) и массой активного материала (согласно Deng и др. 54 ), CPE 2 , емкость объема серного электрода, R 1 , сопротивление переносу заряда электрохимической реакции, CPE 1 , емкость двойного слоя электрода и W o сопротивление массового транспорта.С другой стороны, контур 2 состоит только из R 0 , омического сопротивления, R 1 , сопротивления переноса заряда, CPE 1 , емкости двойного слоя электрода и W o , импеданса Варбурга. . Цепь 1 преобразуется в Цепь 2, когда значение R 2 становится равным нулю. Проанализировав данные импеданса с использованием схемы 1, мы заметили, что R 2 становится пренебрежимо низким ниже 60% SOC (рис. 4a). Это изменение значения R 2 связано с полным преобразованием серы в растворимые полисульфиды, которые диффундируют из электрода.Таким образом, больше нет сопротивления, связанного с межфазным контактом между активным материалом и токосъемником. Это преобразование заметно, когда разряд проводится с очень низкой скоростью C / 60. В этих условиях полисульфиды могут свободно диффундировать в объем электролита и по направлению к аноду, обеспечивая полное растворение полисульфидов, избегая образования осадка на катоде.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 4. (a) Изменение внутреннего сопротивления в зависимости от степени заряда для жидкого Li-S элемента. (b) Изменение внутреннего сопротивления в зависимости от состояния заряда для элемента CEBE Li-S.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияНа графике Найквиста ячейки CEBE Li-S мы находим один полукруг и наклонную линию (рис. 3c). Вначале отметим, что общее сопротивление элемента CEBE Li-S ниже, чем у элемента с жидкостью.Импеданс элементов CEBE-Li-S может быть смоделирован с помощью схемы 2 (рис. 3d), как описано на этапе осаждения ячейки с жидким электролитом. Отсутствие двух полукругов во время процесса разряда в Li-S-элементе CEBE предполагает, что межфазное сопротивление между активным материалом и токосъемником незначительно, и что наночастицы интеркаляционных материалов в катоде обеспечивают достаточную электрическую проводимость между различные фазы. Значение R 0 сравнимо со значением, наблюдаемым в ячейке с жидким электролитом, подтверждая, что двухслойный электролит и структура катода имеют сравнимую проводимость с ячейкой с жидким электролитом.Однако мы действительно наблюдаем, что сопротивление элемента уменьшается и в небольшой степени увеличивается во время процесса разряда. На рисунке 4b показано изменение R 0 и R 1 в зависимости от SOC для элемента CEBE Li-S. Изменение сопротивления переносу заряда с помощью SOC согласуется с предыдущими отчетами, предполагающими, что полисульфиды низкого порядка обладают более высоким сопротивлением переносу заряда по сравнению с полисульфидами более высокого порядка. 56 Мы также наблюдаем, что величина сопротивления переносу заряда R 1 ниже для элемента CEBE Li-S по сравнению с элементом жидкого Li-S, что также связано с большой площадью поверхности раздела, обеспечиваемой интеркаляционным материалом из наночастиц. .В отличие от Li-S элемента CEBE, общее сопротивление жидкого элемента уменьшается с увеличением SOC (рис. 3b и 4a). Последнее объясняется растворением и диффузией полисульфидов более высокого порядка по направлению к аноду (особенно при низких скоростях). Таким образом, результаты импеданса подтверждают, что способность элемента CEBE Li-S работать при комнатной температуре обусловлена низким межфазным сопротивлением и высокой проводимостью двухслойного электролита.
Эффект гальваностатического цикла
Li-S элементы CEBE циклически включались при комнатной температуре между 2.8 В и 1,4 В с разной скоростью. При C / 20 элемент показал высокую удельную емкость 1445 мАч g -1 во время первого разряда, демонстрируя, что использование серы составило почти 85% (рис. 5a). 1С соответствовал току 1675 мА g −1 . Замечательная удельная емкость твердотельной Li-S батареи при комнатной температуре объясняется быстрым переносом ионов в катоде, чему способствует интеркалированный материал с высоким коэффициентом диффузии ионов лития. Ячейку можно было многократно включать в цикл со скоростью C / 20, и емкость постепенно уменьшалась, при этом примерно 63% емкости (1050 мАч g -1 ) сохранялось даже после четвертого цикла.Результаты заряда / разряда для скоростей C / 20 и C / 8 показаны на рис. 5а и 5б соответственно. Когда элементы циклировались со скоростью C / 8, можно было использовать около 50% емкости серного электрода (820 мАч г -1 ), все еще значительную часть емкости катода. Однако уменьшение емкости с C / 20 до C / 8 предполагает, что диффузия ионов лития ограничивает скорость. Для сравнения, элементы с жидким электролитом при разряде при C / 20 давали только 54% от теоретической емкости (906 мАч g -1 ).Использование в ячейке с жидким электролитом сильно зависит от скорости, отношения серы к углероду, пористости и доступной площади поверхности из-за осаждения и зародышеобразования нерастворимых полисульфидов. Напротив, на клетки CEBE процессы преципитации и зародышеобразования не так сильно влияют из-за отсутствия растворимых видов. Кроме того, наночастицы увеличивают доступную площадь поверхности, увеличивая пористость электрода и создавая иерархическую структуру пор с помощью Ketjen Black.
Увеличить Уменьшить Сбросить размер изображения
Рис. 5. (a) Кривые гальваностатического заряда / разряда батареи CEBE Li-S для первого и четвертого цикла при скорости C / 20 (1C = 1675 мА g −1 ). (b) Кривые гальваностатического заряда / разряда батареи CEBE Li-S для первого и второго цикла при C / 8.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияМы обнаружили, что повторяющиеся циклы приводят к постоянной потере мощности в каждом цикле.После восьми циклов при комнатной температуре со скоростью C / 20 сохранилось около 15% емкости первого цикла (рис. 7a). Мы объясняем эту потерю емкости результатом увеличения объема на 79%, которое происходит во время разряда катода, когда сера превращается в дисульфид лития. Расширение и сжатие, происходящие во время повторяющихся циклов, могут вызвать потерю контакта между слоями, а также между частицами в катоде. Такие изменения объема будут иметь тенденцию влиять на все традиционные ячейки с твердым электролитом в большей степени, чем ячейки с жидким электролитом, из-за неспособности обычных ячеек с твердым электролитом с жесткими конструкциями приспособиться к изменениям объема.Если мы сможем повысить сопротивляемость катодного слоя и электролита, можно будет достичь более длительного срока службы. Данные по импедансу ячейки предполагают, что контакты между частицами теряются при циклировании, что приводит к примерно 350-кратному увеличению сопротивления переносу заряда (рис. 6). Однако при использовании композитного двухслойного типа ячейки с твердым электролитом слой полимерного электролита потенциально может буферизовать изменения за счет упругой деформации.
Увеличить Уменьшить Сбросить размер изображения
Рисунок 6. Сравнение импедансной характеристики элемента CEBE Li-S до цикла (показано кружками) и после восьми циклов (показано квадратами).
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияБлагоприятные эффекты добавления оксида алюминия к слою полимерного электролита
Мы обнаружили, что слой полимерного электролита не имеет такой же механической прочности, как слой MCM. Таким образом, слой полимерного электролита мог необратимо деформироваться при изменении объема, сопровождающем циклирование.В литературных источниках предполагается, что добавление оксида алюминия в качестве неорганического наполнителя в ПЭО увеличивало механическую прочность и улучшало ионную проводимость. 32,57,58 Упрочнение было вызвано адгезией наполнителя к макромолекулярным цепям, что привело к иммобилизации полимерных цепей. . 57,59 Сообщалось, что твердотельные полимерные электролиты при контакте с литием имеют тенденцию образовывать стабильные границы раздела фаз. 60,61 Кроме того, использование неорганических наполнителей в слое полимерного электролита в виде Al 2 O 3 снижает межфазное сопротивление на литиевом электроде. 62,63 Кроме того, сообщалось, что 10 мас.% Al 2 O 3 может повысить ионную проводимость 64 от 1 × 10 –8 до 1 × 10 –5 См см –1 при 30 ° C. Поэтому мы диспергировали наночастицы оксида алюминия (10 мас.%) В суспензии полимерного электролита, а затем наносили ее на слой MCM. Ячейки CEBE Li-S с двухслойным слоем MCM / PEO-LiTFSI-Al 2 O 3 были циклированы при C / 20 между 2.8 В и 1,4 В при комнатной температуре. Ячейка CEBE-Al 2 O 3 Li-S при разряде со скоростью C / 20 достигла почти 88% (1481 мАч г -1 ) от теоретической емкости (рис. 7a), как и у элементов. который не содержал оксида алюминия в полимерном электролите. Однако даже после восьми циклов (рис. 7b) ячейка с оксидом алюминия, содержащим ПЭО, сохранила 60% емкости первого цикла (901 мАч г -1 ), примерно в 5 раз большую емкость по сравнению с ячейками без оксида алюминия.Эти результаты позволяют предположить, что слой полимерного электролита можно укрепить, чтобы уменьшить некоторые потери емкости.
Увеличить Уменьшить Сбросить размер изображения
Рис. 7. (a) Сравнение графика зависимости удельной емкости от числа циклов между элементом CEBE Li-S с двухслойным слоем из MCM / PEO-LiTFSI на C / 20 (показано квадратами) и элементом CEBE Li-S с двухслойным слоем из MCM / PEO-LiTFSI-Al 2 O 3 при C / 20 (изображены кружками) (b) Кривые гальваностатического заряда / разряда для элемента CEBE Li-S с двухслойным слоем из MCM / PEO-LiTFSI-Al 2 O 3 для первого и восьмого цикла при C / 20.
Загрузить рисунок:
Стандартное изображение Изображение высокого разрешенияМы представили уникальный твердотельный литий-серный элемент на основе гибкого бислоя из литий-ионного интеркаляционного материала и полимерного электролита. Несмотря на то, что он является твердотельным элементом, его можно заряжать и разряжать при комнатной температуре при C / 20, чтобы получить до 85% от теоретической емкости. Твердотельный элемент и двухслойный элемент исключают использование легковоспламеняющихся электролитов и устраняют проблему переноса полисульфидов через элемент.Двухслойный слой является гибким, его легко изготовить, и ему можно придать любую форму ячейки, в отличие от многих обычных твердотельных ячеек. Твердотельная двухслойная конфигурация приводит к более низкому сопротивлению по сравнению с ячейкой с жидким электролитом из-за высокопроводящей мембраны со смешанной проводимостью и тонкого слоя полимерного электролита. Добавление наночастиц интеркаляционных материалов в серный электрод обеспечивает хорошее использование активных материалов даже при скорости C / 8, дающей> 50% теоретической емкости.Способность поддерживать такие высокие скорости, как C / 8, объясняется быстрым переносом ионов лития и большой межфазной площадью, обеспечиваемой интеркалирующим материалом в виде наночастиц. Повторяющееся переключение этих ячеек приводит к потере емкости из-за неспособности ячейки выдерживать большие изменения объема, сопровождающие разряд на серном электроде, что приводит к потере контакта между частицами. Добавление неорганических наполнителей, таких как оксид алюминия, в слой полимерного электролита снижает скорость потери емкости, доказывая, что слой электролита также должен быть механически прочным.Композитные электроды, которые могут упруго деформироваться, чтобы приспособиться к изменениям объема твердотельного катода, потребуются для решения проблемы снижения емкости. То, что представлено здесь, является доказательством концепции нового подхода, и потребуются дополнительные усилия для оптимизации состава серного электрода за счет увеличения поверхностной нагрузки активного материала для достижения ячеек с более высокой плотностью энергии. Альтернативные смешанные проводники, которые будут обеспечивать не только быстрый перенос ионов, но и емкость катода, будут полезны для сохранения высокой плотности энергии литий-серных элементов.Представленные здесь результаты демонстрируют, что архитектура композитный электрод / двухслойный электролит — это новый путь для дальнейшего развития литий-серных твердотельных батарей.
Авторы выражают признательность за финансовую поддержку этого исследования проекту CERDEC армии США (GTS-S-17-355) «Носимая, эффективная и высокоэнергетическая перезаряжаемая литий-серная батарея», Исследовательского института углеводородов Локера, Центрального центра. передового опыта в области наноизображения и химического факультета Университета Южной Калифорнии.
Границы | Последние достижения в области электролитов для цинково-воздушных батарей
Введение
БатареяZn – air имеет высокую удельную энергию (1,218 Втч · кг, –1 ). Между тем, присущие ему особенности, в том числе безопасность и низкая стоимость, делают его одним из самых многообещающих аккумуляторов следующего поколения (Fu et al., 2017; Tan et al., 2017; Han et al., 2019). Роль электролитов упускается из виду по сравнению с горячими исследованиями бифункциональных воздушных электродов для Zn-воздушных батарей. Характеристики электролитов напрямую определяют ионную проводимость и межфазные свойства Zn-воздушной батареи в процессе эксплуатации.Кроме того, это дополнительно влияет на емкость, стабильность при циклическом режиме, а также эффективность зарядки и разрядки элемента (Pei et al., 2014). Zn-воздушные батареи развиваются в направлении высокой эффективности и долговечности, которые невозможно отделить от поддержки электролита с превосходными характеристиками во всех аспектах (R. Mainar et al., 2016). Таким образом, очень важно углубиться в изучение работы электролитов в Zn-воздушных батареях (Mainar et al., 2018).
В настоящее время щелочной электролит все еще широко используется в батареях на основе цинка для удовлетворения требований низкой стоимости и высокой ионной проводимости и обеспечения стабильности цинкового электрода (R.Mainar et al., 2016; Сюй и др., 2020). Однако он чувствителен к воздействию CO 2 окружающей среды и относительной влажности. Zn-воздушная батарея в основном зависит от характеристик воздушного электрода. К сожалению, CO 2 может привести к образованию в электролите K 2 CO 3 , что отрицательно влияет на пустоту в воздушном электроде (Wang et al., 2014; Fu et al., 2017). Zn – воздушные батареи должны решать проблему испарения электролита или поглощения воды из внешней среды, чтобы хорошо работать в сложной внешней среде.Первый заставляет батарею расширяться, а второй влияет на перенос OH — (Chakkaravarthy et al., 1981; Mainar et al., 2018). Ионные жидкости комнатной температуры (RTIL) и твердые электролиты являются альтернативными и эффективными решениями для решения вышеуказанной проблемы. Однако их производительность была ограничена их низкой ионной проводимостью и неквалифицированным интерфейсом. Поэтому в следующих частях мы обсудим статус исследования щелочных электролитов и неводных электролитов в Zn-воздушных батареях.
Водный электролит
LiOH, NaOH и KOH — обычные электролиты для Zn-воздушных аккумуляторов. По сравнению с нейтральными и кислотными электролитами щелочные электролиты хорошо сочетаются с цинковыми электродами и материалами катализатора. Между тем, электролит КОН обладает высокой ионной проводимостью и низкой вязкостью. Когда Zn-воздушная батарея разряжается, внешний кислород входит в батарею и реагирует (Уравнение 1) (реакция восстановления кислорода) на границе раздела газ-жидкость-твердое тело (кислород, электролит, электрокатализатор).Цинковый электрод переносит электроны к воздушному электроду через внешнюю нагрузку, а OH — в месте реакции генерирует Zn (OH) 42- (уравнение 2). Когда концентрация Zn (OH) 42- достигает максимума, он далее разлагается на ZnO (уравнение 3). Полная реакция цинкового электрода показана в уравнении 4. Во время процесса зарядки происходит обратная реакция (уравнение 1) (реакция выделения кислорода) на границе раздела цинк-электролит, и электрическая энергия накапливается, в то время как цинк осаждается в результате обратной реакции. (Уравнение 3).
O2 + 2h3O + 4e-↔4OH-E = 0,40 В по сравнению с SHE (1) Zn + 4OH-↔Zn (OH) 42- + 2e-E = 1,26 В по сравнению с SHE (2) Zn (OH) 42-↔ZnO + h3O + 2OH- (3) Zn + 2OH-↔ZnO + h3O + 2e-E = 1,26 В по сравнению с SHE (4)Когда концентрация КОН составляет 6 М, плотность обмена током Zn / Zn 2+ достигает 0,21 А · см -2 , а растворимость ZnO увеличивается с увеличением концентрации КОН (See and White, 1997; Dyer и др., 2009). Поэтому необходимо обращать внимание на неблагоприятное влияние электролита КОН с высокой концентрацией на цинковый электрод.Высокая концентрация ZnO производит избыток Zn (OH) 42- и осаждается после разряда, что увеличивает пассивирующее сопротивление цинкового электрода. Кроме того, кинетические параметры восстановления кислорода цинка были очень высокими, что приводило к растворению, миграции и переотложению цинка в различных условиях (R. Mainar et al., 2016).
Есть две основные стратегии решения этой проблемы. Один заключается в изменении состава и структуры цинкового электрода, а другой — в поиске подходящих добавок к электролиту.Известные методы, такие как создание трехмерной структуры цинкового электрода (Parker et al., 2014; Chamoun et al., 2015; Yan et al., 2015) или эффективная добавка для цинкового электрода (Fan et al., 2013; Masri and Mohamad, 2013; Huang et al., 2015) оказались эффективной стратегией решения. Актуальной задачей является точное измерение потенциала и концентрации ионов цинка на поверхности цинкового электрода, чтобы обеспечить адекватную теоретическую поддержку для улучшения условий жизни цинкового электрода в щелочном электролите.В таблице 1 мы суммировали последние работы по добавкам щелочных электролитов. Подходящие добавки в электролиты могут улучшить изменение формы цинкового электрода и производительность Zn-воздушной батареи. Если мы сможем снизить концентрацию КОН, насколько это возможно, не влияя на ионную проводимость электролита, мы полагаем, что производительность Zn-воздушной батареи будет еще больше улучшена. Добавляя K 2 CO 3 к высококонцентрированному раствору KOH и оптимизируя структуру батареи, Schröder et al.(2015) не только получили стабильный электрический потенциал, но также улучшили фактическую плотность энергии и долгосрочную стабильность Zn-воздушной батареи. Кроме того, ингибирование роста дендритов и выделения водорода из цинкового электрода также зарегистрировано в Zn-воздушной батарее с щелочными электролитами, использующими додецилбензолсульфонат натрия (SDBS) (Yang et al., 2004), полиэтиленгликоль (PEG) (Banik and Akolkar). , 2013), винной / янтарной / лимонной кислотами (Lee et al., 2006) и гидроксидами тетраалкиламмония (Lan et al., 2007).
Таблица 1 . Краткое изложение недавно опубликованной добавки к щелочному электролиту для Zn-воздушных батарей.
Zn – air аккумулятор представляет собой полуоткрытую систему, которой для участия в процессе реакции требуется богатый кислород из внешней среды. Углекислый газ (CO 2 ) трудно избежать во влажной атмосфере. CO 2 из внешней атмосферы попадает в батарею через воздушный электрод и реагирует с OH — в электролите (уравнения 5, 6).
СО2 + ОН- → HCO3- (5) HCO3− + OH − ↔CO32− + h3O (6)Ионная проводимость электролита ослабляется из-за образования HCO3- и CO32- и низкой растворимости K 2 CO 3 и KHCO 3 . Когда они осаждаются на воздушном электроде, перенос кислорода будет до некоторой степени заблокирован, что приведет к снижению производительности Zn-воздушной батареи. Оптимизация структуры Zn-воздушной батареи и состава слоя адсорбции газа, чтобы позволить кислороду проходить беспрепятственно, но препятствовать прохождению диоксида углерода и водяного пара, является идеальным решением.Для решения вышеуказанных проблем исследователи также предложили несколько решений. Pedicini et al. (1996) создали систему управления воздухом для рециркуляции реагирующего воздуха в металл-воздушной батарее. Goldstein et al. (1997) предложили скрубберную систему для удаления диоксида углерода из металл-воздушной батареи или батареи топливных элементов. Педикни (2002) предложил ограничивать выбросы углекислого газа и водяного пара, когда батарея не используется, путем загрузки воздушной заслонки для электрохимического элемента. Есть много решений для решения этих проблем, но ограничениями являются пороговые значения высокой стоимости и ограниченное использование пространства, что ограничивает развитие Zn-воздушных батарей в практических приложениях.
Система проточного электролита — очень эффективный метод для Zn-воздушных батарей. Электролит перекачивается и циркулирует через систему питания внешних труб и насосов. В дополнение к удалению осажденного карбоната и других побочных продуктов через внешние фильтры проточный электролит улучшает перенос OH — и снижает градиенты концентрации (Iacovangelo and Will, 1985; Cheng et al., 2007). По сравнению со статическим электролитом, Zn-воздушная батарея значительно улучшена, включая срок службы и рабочее напряжение с системой циркуляции электролита.Однако мощность циркуляции электролита должна поддерживаться внешней системой откачки и электрической энергией. Следовательно, если система циркуляции электролита применяется на практике, необходимо решить проблему, которую трудно применить к крупномасштабной сетевой системе хранения энергии со строгими требованиями к пространству и весу.
Ионная жидкость комнатной температуры
Ионная жидкость комнатной температуры представляет собой расплавленную соль, которая существует в виде жидкости при комнатной температуре или ниже.Он имеет широкое электрохимическое окно и нелегко воспламеняется (Balaish et al., 2014). Поэтому все больше внимания уделяется RTIL как заменителю щелочных электролитов. Внутренняя безопасность и стабильность RTIL в широком диапазоне электрохимических потенциалов привели к его применению в литиевых батареях (Chou et al., 2008; Xiang et al., 2010). Использование RTIL в Zn-воздушных батареях может эффективно решить проблемы повреждения цинкового электрода (Simons et al., 2012), повреждения CO 2 и испарения электролита (Harting et al., 2012) в щелочном электролите водяной системы, упомянутой выше, и позволяют батарее работать при высоких температурах. Более того, для апротонных RTIL отсутствие протонов может эффективно избежать коррозии цинкового электрода, вызванной выделением водорода. Поэтому RTIL как электролит для Zn-воздушных аккумуляторов в последние годы попали в список.
RTIL, используемые в качестве электролита для Zn-воздушной ячейки, цинк окисляется до Zn 2+ во время разряда, и обратимая электрохимическая реакция цинка в RTIL оказалась возможной (Xu et al., 2015). Здесь необходимо отметить, что неподходящие RTIL могут образовывать нерастворимые вещества с Zn 2+ и делать их неспособными эффективно восстанавливаться. Предложен механизм воздушного электрода в электролите RTIL (Kar et al., 2014).
Когда в электролите RTIL происходит восстановление кислорода, кислород приобретает электроны и образует супероксид (O2 · -) (уравнение 7). Эта реакция считается квазиобратимой (AlNashef et al., 2002). Для апротонных RTIL отсутствует дальнейший перенос электронов из-за присутствия супероксида.Напротив, для протонных RTIL супероксид является сильным нуклеофилом, который может далее реагировать с протонами в RTIL с образованием пер-гидроксильного радикала (HO2 ·) (уравнение 8). Затем пер-гидрокси-радикал может также реагировать с супероксидом с образованием пероксида (HO2-) (уравнения 9, 10) и, наконец, завершить процесс восстановления (уравнение 11).
O2 + e− → O2⋅− (7) O2⋅− + H + → HO2⋅ (8) HO2⋅ + O2⋅− → HO2− + O2 (9) HO2⋅ + e− → HO2− (10) HO2− + H + → h3O2 (11)Что касается того, может ли перекись водорода разлагаться на H 2 O, Зеллер (2011) указывает, что это определяется используемым электродом.Согласно Kar et al. (2014) краткое изложение реакций восстановления кислорода и осаждения кислорода в RTIL, в реакции, как упоминалось выше, пути оказались обратимыми и относительно стабильными продуктами пероксида. Однако все еще есть некоторые связанные реакции диспропорционирования. Перекись водорода требует меньше энергии активации для производства кислорода, что делает ее эффективной поддержкой для восстановления кислорода и реакций выделения кислорода в RTIL.
Разработка RTIL в Zn-воздушной батарее все еще сталкивается с огромными проблемами.С одной стороны, высокая стоимость RTIL затрудняет использование в больших масштабах. С другой стороны, двухэлектронный реакционный механизм RTIL снижает удельную энергию батареи в сочетании с ее высокой вязкостью и низкой проводимостью, что означает, что Zn-воздушная батарея может работать только при низком токе. Используя Li 0,87 Na 0,63 K 0,50 CO 3 и NaOH в качестве электролита, Liu et al. (2017) исследовали Zn-воздушную батарею, способную заряжаться и разряжаться при 550 ° C в течение 100 циклов с кулоновской эффективностью 96.9%. Когда Ingale et al. (2017) применили ионную жидкость трифторметансульфонат диэтилметиламмония (DEATfO) к Zn-воздушной батарее, они обнаружили, что, хотя образования дендритов цинка не было, слабое поверхностное натяжение DEATfO привело к неудовлетворительной плотности энергии (Pozo-Gonzalo et al., 2014). Кроме того, Ghazvini et al. (2018) указали на положительное влияние добавления воды на ионное взаимодействие при использовании электролита RTIL в Zn-воздушных батареях. Вышеупомянутая работа представляет собой хорошую стратегию для улучшения характеристик Zn-воздушной батареи с RTIL в качестве электролита.
Кроме того, следует изучить возможность применения большего количества типов RTIL в Zn-воздушных батареях, включая положительные эффекты добавок в RTIL. Также необходимо разработать специальные бифункциональные катализаторы для снижения энергетического барьера реакции восстановления кислорода и реакции выделения кислорода. Хотя электролит RTIL требует дальнейшего изучения с точки зрения свойств интерфейса, механизма электрохимической реакции кислорода и пути миграции активных веществ, различные свидетельства указывают на то, что RTIL являются многообещающими электролитами для Zn-воздушных батарей.
Квазитвердый гибкий электролит
В связи с растущим спросом на гибкие носимые электронные устройства, исследования гибких батарей, особенно квазитвердых электролитов, выдвинули более высокие требования. По сравнению с другими металл-воздушными батареями, Zn-воздушные батареи с высокой объемной плотностью энергии обладают характеристиками низкой стоимости и высокой безопасности. Напротив, цинк в качестве электрода имеет более энергетические механические свойства и производительность в гибких батареях. Например, батареи Zn – MnO 2 , в которых используются полимерные электролиты, были коммерчески произведены с использованием технологии печати (MacKenzie and Ho, 2015).Следовательно, необходимо проводить научные исследования структуры и характеристик гибкой Zn-воздушной батареи, а производство этого типа батареи и соответствующего квазитвердого электролита необходимо постоянно оптимизировать.
Квазитвердый гибкий электролит обычно получают из щелочного водного раствора и полимеров, таких как поливиниловый спирт (ПВС) (Fan et al., 2019), полиакриловая кислота (PAA) (Wu et al., 2006; Zhu et al., 2018), желатин (Park et al., 2015) и родственный им привитой сополимер (Yu et al., 2017), которые необходимы для обеспечения стабильной конфигурации, разделения катода и анода и квалифицированной ионной проводимости. В процессе приготовления большинство квазитвердых гибких электролитов могут образовывать сшитую сеть с большим количеством гидрофильных функциональных групп (таких как гидроксильные группы), что обеспечивает более высокое удержание воды и ионную проводимость в квазитвердых гибких электролитах. В первичной Zn-воздушной ячейке щелочной гелевый электролит может эффективно уменьшить утечку и улетучивание электролита, и был применен (Hilder et al., 2009). Однако для перезаряжаемых гибких Zn-воздушных батарей из-за цинкового электрода в квазитвердом гибком электролите они могут нести лишь небольшое количество Zn (OH) 42-. Блокируется процесс восстановления ZnO до Zn (OH) 42- (Xu et al., 2015). Поэтому создание перезаряжаемых Zn-воздушных батарей для работы с большим током является большой проблемой.
Гибкая удельная мощность и циклическая производительность Zn-воздушной батареи были высоко оценены. Однако есть несколько важных аспектов бифункционального катализатора электрохимических кислородных реакций, ионной проводимости квазитвердого гибкого электролита и характеристик границы раздела электролит-электрод.Ионная проводимость электролита зависит в основном от типа полимера и добавок к электролиту. Fan et al. (2019) приготовили пористый электролит ПВС + SiO 2 с высокой ионной проводимостью 57,3 мСм · см −1 , отличными характеристиками циклирования и удельной мощностью. Ли и др. (2019) изготовили полимерный диэлектрик TEAOH-PVA, который через 2 недели все еще имел ионную проводимость 30 мСм · см −1 , демонстрируя отличные эксплуатационные характеристики и срок службы. Нетрудно обнаружить, что отдельный полимер вряд ли может стать гибким электролитом квазитвердого состояния с превосходными характеристиками.Однако небольшое количество добавок может значительно улучшить характеристики электролитов, что также является процессом функционализации полимера. Это происходит главным образом потому, что добавка оптимизирует структуру сшитой сетки полимерного электролита, увеличивает количество гидрофильных функциональных групп (таких как гидроксильные группы) и дополнительно улучшает способность электролита удерживать воду, что имеет большое влияние на ионную проводимость. Более того, помимо ионной проводимости и характеристик удержания воды квазитвердого гибкого электролита, следует уделять больше внимания скорости переноса OH — и Zn (OH) 42-, которой уделялось недостаточно внимания при настоящее время.Процесс их переноса также оказывает сильное влияние на плотность энергии и другие характеристики гибких Zn-воздушных батарей.
Перед гибкой Zn-воздушной батареей стоит задача улучшить характеристики границы раздела электролит – электрод (особенно границы электролит – воздух). Смачиваемость квазитвердого гибкого электролита была снижена, что значительно затрудняет выполнение катализатором своей функции, чем в щелочном электролите водной системы.При сборке аккумулятора Xu et al. (2019) прессовали батарею в течение 3 минут при давлении 3 МПа с помощью таблеточного пресса, чтобы сделать ламинированную структуру более полной, а гибкая Zn-воздушная батарея могла стабилизировать циркуляцию в течение 35 часов. По-прежнему необходимы дополнительные исследования для улучшения границы раздела электролит-электрод, подготовки электролита и метода упаковки батареи.
Гибкая Zn-воздушная батарея также выдвигает более высокие требования к характеристикам изгиба, растяжения и сжатия цинкового электрода, воздушного электрода и электролита в батарее.Гибкая Zn-воздушная батарея обычно подразделяется на 1D-структуру (линейный тип) и 2D-структуру (сэндвич-форму). Ma et al. (2019) подготовили гидрогелевый электролит с двойной сеткой (полиакрилатный гидрогель, сшитый цепями целлюлозы и N, N-метилен-бисакриламидными якорями) и оптимизировали структуру цинковых и воздушных электродов для сборки Zn-воздушной батареи с превосходными характеристиками растяжения. Pan et al. (2019) сконструировали губчатую сжимаемую Zn-воздушную батарею, которая хорошо себя показала после 60% деформации сжатия или 500 циклов повторных испытаний на сжатие.Ли и др. (2018) приготовили одномерную вязанную Zn-воздушную батарею с диаметром всего 1,03 мм через путь, которая имела отличные характеристики гибкости, заряда и разряда.
В Таблице 2 перечислены более сравниваемые характеристики, чтобы предоставить более значимые пути разработки квазитвердых гибких электролитов для Zn-воздушных аккумуляторов. Однако получить компетентную оценку сложно из-за различной конструкции батареи, катализатора и электролита, используемых в записанных работах. Следовательно, необходимо установить единый стандарт оценки для гибкой Zn-воздушной батареи, чтобы лучше оценивать характеристики соответствующего электролита.Кроме того, состав электролита в гибкой Zn-воздушной батарее в основном находится в режиме «полимер + раствор КОН», что приводит к преимуществам и недостаткам упомянутого выше водного электролита, действующего на квазитвердый электролит. В то же время комбинация RTIL с полимером может придать новый импульс безопасности и стабильности Zn-воздушных батарей, но ее практическая осуществимость должна быть проверена в ближайшем будущем.
Таблица 2 .Краткое изложение недавно опубликованной квазитвердой добавки к гибкому электролиту для Zn-воздушных батарей.
Сводка
Учитывая потребность в мощных, долговечных и гибких перезаряжаемых Zn-воздушных батареях, разработка электролитов отвечает возможностям и задачам. Электролит, как критическая часть Zn-воздушной батареи, оказывает сильное влияние на эффективность циркуляции, удельную мощность и характеристики емкости. До сих пор щелочные электролиты являются основным направлением из-за их превосходной ионной проводимости и межфазных свойств.Однако щелочные электролиты чувствительны к воздействию содержания углекислого газа и относительной влажности во внешней среде. С одной стороны, следует изучить подходящий тип и пропорцию добавок для улучшения свойств щелочного электролита. С другой стороны, RTIL, как электролит для Zn-воздушных батарей, имеют высокий порог старения, и его защита и безопасность для цинковых электродов очевидны. Более того, исследования квазитвердого гибкого электролита в большей степени способствуют созданию портативных и гибких Zn-воздушных батарей, которые обеспечивают устранение недостатков в характеристиках интерфейса и ионной проводимости.Подбор подходящих RTIL и полимеров имеет смысл улучшить характеристики электролита.
Кроме того, мы думаем, что три упомянутых выше электролита могут иметь разные характеристики. Подходящие добавки к электролиту могут также способствовать применению RTIL и квазитвердых электролитов в Zn-воздушных батареях, а комбинация RTIL и полимеров также может улучшить характеристики электролитов. Следует уделять больше внимания исследованиям электролитов, чтобы воздушно-цинковые батареи отвечали требованиям нового поколения аккумуляторов энергии.
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Финансирование
Работа выполнена при финансовой поддержке Китайского фонда естественных наук (U1832136, 21303038), Национальной программы обучения студентов инновациям и предпринимательству (2019010) и Фонда естественных наук провинции Аньхой (1808085QE140).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
АльНашеф И. М., Леонард М. Л., Мэтьюз М. А. и Вайднер Дж. У. (2002). Электрохимия супероксида в ионной жидкости. Ind. Eng. Chem. Res. 41, 4475–4478. DOI: 10.1021 / ie010787h
CrossRef Полный текст | Google Scholar
Баник, С. Дж., Аколкар, Р. (2013). Подавление роста дендритов при электроосаждении цинка добавкой ПЭГ-200. J. Electrochem. Soc. 160, D519 – D523. DOI: 10.1149 / 2.040311jes
CrossRef Полный текст | Google Scholar
Чаккараварти, К., Вахид А.А. и Удупа Х. (1981). Цинково-воздушные щелочные батареи — обзор. J. Источники энергии 6, 203–228. DOI: 10.1016 / 0378-7753 (81) 80027-4
CrossRef Полный текст | Google Scholar
Чамун, М., Герцберг, Б. Дж., Гупта, Т., Дэвис, Д., Бхадра, С., Ван Тасселл, Б., и др. (2015). Гипердендритные нанопористые аноды из цинковой пены. NPG Asia Mater. 7: e178. DOI: 10.1038 / am.2015.32
CrossRef Полный текст | Google Scholar
Чен, X., Лю, Б., Чжун, К., Лю, З., Лю, Дж., Ма, Л. и др. (2017). Ультратонкий Co 3 O 4 слоев с большой площадью контакта на углеродных волокнах в качестве высокоэффективного электрода для гибкой воздушно-цинковой батареи, интегрированной с гибким дисплеем. Adv. Energy Mater. 7: 1700779. DOI: 10.1002 / aenm.201700779
CrossRef Полный текст | Google Scholar
Cheng, J., Zhang, L., Yang, Y.-S., Wen, Y.-H., Cao, G.-P., and Wang, X.-D. (2007). Предварительные исследования однопоточной цинк-никелевой батареи. Электрохим. Commun. 9, 2639–2642. DOI: 10.1016 / j.elecom.2007.08.016
CrossRef Полный текст | Google Scholar
Chou, S.-L., Wang, J.-Z., Sun, J.-Z., Wexler, D., Forsyth, M., Liu, H.-K., et al. (2008). Высокая емкость, безопасность и улучшенная циклируемость литий-металлической батареи с использованием катода из наноматериала V 2 O 5 и ионно-жидкого электролита при комнатной температуре. Chem. Матер. 20, 7044–7051. DOI: 10,1021 / см801468q
CrossRef Полный текст | Google Scholar
Дайер, К.К., Мозли П. Т., Огуми З., Рэнд Д. А. и Скросати Б. (2009). Энциклопедия электрохимических источников энергии. (Newnes: Elsevier Science & Technology).
Google Scholar
Фан, X., Лю, Дж., Сун, З., Хань, X., Дэн, Ю., Чжун, К., и др. (2019). Пористый нанокомпозитный гелевый полимерный электролит с высокой ионной проводимостью и превосходной способностью удерживать электролит для гибких воздушно-цинковых батарей с длительным сроком службы. Nano Energy 56, 454–462.DOI: 10.1016 / j.nanoen.2018.11.057
CrossRef Полный текст | Google Scholar
Фань, X., Ян, Z., Xie, X., Long, W., Wang, R., and Hou, Z. (2013). Электрохимическое поведение Zn – Al – La-гидроталькита во вторичных ячейках Zn-Ni. J. Источники энергии 241, 404–409. DOI: 10.1016 / j.jpowsour.2013.04.136
CrossRef Полный текст | Google Scholar
Фу, Дж., Кано, З. П., Парк, М. Г., Ю, А., Фаулер, М., и Чен, З. (2017). Электрически перезаряжаемые воздушно-цинковые батареи: прогресс, проблемы и перспективы. Adv. Матер. 29: 1604685. DOI: 10.1002 / adma.201604685
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Fu, J., Lee, D. U., Hassan, F. M., Yang, L., Bai, Z., Park, M. G., et al. (2015). Гибкие высокоэнергетические аккумуляторные воздушно-цинковые батареи на полимерно-электролитной основе. Adv. Матер. 27, 5617–5622. DOI: 10.1002 / adma.201502853
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Газвини, М.С., Пуллетикурти, Г., Цуй, Т., Кул, К., и Эндрес, Ф. (2018). Электроосаждение цинка из смесей ацетата 1-этил-3-метилимидазолия и воды: исследования применимости электролита для Zn-воздушных батарей. J. Electrochem. Soc. 165: D354. DOI: 10.1149 / 2.0181809jes
CrossRef Полный текст | Google Scholar
Гольдштейн, Дж. Р., Харац, Ю., Шарон, Ю., и Наймер, Н. (1997). Система скруббера для удаления углекислого газа из металлической батареи или батареи топливных элементов. Патент США №5,595,949. (Вашингтон, округ Колумбия: патентная заявка Управления США по патентам и товарным знакам).
Google Scholar
Гуань К., Сумбоджа А., Занг В., Цянь Ю., Чжан Х., Лю X. и др. (2019). Декорирование наночастиц Co / CoNx в углеродных наночастицах, легированных азотом, для гибких и перезаряжаемых воздушно-цинковых батарей. Energy Storage Mater. 16, 243–250. DOI: 10.1016 / j.ensm.2018.06.001
CrossRef Полный текст | Google Scholar
Хан, Дж., Мэн, X., Лу, Л., Биан, Дж., Ли, З., и Сан, К. (2019). Одноатомный Fe-Nx-C как эффективный электрокатализатор для цинково-воздушных аккумуляторов. Adv. Функц. Матер. 29: 1808872. DOI: 10.1002 / adfm.201808872
CrossRef Полный текст | Google Scholar
Хартинг, К., Кунц, У., Турек, Т. (2012). Цинково-воздушные батареи: перспективы и проблемы для дальнейшего совершенствования. Z. Phys. Chem. 226, 151–166. DOI: 10.1524 / zpch.2012.0152
CrossRef Полный текст | Google Scholar
Гильдер, М., Винтер-Йенсен, Б., и Кларк, Н. (2009). Бумажная, печатная воздушно-цинковая батарея. J. Источники энергии 194, 1135–1141. DOI: 10.1016 / j.jpowsour.2009.06.054
CrossRef Полный текст | Google Scholar
Хоссейни С., Аббаси А., Уджинет Л.-О., Хаустраэте Н., Прасертдам С., Йонезава Т. и др. (2019). Влияние диметилсульфоксида как добавки к электролиту на анодное растворение щелочной цинково-воздушной аккумуляторной батареи. Sci. Rep. 9: 14958. DOI: 10.1038 / s41598-019-51412-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хоссейни, С., Хан, С. Дж., Арпонвичаноп, А., Йонедзава, Т., и Кхеахом, С. (2018). Этанол в качестве добавки к электролиту для щелочных воздушно-цинковых батарей. Sci. Rep. 8: 11273. DOI: 10.1038 / s41598-018-29630-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, Дж., Ян, З., Ван, Р., Чжан, З., Фэн, З., и Се, X. (2015). Слоистые двойные оксиды Zn-Al в качестве высокоэффективных анодных материалов для вторичных батарей на основе цинка. J. Mater. Chem. А 3, 7429–7436.DOI: 10.1039 / C5TA00279F
CrossRef Полный текст | Google Scholar
Якованджело, К. Д., Уилл, Ф. Г. (1985). Параметрическое исследование осаждения цинка на пористом углероде в ячейке с проточным электролитом. J. Electrochem. Soc. 132: 851.
Google Scholar
Ингейл П., Сакхивел М. и Дриллет Дж. Ф. (2017). Испытание ионной жидкости трифторметансульфоната диэтилметиламмония в качестве электролита в электрически перезаряжаемой Zn / воздушной батарее. Дж.Электрохим. Soc. 164, H5224 – H5229. DOI: 10.1149 / 2.0351708jes
CrossRef Полный текст | Google Scholar
Кар, М., Саймонс, Т. Дж., Форсайт, М., и Макфарлейн, Д. Р. (2014). Ионные жидкие электролиты как платформа для перезаряжаемых металло-воздушных батарей: перспектива. Phys. Chem. Chem. Phys. 16, 18658–18674. DOI: 10.1039 / C4CP02533D
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кумар, К. К., Бринда, Р., Нандхини, М., Селвам, М., Саминатан, К., и Шактипанди, К. (2019). Взвешенный в воде графен в качестве добавки к электролиту в системе цинково-воздушных щелочных батарей. Ionics 25, 1699–1706. DOI: 10.1007 / s11581-019-02924-7
CrossRef Полный текст | Google Scholar
Лан, К., Ли, К., и Чин, Т. (2007). Гидроксиды тетраалкиламмония как ингибиторы дендрита цинка во вторичных батареях на основе цинка. Электрохим. Acta 52, 5407–5416. DOI: 10.1016 / j.electacta.2007.02.063
CrossRef Полный текст | Google Scholar
Ли, К.W., Sathiyanarayanan, K., Eom, S. W., Kim, H. S., and Yun, M. S. (2006). Новое электрохимическое поведение цинковых анодов в цинково-воздушных батареях в присутствии добавок. J. Источники энергии 159, 1474–1477. DOI: 10.1016 / j.jpowsour.2005.11.074
CrossRef Полный текст | Google Scholar
Li, M., Liu, B., Fan, X., Liu, X., Liu, J., Ding, J., et al. (2019). Полимерный электролит длительного хранения на основе гидроксида тетраэтиламмония для гибких воздушно-цинковых аккумуляторов. ACS Appl.Матер. Интерфейсы 11, 28909–28917. DOI: 10.1021 / acsami.9b09086
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, М., Ло, Ф., Чжан, К., Ян, З. и Сюй, З. (2020). Нанолисты атомарного слоя Co3O4-x как эффективный и стабильный электрокатализатор для аккумуляторных воздушно-цинковых батарей. Дж. Катал . 381, 395–401. DOI: 10.1016 / j.jcat.2019.11.020
CrossRef Полный текст | Google Scholar
Ли Ю., Чжун, К., Лю, Дж., Цзэн, X., Цюй, С., Han, X., et al. (2018). Атомарно тонкий мезопористый Co 3 O 4 слоев, прочно связанных с нанолистами N-rGO, в качестве высокоэффективных бифункциональных катализаторов для одномерных связываемых цинковоздушных батарей. Adv. Матер. 30, 1703657. doi: 10.1002 / adma.201703657
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю С., Хань В., Цуй Б., Лю X., Чжао Ф., Стюарт Дж. И др. (2017). Новый перезаряжаемый воздушно-цинковый аккумулятор с расплавленным солевым электролитом. J. Источники энергии 342, 435–441. DOI: 10.1016 / j.jpowsour.2016.12.080
CrossRef Полный текст | Google Scholar
Ma, L., Chen, S., Wang, D., Yang, Q., Mo, F., Liang, G., et al. (2019). Суперэластичные воздушно-цинковые батареи на основе щелочно-толерантного двухсетевого гидрогелевого электролита. Adv. Energy Mater. 9: 1803046. DOI: 10.1002 / aenm.201803046
CrossRef Полный текст | Google Scholar
Маккензи, Дж. Д., и Хо, К. (2015). Перспективы накопления энергии для гибких электронных систем. P. IEEE 103, 535–553. DOI: 10.1109 / JPROC.2015.2406340
CrossRef Полный текст | Google Scholar
Майнар, А. Р., Ируин, Э., Кольменарес, Л. К., Кваша, А., де Меатза, И., Бенгоэча, М., и др. (2018). Обзор достижений электролитов для вторичных воздушно-цинковых батарей и других систем хранения на основе цинка. J. Хранение энергии 15, 304–328. DOI: 10.1016 / j.est.2017.12.004
CrossRef Полный текст | Google Scholar
Майнар, Р.А., Леонет, О., Бенгоэча, М., Бояно, И., де Меатза, И., и др. (2016). Водно-щелочные электролиты для вторичных цинково-воздушных аккумуляторов: обзор. Внутр. J. Energy Res. 40, 1032–1049. DOI: 10.1002 / er.3499
CrossRef Полный текст | Google Scholar
Масри, М. Н., и Мохамад, А. А. (2013). Эффект добавления технического углерода к пористому цинковому аноду в воздушно-цинковой батарее. J. Electrochem. Soc. 160, A715 – A721. DOI: 10.1149 / 2.007306jes
CrossRef Полный текст | Google Scholar
Мяо, Х., Chen, B., Li, S., Wu, X., Wang, Q., Zhang, C., et al. (2020). Полностью твердотельный гибкий воздушно-цинковый аккумулятор с полиакриламидным щелочно-гелевым электролитом. J. Источники энергии 450: 227653. DOI: 10.1016 / j.jpowsour.2019.227653
CrossRef Полный текст | Google Scholar
Пан, З., Янг, Дж., Занг, В., Коу, З., Ван, К., Дин, X., et al. (2019). Полностью твердотельный губчатый сжимаемый воздушно-цинковый аккумулятор. Energy Storage Mater. 23, 375–382. DOI: 10.1016 / j.ensm.2019.04.036
CrossRef Полный текст | Google Scholar
Парк, Дж., Парк, М., Нам, Г., Ли, Дж. С. и Чо, Дж. (2015). Полностью твердотельная гибкая воздушно-цинковая батарея кабельного типа. Adv. Матер. 27, 1396–1401. DOI: 10.1002 / adma.201404639
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Паркер, Дж. Ф., Червин, К. Н., Нельсон, Э. С., Ролисон, Д. Р., и Лонг, Дж. У. (2014). Трехмерная разводка цинка меняет характеристики батареи — цикл без дендритов. Energy Environ. Sci. 7, 1117–1124. DOI: 10.1039 / C3EE43754J
CrossRef Полный текст | Google Scholar
Pedicini, C., Sieminski, D. P., Skeggs, L. T., Young, J. E., and Cherry, E. C. (1996). Система управления воздухом для рециркуляции реактивного воздуха в металло-воздушной батарее. Патент США № 5,560,999. Вашингтон, округ Колумбия: заявка на патент Управления по патентам и товарным знакам США.
Google Scholar
Pedicni, C. S. (2002). Воздушная заслонка для электрохимической ячейки, реагирующая на нагрузкуПатент США №6,350,537. Вашингтон, округ Колумбия: заявка на патент в Ведомстве США по патентам и товарным знакам.
Google Scholar
Пей П., Ван К. и Ма З. (2014). Технологии продления срока службы воздушно-цинковых батарей: обзор. Прил. Энергия 128, 315–324. DOI: 10.1016 / j.apenergy.2014.04.095
CrossRef Полный текст | Google Scholar
Посо-Гонсало, К., Вирджилио, К., Ян, Ю., Хоулет, П. К., Бирн, Н., МакФарлейн, Д. Р., и др. (2014). Повышенная эффективность ионных жидкостей на основе фосфония в отношении реакции восстановления кислорода с 4 электронами при добавлении слабого источника протонов. Электрохим. Commun. 38, 24–27. DOI: 10.1016 / j.elecom.2013.10.004
CrossRef Полный текст | Google Scholar
Шредер Д., Боркер Н. С., Кёниг М. и Кревер У. (2015). Характеристики воздушно-цинковых батарей с добавлением K 2 CO 3 в щелочном электролите. J. Appl. Электрохим. 45, 427–437. DOI: 10.1007 / s10800-015-0817-0
CrossRef Полный текст | Google Scholar
См. Д. М. и Уайт Р. Э. (1997).Температурная и концентрационная зависимость удельной проводимости концентрированных растворов гидроксида калия. J. Chem. Англ. Данные 42, 1266–1268. DOI: 10.1021 / je970140x
CrossRef Полный текст | Google Scholar
Шинде, С.С., Ли, К.Х., Юнг, Ж.-Й., Ваг, Н.К., Ким, С.-Х., Ким, Д.-Х., и др. (2019). Презентация двухзвенных металлоорганических каркасов из гексаиминобензола в 3D для создания долговечных усовершенствованных обратимых Zn-воздушных батарей. Energy Environ. Sci. 12, 727–738. DOI: 10.1039 / c8ee02679c
CrossRef Полный текст | Google Scholar
Саймонс Т., Торриеро А., Хоулетт П., Макфарлейн Д. Р. и Форсайт М. (2012). Высокая плотность тока, эффективное циклирование Zn 2+ в ионной жидкости дицианамида 1-этил-3-метилимидазолия: влияние концентрации соли и воды Zn 2+ . Электрохим. Commun. 18, 119–122. DOI: 10.1016 / j.elecom.2012.02.034
CrossRef Полный текст | Google Scholar
Тан, П., Chen, B., Xu, H., Zhang, H., Cai, W., Ni, M., et al. (2017). Гибкие Zn- и Li-air аккумуляторы: последние достижения, проблемы и перспективы на будущее. Energy Environ. Sci. 10, 2056–2080. DOI: 10.1039 / c7ee01913k
CrossRef Полный текст | Google Scholar
Ван К., Пей П., Ма З., Сюй Х., Ли П. и Ван X. (2014). Контроль морфологии регенерации цинка для воздушно-цинковых топливных элементов и батарей. J. Источники энергии 271, 65–75. DOI: 10.1016 / j.jpowsour.2014.07.182
CrossRef Полный текст | Google Scholar
Ван В., Тан М., Чжэн З. и Чен С. (2019). Ультратонкий, гибкий и высокопроизводительный твердотельный Zn-воздушный аккумулятор на основе щелочно-полимерной мембраны. Adv. Energy Mater. 9, 1803628. doi: 10.1002 / aenm.201803628
CrossRef Полный текст | Google Scholar
Ван, X., Сунарсо, Дж., Лу, К., Чжоу, З., Дай, Дж., Гуань, Д., и др. (2020). Высокопроизводительный бифункциональный кислородный электрокатализатор из платино-перовскитного композитного материала для аккумуляторных Zn-воздушных батарей. Adv. Энергетика . 10: 11. DOI: 10.1002 / aenm.2011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ву Г., Линь С. и Ян К. (2006). Щелочные Zn-воздушные и Al-воздушные ячейки на основе новых твердотельных полимерных электролитных мембран ПВС / ПАА. J. Membr. Sci. 280, 802–808. DOI: 10.1016 / j.memsci.2006.02.037
CrossRef Полный текст | Google Scholar
Xiang, H., Yin, B., Wang, H., Lin, H., Ge, X., Xie, S., et al. (2010).Улучшение электрохимических свойств электролита на основе ионной жидкости комнатной температуры (RTIL) для литий-ионных аккумуляторов. Электрохим. Acta 55, 5204–5209. DOI: 10.1016 / j.electacta.2010.04.041
CrossRef Полный текст | Google Scholar
Xu, L., Liu, J., Chen, P., Wang, Z., Tang, D., Liu, X., et al. (2020). Мощные водные батареи Zn-h3O2 для широкого применения. Cell Rep. Phys. Sci . 1: 100027. DOI: 10.1016 / j.xcrp.2020.100027
CrossRef Полный текст | Google Scholar
Сюй, М., Айви, Д., Се, З., и Цюй, В. (2015). Перезаряжаемые Zn-воздушные батареи: прогресс в разработке электролитов и улучшении конфигурации элементов. J. Источники энергии 283, 358–371. DOI: 10.1016 / j.jpowsour.2015.02.114
CrossRef Полный текст | Google Scholar
Xu, N., Zhang, Y., Wang, M., Fan, X., Zhang, T., Peng, L., et al. (2019). Высокопроизводительные перезаряжаемые / гибкие воздушно-цинковые батареи с координированным иерархическим биметаллическим электрокатализатором и гетероструктурной анионообменной мембраной. Nano Energy 65: 104021. DOI: 10.1016 / j.nanoen.2019.104021
CrossRef Полный текст | Google Scholar
Янь З., Ван Э., Цзян Л. и Сунь Г. (2015). Превосходная циклическая стабильность и высокая производительность трехмерных электродов из вспененного цинка / меди для щелочных батарей на основе цинка. RSC Adv. 5, 83781–83787. DOI: 10.1039 / C5RA16264E
CrossRef Полный текст | Google Scholar
Ян, Х., Цао, Й., Ай, X., и Сяо, Л. (2004). Повышенная разрядная способность и подавление пассивации поверхности цинкового анода в разбавленном щелочном растворе с использованием поверхностно-активных добавок. J. Источники энергии 128, 97–101. DOI: 10.1016 / j.jpowsour.2003.09.050
CrossRef Полный текст | Google Scholar
Yu, M., Wang, Z., Hou, C., Wang, Z., Liang, C., Zhao, C., et al. (2017). Co 3 O 4 мезопористые нанопроволочные массивы, легированные азотом, в качестве воздушного катода без добавок для гибких твердотельных воздушно-цинковых батарей. Adv. Матер. 29: 1602868. DOI: 10.1002 / adma.201602868
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Целлер Р.А. (2011). Влияние внешней и внутренней активности протонов на механизм восстановления кислорода в ионных жидкостях . (Темп, Аризона: Государственный университет Аризоны, ProQuest Dissertations Publishing).
Google Scholar
Чжун, X., И, В., Цюй, Ю., Чжан, Л., Бай, Х., Чжу, Ю., и др. (2020). Одноатомный атом Co закреплен на Co3O4 и активированном угле, легированном азотом, в направлении бифункционального катализатора для воздушно-цинковых батарей. Заявл. Catal., B 260, 118188. DOI: 10.1016 / j.apcatb.2019.118188
CrossRef Полный текст | Google Scholar
Zhu, L., Zheng, D., Wang, Z., Zheng, X., Fang, P., Zhu, J., et al. (2018). Стратегия ограничения для стабилизации бифункциональных катализаторов на основе ZIF в качестве эталонного катода гибких полностью твердотельных цинково-воздушных батарей. Adv. Матер. 30: e1805268. DOI: 10.1002 / adma.201805268
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Оценка отложений никеля, полученных с помощью электролита Уоттса при температуре окружающей среды
DiBari, GA, «Хронология никелевого гальванического покрытия». Металлическая отделка. , 100 34–49 (2002)
CAS Статья Google Scholar
Институт никеля (2007) http://www.nickelinstitute.org.
Центнер, В., Бреннер, А., Дженнингс, К.В., «Физические свойства электроосажденных металлов». Покрытие , 39 865–894 (1953)
Google Scholar
Lowenheim, FA, Гальваника . Макгроу-Хилл, Нью-Йорк (1978)
Google Scholar
Пуллицци, Т.Дж., «Устранение неисправностей в современных решениях для блестящего никелирования». Finishing.com, http://www.finishing.com/Library/brightnickel.html, (1988).
Мандич, Н.В., Гедулд, Х, «Понимание и устранение неисправностей в системах декоративного никелевого гальванического покрытия — Часть I: Введение и проблемы яркости». Обработка металлов , 100 83–91 (2002)
CAS Статья Google Scholar
Mest, GT, «Никелирование и устранение неисправностей». PFOnline.com, http://www.pfonline.com/articles/pfdmest01.html, (2008 г.).
Pourbaix, M, Атлас электрохимических равновесий в водных растворах . Pergamon Press, Лондон (1974)
Google Scholar
Беверског, Б., Пуигдоменек, И. «Пересмотренные диаграммы Пурбе для никеля при 25–300 ° C». Коррос. Sci. , 39 969–980 (1997)
CAS Статья Google Scholar
Гер, доктор медицины, «Электрохимическое осаждение композитов никель / SiC в присутствии поверхностно-активных веществ». Mater. Chem. Phys. , 87 67–74 (2004)
CAS Статья Google Scholar
Бадарулзаман, Н.А., Пурвадария, С., Мохамад, А.А., Ахмад, З.А., «Производство никель-глиноземного композитного покрытия с помощью гальваники». Ionics , 15 603–607 (2009)
CAS Статья Google Scholar
Гофер, А., «Процесс поддержки и очистки сетчатого анодного мешка». Патент США 5431823, 1995.
Аал, А.А., Ибрагим, К.М., Хамид, З.А., «Повышение износостойкости ковкого чугуна с помощью композитного покрытия Ni – SiC». Износ , 260 1070–1075 (2006)
Артикул Google Scholar
Benea, L, Wenger, F, Ponthiaux, P, Celis, JP, «Поведение наноструктурированных композитных покрытий Ni / SiC, полученных методом электроосаждения, при трибокоррозии.” Износ , 266 398–405 (2008)
Артикул Google Scholar
Бинь-ши, Х, Хай-доу, В., Ши-юнь, Д, Бин, Дж, Вэй-й, Т., «Электроосаждение никелево-кремнеземных нанокомпозитных покрытий». Электрохим. Commun. , 7 572–575 (2005)
Артикул Google Scholar
Фэн, Кью, Ли, Т, Чжан, З., Чжан, Дж, Лю, М., Джин, Дж, «Получение наноструктурированных Ni / Al 2 O 3 Композитных покрытий в сильном магнитном поле .” Surf. Пальто. Technol. , 201 6247–6252 (2007)
CAS Статья Google Scholar
Моханти, США, Трипати, Британская Колумбия, Дас, Южная Каролина, Мисра, В.Н., «Влияние тиомочевины во время электроосаждения никеля из кислых сульфатных растворов». Металл. Матер. Пер. B , 36B 737–741 (2005)
CAS Статья Google Scholar
Кубишталь, Дж., Будниок, А., Ласия, А., «Исследование реакции оценки водорода на композиционных покрытиях на основе никеля, содержащих порошок молибдена». Внутр. J. Hydrogen Energy , 32 1211–1218 (2007)
CAS Статья Google Scholar
Попов К.И., Джокич С.С., Гргур Б.Н., Фундаментальные аспекты электрометаллургии . Kluwer Academic / Plenum Publishers, Нью-Йорк (2004)
Google Scholar
Белоглазов С.М. Поглощение водорода сталью при травлении и гальванике. Физико-химическая механика материалов , 1 283–288 (1965)
КАС Google Scholar
Миркова, Л., Маурин, Г., Монев, М., Цветкова, С, «Коэволюция водорода, проницаемость при гальванике никеля». J. Appl. Электрохим. , 33 93–100 (2003)
CAS Статья Google Scholar
Aruna, ST, Bindu, CN, Selvi, VE, Grips, VKW, Rajam, KS, «Синтез, свойства электроосажденных нанокомпозитных покрытий Ni / церия, синтез и свойства электроосажденных нанокомпозитных покрытий Ni / Ceria». Surf. Пальто. Technol. , 200 6871–6880 (2006)
CAS Статья Google Scholar
Ганеш, В., Виджаярагхаван, Д., Лакшминараянан, В., «Рост мелких зерен никелевого электроосаждения: влияние приложенного магнитного поля во время осаждения».” Appl. Прибой. Sci. , 240 286–295 (2005)
CAS Статья ОБЪЯВЛЕНИЯ Google Scholar
Gheorghies, C, Carac, G, Stasi, V, «Приготовление, структурная характеристика композиционных покрытий из наночастиц никеля и оксида алюминия». J. Optoelectr. Adv. Матер. , 8 1234–1237 (2006)
CAS Google Scholar
Li, Y, Jiang, H, Huang, W, Tian, H, «Влияние пиковой плотности тока на механические свойства нанокристаллических сплавов Ni – Co, полученных методом импульсного электроосаждения». Заявл. Прибой. Sci. , 254 6865–6869 (2008)
CAS Статья ОБЪЯВЛЕНИЯ Google Scholar
Линс, VFC, Чекконелло, ES, Матенсио, Т., «Влияние плотности тока на морфологию, пористость и трибологические свойства электроосажденного никеля на меди.” J. Mater. Англ. Выполнять. , 17 741–745 (2008)
CAS Статья Google Scholar
Чао-цюнь, Л., Синь-хай, Л., Чжи-син, В., Хуа-цзюнь, Г., «Электроосаждение никеля из новой цитратной ванны». Пер. Цветной металл Soc. Китай , 17 1300–1306 (2007)
Артикул Google Scholar
Простой метод изготовления гибких электролитных листов на керамической основе для литий-металлических батарей
В ближайшем будущем литий-металлические батареи с гибким листом электролита LLZO могут быть использованы в современных электромобилях (электромобилях).Предоставлено: Токийский столичный университет.Исследователи из Токийского столичного университета разработали новый метод изготовления гибких электролитных листов на керамической основе для литий-металлических батарей. Они объединили керамику типа граната, полимерное связующее и ионную жидкость, создав квазитвердый листовой электролит. Синтез осуществляется при комнатной температуре и требует значительно меньше энергии, чем существующие высокотемпературные (> 1000 ° C) процессы. Он работает в широком диапазоне температур, что делает его многообещающим электролитом для аккумуляторов. E.г., в электромобилях.
Ископаемое топливо обеспечивает большую часть мировых потребностей в энергии, включая электричество. Но ископаемое топливо заканчивается, и его сжигание также приводит к прямым выбросам в атмосферу углекислого газа и других загрязняющих веществ, таких как токсичные оксиды азота. В мире существует потребность в переходе на более чистые возобновляемые источники энергии. Но основные источники возобновляемой энергии, такие как ветер и солнечная энергия, часто работают с перебоями: ветер дует не постоянно, а солнце не светит ночью.Таким образом, необходимы современные системы хранения энергии для более эффективного использования возобновляемых периодических источников. Литий-ионные батареи оказали глубокое влияние на современное общество, питая широкий спектр портативной электроники и приборов, таких как беспроводные пылесосы, с момента их коммерциализации Sony в 1991 году. Но использование этих батарей в электромобилях (электромобилях) по-прежнему требует существенного улучшения емкость и безопасность современной литий-ионной технологии.
Это привело к возрождению исследовательского интереса к литий-металлическим батареям: литий-металлические аноды имеют гораздо более высокую теоретическую емкость, чем графитовые аноды, которые сейчас используются в коммерческих целях.По-прежнему существуют технологические препятствия, связанные с анодами из металлического лития. Например, в батареях на жидкой основе могут расти дендриты лития (или рукава), что может вызвать короткое замыкание батареи и даже привести к пожарам и взрывам. Вот где пришли твердотельные неорганические электролиты: они значительно безопаснее, а керамика типа граната (типа структуры) Li 7 La 3 Zr 2 O 12 , более известная как LLZO, является в настоящее время широко рассматривается как многообещающий твердотельный электролит из-за его высокой ионной проводимости и совместимости с металлическим литием.Однако для производства электролитов LLZO с высокой плотностью требуются очень высокие температуры спекания, достигающие 1200 ° C. Это неэффективно с точки зрения энергии и требует много времени, что затрудняет крупномасштабное производство электролитов LLZO. Кроме того, плохой физический контакт между хрупкими электролитами LLZO и материалами электродов обычно приводит к высокому межфазному сопротивлению, что значительно ограничивает их применение в полностью твердотельных литий-металлических батареях.
Исследователи из Токийского столичного университета разработали новый метод изготовления гибких электролитных листов на керамической основе для литий-металлических батарей.Они объединили керамику типа граната, полимерное связующее и ионную жидкость, создав квазитвердотельный листовой электролит. Синтез осуществляется при комнатной температуре и требует значительно меньше энергии, чем существующие высокотемпературные (> 1000 ° C) процессы. Он работает в широком диапазоне температур, что делает его многообещающим электролитом для аккумуляторов, например, в электрические транспортные средства. Предоставлено: Токийский столичный университетТаким образом, группа под руководством профессора Киёси Канамура из Токийского столичного университета приступила к разработке гибкого композитного листового электролита из LLZO, который можно производить при комнатной температуре.Они выливают керамическую суспензию LLZO на тонкую полимерную основу, как масло, намазываемое на тосты. После сушки в вакуумной печи листовой электролит толщиной 75 микрон был пропитан ионной жидкостью (ИЖ) для улучшения его ионной проводимости. ИЖ — это соли, которые являются жидкими при комнатной температуре, известны своей высокой проводимостью, но при этом почти негорючие и нелетучие. Внутри листов ИЖ успешно заполняла микроскопические зазоры в структуре и перекрывала частицы LLZO, создавая эффективный путь для ионов лития.Они также эффективно снижают межфазное сопротивление на катоде. При дальнейшем исследовании они обнаружили, что ионы лития диффундируют как через частицы ИЖ, так и через частицы LLZO в структуре, подчеркивая роль обоих. Синтез прост и подходит для промышленного производства: весь процесс осуществляется при комнатной температуре без необходимости высокотемпературного спекания.
Команда утверждает, что механическая прочность и работоспособность гибкого композитного листа в широком диапазоне температур делает его многообещающим электролитом для литий-металлических батарей.Предоставлено: Токийский столичный университет.Несмотря на то, что проблемы остаются, команда утверждает, что механическая прочность и работоспособность гибкого композитного листа в широком диапазоне температур делает его многообещающим электролитом для литий-металлических батарей. Простота этого нового метода синтеза может означать, что мы увидим на рынке литий-металлические батареи большой емкости раньше, чем мы думаем.
Инновационный метод повышает безопасность литий-серных батарей
Дополнительная информация: Эрик Цзяньфенг Ченг и др., Гибкий листовой электролит на керамической основе для литиевых батарей, ACS Applied Materials & Interfaces (2020).



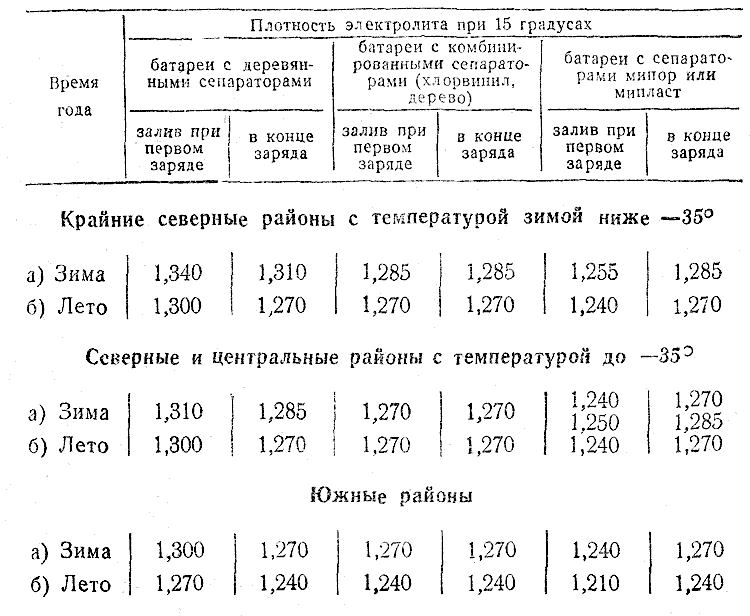
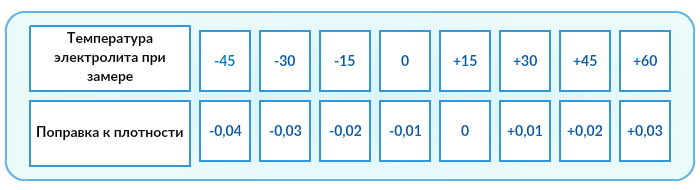 е. с добавкой едкого лития
е. с добавкой едкого лития